Kemi's periodiske system er noget, elever bliver bedt om at lære udenad uden selv at kende det egentlige motiv bag at lære det. For nogle mennesker er det bare et emne, der er inkluderet i deres pensum.
Men i en reel forstand er dette lille periodiske system langt vigtigere end det; det er en køreplan, der åbner en million muligheder for videnskabsmænd og forskere verden over. Dmitri Mendeleyev er opfinderen af det periodiske system.
Før ham prøvede mange hårdt at arrangere kemiske elementer på forskellige måder. Men Dmitris resultat blev accepteret over hele verden.
I videnskabelige forkortelser omtales rækkerne som henholdsvis perioder og kolonnerne som grupper.
Nøgleforsøg
- Perioder er de vandrette rækker i det periodiske system, der angiver antallet af elektronskaller i et grundstofs atomer, hvor grundstoffer i samme periode har lignende atomstrukturer.
- Grupper er de lodrette søjler i det periodiske system, bestående af grundstoffer med det samme antal elektroner i deres ydre skal, hvilket fører til lignende kemiske egenskaber.
- Både perioder og grupper organiserer elementer i det periodiske system, hvor perioder repræsenterer vandrette rækker baseret på elektronskaller og grupper, der repræsenterer lodrette søjler baseret på ydre skalelektroner og kemiske egenskaber.
Periode vs. gruppe
En periode er en vandret række, der går fra venstre side til højre side af det periodiske system, og elektronegativiteten øges på tværs af den. En gruppe er en vertikal kolonne der går fra toppen af det periodiske system til bunden, og elektronegativiteten stiger fra bund til top.

I løbet af arrangementet efterlod Mendeleyev nogle få rækker tomme med indtryk af, at nogle andre elementer ville komme ind i den nærmeste fremtid. Og overraskende nok var et af de elementer, der passede ind i det hul Gallium.
Sammenligningstabel
| Parameter for sammenligning | Periode | gruppe |
|---|---|---|
| Lederskab | Perioder er de vandrette rækker i det moderne periodiske system | Grupper er de lodrette kolonner, der løber gennem toppen af det periodiske system |
| Ejendomme | Grundstofferne i en periode har ikke lignende egenskaber. | Elementerne i hver gruppe har nogle lignende egenskaber, men ikke identiske egenskaber. |
| ligheden | Grundstoffer i samme periode har lige mange elektronsammensætning | Grundstoffer i hver gruppe har lige mange valenselektroner |
| Sum | Der er 7 perioder i det periodiske system | Gruppen indeholder 18 elementer arrangeret lodret i det moderne periodiske system. |
| elektronegativitet | Det øges fra venstre mod højre. | Det stiger fra bund til top i en gruppe. |
Hvad er periode?
Et punktum er en vandret række fra yderst til venstre til yderst til højre på det periodiske system. Lige nu er der 7 perioder i det periodiske system.
En ny periode begynder, når et frisk fundamentalt energiniveau lægger sig sammen med elektronerne. Hvert grundstof i en periode vil sandsynligvis have lige mange atomare orbitaler.
For eksempel – hvert element i 1st periode har kun 1 orbital for dets elektroner, 2nd periode omfatter 2 orbitaler for elektronerne. På samme måde bliver orbitaler ved med at stige, når du bevæger dig ned i rækken.
Grundstoffets størrelse falder, når du bevæger dig hen over en periode, da antallet af elektronskaller forbliver konstant, men antallet af protoner stiger i kernen. Det er derfor, at atomet bliver tungere, men størrelsen bliver ved med at falde.
Ser du på det periodiske system, vil du se forskellige elementer monteret i hver række. 1. periode har kun 2 elementer (1 & 18), 2. og 3. periode har 8 elementer hver, 4. og 5. periode har 18 elementer, og 6. og 7. periode har henholdsvis 32 elementer hver.
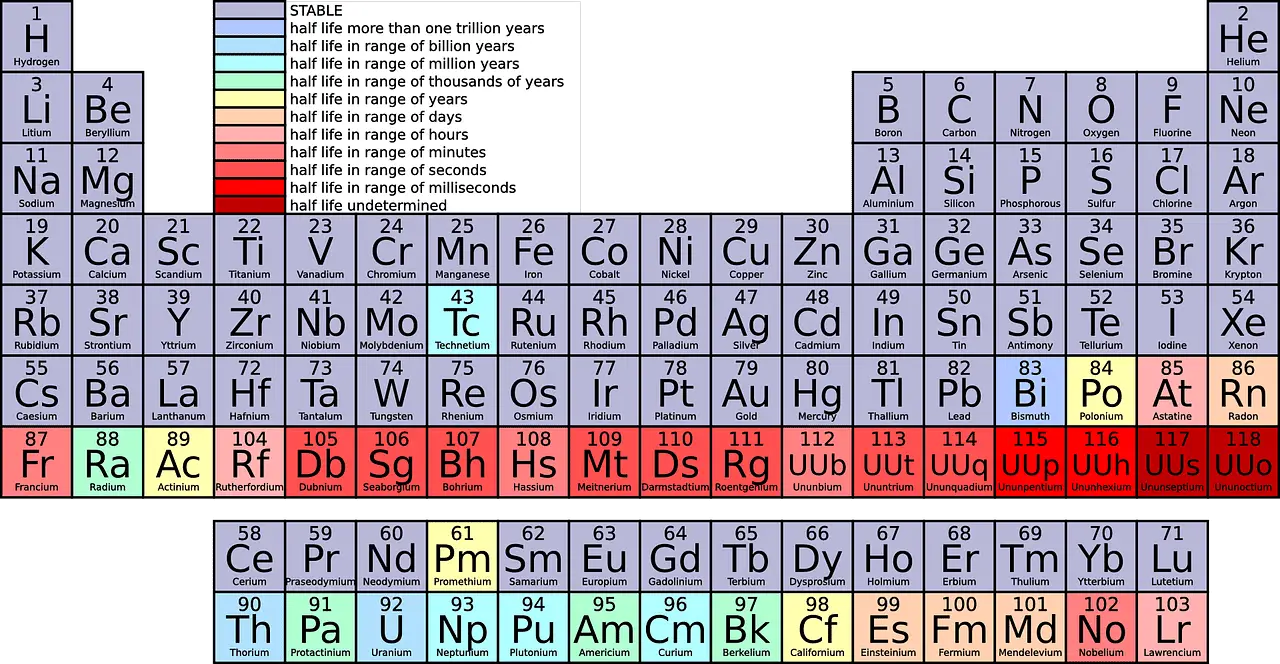
Hvad er gruppe?
Tællende fra top til bund er der 18 grupper i det periodiske system. Alle grupper tildeles særskilte navne.
Grupperne er blandede kategorier af metaller, ikke-metaller og halvmetaller, grupperet i familier efter deres lignende egenskaber. Gruppe 1 tilhører f.eks. Lithium-familien, klassificeret som alkenmetaller.
På samme måde har hver gruppe i banen sit efternavn. Grundstoffer i den beslægtede gruppe har lignende træk, fordi de har det samme elektronantal i deres yderste skal.
Størrelsen af elementet øges, når du flytter en gruppe nedad. Dette skyldes, at der findes et stort antal protoner og neutroner i kernen.
Oven i dette gør en ekstra elektronskal atomet tungere. For grupper er der to forskellige måder at illustrere elementerne på.
Det er vigtigt at forstå begge nummersystemer, fordi det periodiske system vises i begge formater. I USA brugte de bogstaverne A&B til at angive hvert element i gruppen, men desværre blev det observeret som et uorganiseret nummereringssystem.
For at eliminere al mulig forvirring, International Union of Pure and Applied Chemistry (IUPAC) Kom på ideen om at nummerere grundstofferne som (1,2, 3...18). Begge nummersystemer er dog acceptable. Men IUPACs nummerering ser velorganiseret og ligetil ud.
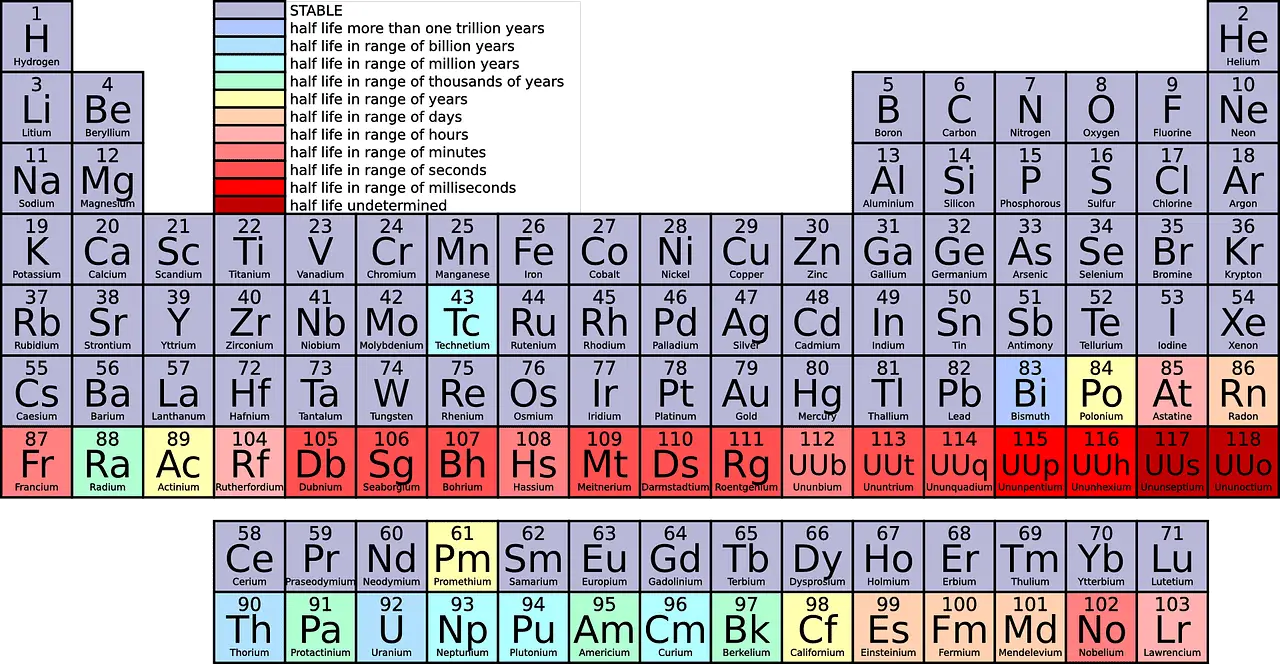
Vigtigste forskelle mellem Periode og gruppe
- Beliggenhed: Grupper er den opretstående kolonne, hvorimod perioder er de lige rækker i det periodiske system.
- Antal: Der er i alt 18 grupper og 7 perioder i det periodiske system, blandt hvilke grupperne er kategoriseret under forskellige familier og metaltyper.
- Kemiske egenskaber: Alle grundstofferne i gruppen har analoge kemiske eller fysiske egenskaber, hvorimod perioder deler det samme elektronhierarki.
- Energiniveau: Når vi går ned i gruppen fra top til bund, stiger elektronernes energiniveau. På den anden side forbliver elektronens energiniveau det samme i hver periode.
- Elektronegativitet: Dette falder fra top til bund i en gruppe og stiger fra venstre mod højre i en periode. Dette er en væsentlig overvejelse, mens du studerer det periodiske system.

Sidst opdateret: 11. juni 2023

Piyush Yadav har brugt de sidste 25 år på at arbejde som fysiker i lokalsamfundet. Han er en fysiker, der brænder for at gøre videnskaben mere tilgængelig for vores læsere. Han har en bachelorgrad i naturvidenskab og en postgraduate diplomuddannelse i miljøvidenskab. Du kan læse mere om ham på hans bio side.

Fantastisk artikel! Dette giver et godt indblik i vigtigheden af det periodiske system. Jeg nød det virkelig!
Jeg er meget glad for, at du fandt det nyttigt. Det gjorde jeg også!
Absolut, enhver naturvidenskabsstuderende bør læse dette.
Meget informativt indlæg. Vi bør presse på for bedre uddannelse og forståelse af videnskabelige emner.
Det er præcis, hvad vi har brug for.
Dette er blot endnu et eksempel på forældede uddannelsesstandarder. Vi bør undervise eleverne i mere relevante emner.
Jeg mener, at det er af afgørende betydning for eleverne at forstå det periodiske system.
Det er en kontroversiel holdning, Joel.
Jeg tror, at folk undervurderer værdien af det periodiske system. Vi burde gøre mere for at forbedre vores undervisning i det.
Absolut, dette er en vigtig pointe.
Jeg synes, det er virkelig interessant, at sådan en tilsyneladende enkel tabel kan rumme så meget værdifuld information.
Ja, det er ret fascinerende.
Dette er oplysende. Det periodiske system er undervurderet.
Dette var en tiltrængt læsning for at starte min dag!
Nogle gyldige punkter præsenteret her, men jeg er stadig ikke overbevist om vigtigheden af det periodiske system.
Jeg er enig med dig, Zach.
Det periodiske system er en hjørnesten i kemi og bør behandles som sådan.
Jeg kunne ikke være mere enig.
Jeg er uenig, jeg mener, at undervisning i det periodiske system på den nuværende måde er forældet og bør revideres.
Jeg kan se, hvorfor nogle måske finder det forældet, men det er virkelig afgørende for den videnskabelige udvikling.
Jeg kan godt se, hvad du siger, men jeg er ikke helt enig.
Selvom jeg forstår vigtigheden af det periodiske system, er det svært at argumentere for, at det nuværende uddannelsessystem er tilstrækkeligt.
Du rejser et vigtigt punkt, Erin.