La tabla periódica de química es algo que se les pide a los estudiantes que memoricen tediosa- mente sin siquiera saber el motivo real detrás de aprenderlo. Para algunas personas, es solo un tema incluido en su programa de estudios.
Pero en un sentido real, esta pequeña tabla periódica es mucho más importante que eso; es una hoja de ruta que desbloquea un millón de oportunidades para científicos e investigadores en todo el mundo. Dmitri Mendeleyev es el inventor de la tabla periódica.
Antes de él, muchos se esforzaron por organizar los elementos químicos de diferentes maneras. Pero el resultado de Dmitri fue aceptado en todo el mundo.
En las abreviaturas científicas, las filas se denominan Períodos y las columnas Grupos, respectivamente.
Puntos clave
- Los períodos son las filas horizontales en la tabla periódica, que indican el número de capas de electrones en los átomos de un elemento, con elementos en el mismo período que tienen estructuras atómicas similares.
- Los grupos son las columnas verticales en la tabla periódica, que consisten en elementos con el mismo número de electrones en su capa externa, lo que conduce a propiedades químicas similares.
- Tanto los períodos como los grupos organizan elementos en la tabla periódica, con períodos que representan filas horizontales basadas en capas de electrones y grupos que representan columnas verticales basadas en electrones de capas externas y propiedades químicas.
Período vs Grupo
Un período es una fila horizontal que va del lado izquierdo al lado derecho de la tabla periódica, y la electronegatividad aumenta a lo largo de ella. Un grupo es una vertical. visión de conjunto que va desde la parte superior de la tabla periódica hasta el fondo, y la electronegatividad aumenta de abajo hacia arriba.

Durante el tiempo de arreglo, Mendeleyev dejó algunas filas vacías con la impresión de que algunos otros elementos entrarían en un futuro cercano. Y sorprendentemente, uno de los elementos que encajaba en ese hueco era Galio.
Tabla de comparación
| Parámetro de comparación | periodo | Grupo procesos |
|---|---|---|
| Dirección | Los períodos son las filas horizontales en la tabla periódica moderna. | Los grupos son las columnas verticales que se encuentran en la parte superior de la tabla periódica. |
| Propiedades | Los elementos de un período no tienen propiedades similares. | Los elementos de cada grupo tienen algunas propiedades similares pero no propiedades idénticas. |
| Similitud | Los elementos en el mismo período tienen el mismo número de composición electrónica | Los elementos de cada grupo tienen el mismo número de electrones de valencia. |
| Suma | hay 7 periodos en la tabla periodica | El grupo contiene 18 elementos dispuestos verticalmente en la tabla periódica moderna. |
| Electronegatividad | Aumenta de izquierda a derecha. | Aumenta de abajo hacia arriba en un grupo. |
¿Qué es el período?
Un período es una fila horizontal desde el extremo izquierdo hasta el extremo derecho en la tabla periódica. A partir de ahora, hay 7 períodos en la tabla periódica.
Comienza un nuevo período cuando un nuevo nivel de energía fundamental se suma a los electrones. Cada elemento en un período probablemente tendrá el mismo número de orbitales atómicos.
Por ejemplo, cada elemento en el 1st el periodo tiene solo 1 orbital por sus electrones, 2nd período incluye 2 orbitales para los electrones. Del mismo modo, los orbitales siguen sumando a medida que avanzas en la fila.
El tamaño del elemento disminuye a medida que avanzas en un período, ya que el número de capas de electrones permanece constante, pero el número de protones aumenta en el núcleo. Esta es la razón por la cual el átomo se vuelve más pesado, pero el tamaño sigue disminuyendo.
Mirando la tabla periódica, verías diferentes elementos encajados en cada fila. El primer período tiene solo 1 elementos (2 y 1), el segundo y el tercer período tienen 18 elementos cada uno, el cuarto y el quinto período tienen 2 elementos, y el sexto y el séptimo período tienen 3 elementos cada uno, respectivamente.
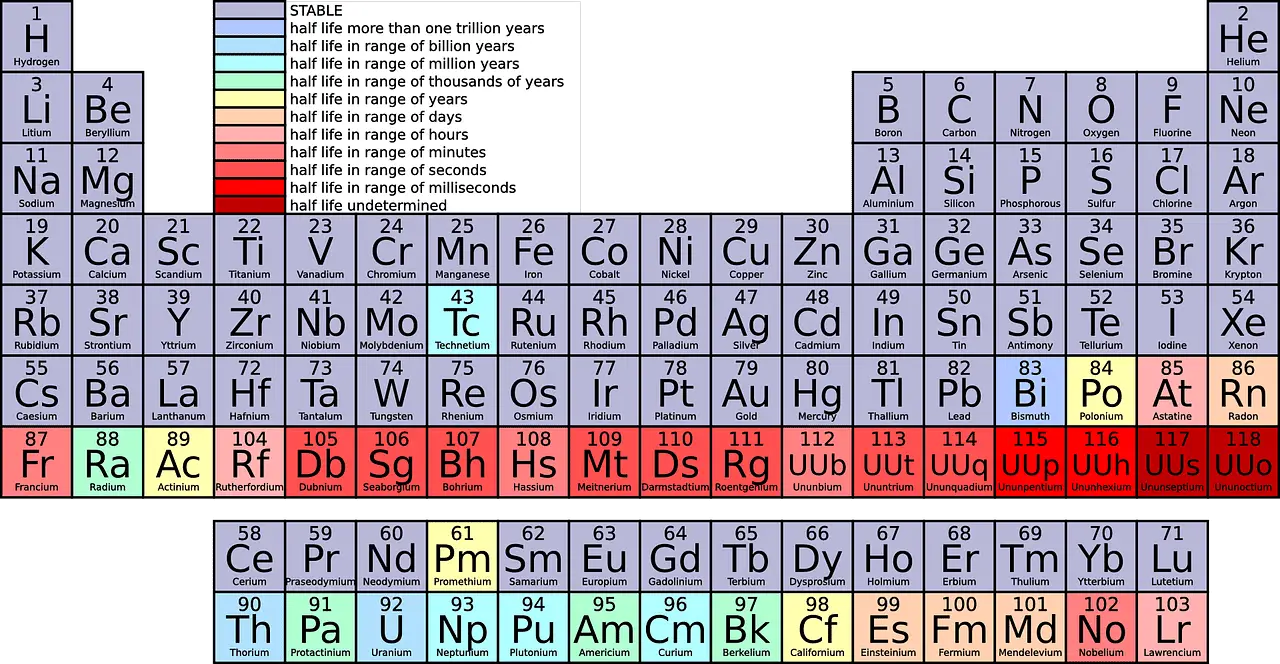
¿Qué es Grupo?
Contando de arriba abajo, hay 18 grupos en la tabla periódica. A todos los grupos se les asignan nombres distintos.
Los grupos son categorías mixtas de metales, no metales y semimetales, agrupados en familias según sus propiedades similares. Por ejemplo, el Grupo 1 pertenece a la familia de los Litios, clasificados como metales Alqueno.
De manera similar, cada grupo en el carril tiene su apellido. Los elementos del grupo relacionado tienen características similares porque tienen el mismo número de electrones en sus capas más externas.
El tamaño del elemento aumenta a medida que mueve cualquier grupo hacia abajo. Esto se debe a que en el núcleo existe una gran cantidad de protones y neutrones.
Además de esto, una capa de electrones extra hace que el átomo sea más pesado. Para los grupos, hay dos maneras diferentes de ilustrar los elementos.
Comprender ambos sistemas de numeración es esencial porque la tabla periódica aparece en ambos formatos. En los Estados Unidos, usaron las letras A&B para indicar cada elemento del grupo, pero desafortunadamente, se observó como un sistema de numeración desorganizado.
Para eliminar toda posible confusión, la International Unión de Química Pura y Aplicada (IUPAC) se le ocurrió la idea de numerar los elementos como (1,2, 3… 18). Sin embargo, ambos sistemas de numeración son aceptables. Pero la numeración de la IUPAC parece bien organizada y sencilla.
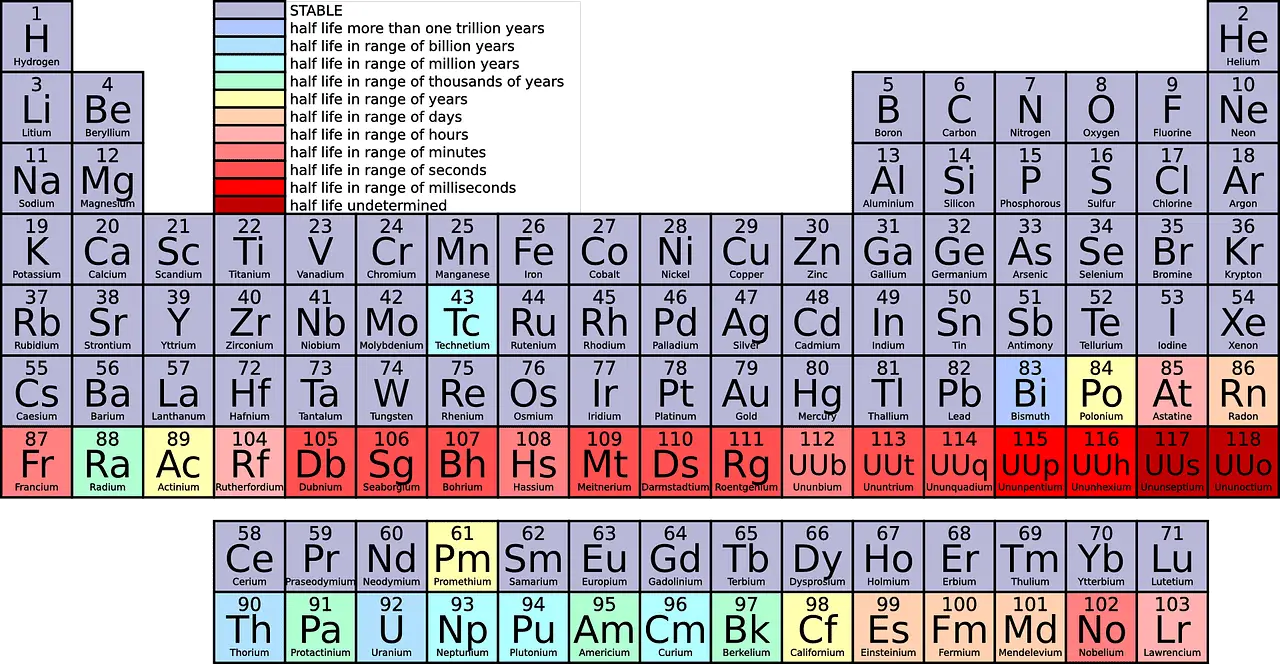
Principales diferencias entre Período y Grupo
- Ubicación: Los grupos son la columna vertical, mientras que los períodos son las filas rectas de la tabla periódica.
- Número: Hay un total de 18 grupos y 7 períodos en la tabla periódica, entre los cuales los grupos se clasifican en diferentes familias y tipos de metales.
- Propiedades químicas: Todos los elementos del grupo tienen propiedades químicas o físicas análogas, mientras que los períodos comparten la misma jerarquía electrónica.
- Nivel de energía: A medida que descendemos por el grupo de arriba a abajo, el nivel de energía de los electrones aumenta. Por otro lado, en cada período, el nivel de energía del electrón permanece igual.
- Electronegatividad: Esta declina de arriba a abajo en un grupo y sube de izquierda a derecha en un período. Esta es una consideración esencial al estudiar la tabla periódica.

Última actualización: 11 de junio de 2023

Piyush Yadav ha pasado los últimos 25 años trabajando como físico en la comunidad local. Es un físico apasionado por hacer que la ciencia sea más accesible para nuestros lectores. Tiene una licenciatura en Ciencias Naturales y un Diploma de Postgrado en Ciencias Ambientales. Puedes leer más sobre él en su página de biografía.

¡Buen artículo! Esto da una gran idea de la importancia de la tabla periódica. ¡Realmente lo disfrute!
Me alegra mucho que te haya resultado útil. ¡Yo también lo hice!
Absolutamente, todo estudiante de ciencias debería leer esto.
Publicación muy informativa. Deberíamos impulsar una mejor educación y comprensión de los temas científicos.
Esto es exactamente lo que necesitamos.
Este es sólo otro ejemplo de estándares educativos obsoletos. Deberíamos enseñar temas más relevantes a los estudiantes.
Creo que es de vital importancia que los estudiantes comprendan la tabla periódica.
Esa es una toma controvertida, Joel.
Creo que la gente subestima el valor de la tabla periódica. Deberíamos hacer más para mejorar nuestra enseñanza al respecto.
Absolutamente, este es un punto importante.
Creo que es realmente interesante que una tabla aparentemente tan simple pueda contener tanta información valiosa.
Sí, es bastante fascinante.
Esto es esclarecedor. La tabla periódica está subestimada.
¡Esta fue una lectura muy necesaria para comenzar mi día!
Aquí se presentan algunos puntos válidos, pero todavía no estoy convencido de la importancia de la tabla periódica.
Estoy de acuerdo contigo, Zach.
La tabla periódica es una piedra angular de la química y debe tratarse como tal.
No podría estar mas de acuerdo.
No estoy de acuerdo, creo que enseñar la tabla periódica de la forma actual está anticuado y debería revisarse.
Puedo entender por qué algunos podrían considerarlo obsoleto, pero realmente es vital para el desarrollo científico.
Puedo ver lo que estás diciendo pero no estoy completamente de acuerdo.
Si bien entiendo la importancia de la tabla periódica, es difícil argumentar que el sistema educativo actual es adecuado.
Planteas un punto importante, Erin.