Periodni sustav kemije nešto je što učenici moraju zamorno pamtiti, a da uopće ne znaju koji je stvarni motiv koji stoji iza njegovog učenja. Za neke ljude to je samo tema uključena u njihov nastavni program.
Ali u pravom smislu, ovaj mali periodni sustav mnogo je važniji od toga; to je putokaz koji otključava milijun mogućnosti znanstvenicima i istraživačima diljem svijeta. Dmitrij Mendeljejev je izumitelj periodnog sustava elemenata.
Prije njega mnogi su se trudili rasporediti kemijske elemente na različite načine. Ali Dmitrijev ishod bio je prihvaćen u cijelom svijetu.
U znanstvenim kraticama, redovi se nazivaju Razdobljima, a stupci Grupama.
Ključni za poneti
- Razdoblja su horizontalni redovi u periodnom sustavu, koji označavaju broj elektronskih ljuski u atomima elementa, pri čemu elementi u istoj periodi imaju slične atomske strukture.
- Grupe su okomiti stupci u periodnom sustavu elemenata koji se sastoje od elemenata s istim brojem elektrona u vanjskoj ljusci, što dovodi do sličnih kemijskih svojstava.
- I periode i grupe organiziraju elemente u periodnom sustavu, s periodima koji predstavljaju vodoravne retke na temelju elektronskih ljuski, a grupe koje predstavljaju okomite stupce na temelju elektrona vanjske ljuske i kemijskih svojstava.
Razdoblje vs Grupa
Perioda je vodoravni red koji ide od lijeve prema desnoj strani periodnog sustava, a elektronegativnost se povećava preko njega. Grupa je vertikala kolona koja ide od vrha periodnog sustava prema dnu, a elektronegativnost raste odozdo prema gore.

Tijekom aranžiranja Mendeljejev je nekoliko redova ostavio praznim s dojmom da će u skoroj budućnosti ući neki drugi elementi. I začudo, jedan od elemenata koji se uklopio u tu prazninu bio je galijum.
Tabela za usporedbu
| Parametar usporedbe | Razdoblje | Klan |
|---|---|---|
| Smjer | Razdoblja su vodoravni redovi u modernom periodnom sustavu | Grupe su okomiti stupci koji prolaze kroz vrh periodnog sustava |
| Nekretnine | Elementi u razdoblju nemaju slična svojstva. | Elementi u svakoj skupini imaju neka slična svojstva, ali ne i identična svojstva. |
| Sličnost | Elementi u istoj periodi imaju jednak broj elektronskih sastava | Elementi u svakoj skupini imaju jednak broj valentnih elektrona |
| Suma | U periodnom sustavu postoji 7 perioda | Grupa sadrži 18 elemenata poredanih okomito u modernom periodnom sustavu. |
| Elektronegativnost | Povećava se s lijeva na desno. | Povećava se odozdo prema gore u skupini. |
Što je mjesečnica?
Perioda je vodoravni red od krajnje lijeve do krajnje desne strane periodnog sustava. Od sada postoji 7 razdoblja na periodnom sustavu.
Novo razdoblje počinje kada se nova osnovna energija zbroji s elektronima. Svaki element u razdoblju vjerojatno će imati jednak broj atomskih orbitala.
Na primjer – svaki element u 1st razdoblje ima samo 1 orbitalni za njegove elektrone, 2nd period uključuje 2 orbitale za elektrone. Slično tome, orbitale se nastavljaju zbrajati kako se pomičete prema dolje u redu.
Veličina elementa se smanjuje kako se krećete kroz razdoblje jer broj elektronskih ljuski ostaje konstantan, ali broj protona raste u jezgri. Zbog toga atom postaje teži, ali se veličina stalno smanjuje.
Gledajući periodni sustav, vidjeli biste različite elemente uklopljene u svaki red. 1. period ima samo 2 elementa (1 & 18), 2. i 3. period imaju po 8 elemenata, 4. i 5. period imaju 18 elemenata, a 6. i 7. period imaju po 32 elementa.
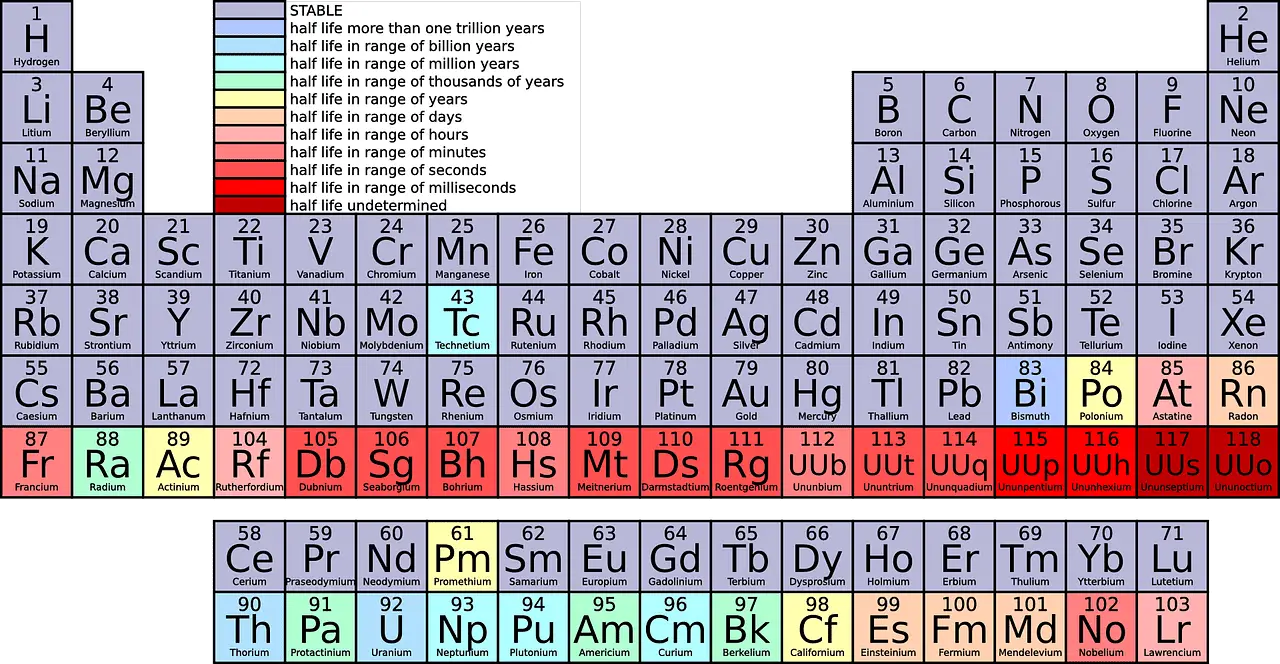
Što je grupa?
Brojeći od vrha prema dolje, u periodnom sustavu postoji 18 grupa. Svim grupama dodijeljena su različita imena.
Grupe su mješovite kategorije metala, nemetala i polumetala, grupiranih u obitelji prema sličnim svojstvima. Npr., grupa 1 pripada obitelji litija, klasificiranih kao alkenski metali.
Slično tome, svaka grupa u stazi ima svoje prezime. Elementi u srodnoj skupini imaju slične osobine jer imaju isti broj elektrona u svojim najudaljenijim ljuskama.
Veličina elementa se povećava kako pomičete bilo koju grupu prema dolje. To je zato što u jezgri postoji veliki broj protona i neutrona.
Povrh toga, dodatna elektronska ljuska čini atom težim. Za grupe postoje dva različita načina za ilustriranje elemenata.
Razumijevanje oba sustava numeriranja bitno je jer se periodni sustav pojavljuje u oba formata. U Sjedinjenim Američkim Državama koristili su slova A&B za označavanje svakog elementa u grupi, ali nažalost, to je promatrano kao neorganiziran sustav numeriranja.
Da otkloni svaku moguću zabunu, Internacional Unija čiste i primijenjene kemije (IUPAC) Došao je na ideju numeriranja elemenata kao (1,2, 3… 18). Međutim, prihvatljiva su oba sustava numeriranja. Ali IUPAC-ovo numeriranje izgleda dobro organizirano i jednostavno.
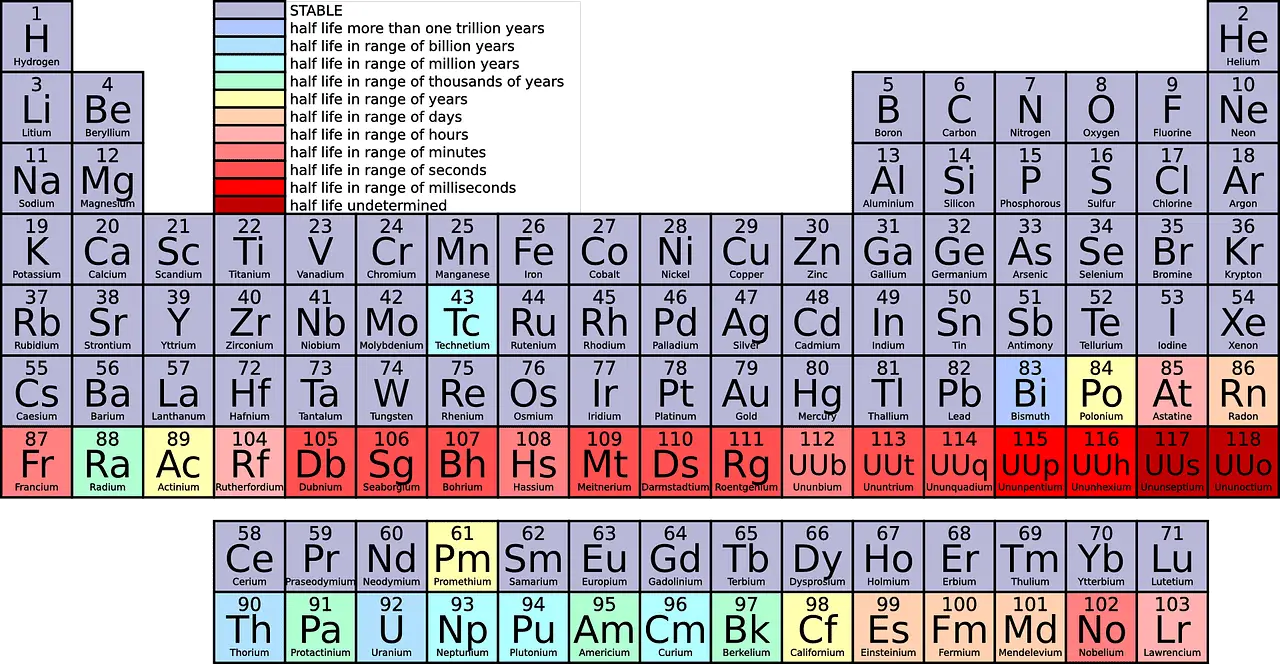
Glavne razlike između Razdoblje i grupa
- Mjesto: Grupe su uspravni stupci, dok su periode ravni redovi u periodnom sustavu.
- Broj: Postoji ukupno 18 grupa i 7 perioda u periodnom sustavu, među kojima su grupe kategorizirane prema različitim obiteljima i vrstama metala.
- Kemijska svojstva: Svi elementi u skupini imaju analogna kemijska ili fizikalna svojstva, dok periode dijele istu elektronsku hijerarhiju.
- Razina energije: Kako idemo niz grupu od vrha prema dolje, razina energije elektrona raste. S druge strane, u svakoj periodi razina energije elektrona ostaje ista.
- Elektronegativnost: To opada odozgo prema dolje u skupini i raste slijeva nadesno u razdoblju. Ovo je ključno razmatranje pri proučavanju periodnog sustava elemenata.

Zadnje ažuriranje: 11. lipnja 2023

Piyush Yadav proveo je posljednjih 25 godina radeći kao fizičar u lokalnoj zajednici. On je fizičar koji strastveno želi učiniti znanost dostupnijom našim čitateljima. Posjeduje diplomu prirodnih znanosti i poslijediplomski studij znanosti o okolišu. Više o njemu možete pročitati na njegovom bio stranica.

Sjajan članak! To daje veliki uvid u važnost periodnog sustava elemenata. Stvarno sam uživao!
Jako mi je drago da ti je pomoglo. I ja sam!
Apsolutno, svaki student znanosti trebao bi ovo pročitati.
Vrlo informativan post. Trebali bismo se zalagati za bolje obrazovanje i razumijevanje znanstvenih tema.
To je upravo ono što nam treba.
Ovo je samo još jedan primjer zastarjelih obrazovnih standarda. Trebali bismo studentima predavati relevantnije teme.
Vjerujem da je od vitalne važnosti da učenici razumiju periodni sustav.
To je kontroverzan stav, Joel.
Mislim da ljudi podcjenjuju vrijednost periodnog sustava elemenata. Trebali bismo učiniti više kako bismo poboljšali naše podučavanje o tome.
Apsolutno, ovo je važna točka.
Mislim da je jako zanimljivo da tako naizgled jednostavna tablica može sadržavati toliko vrijednih informacija.
Da, prilično je fascinantno.
Ovo je prosvjetljujuće. Periodni sustav je podcijenjen.
Ovo je bilo prijeko potrebno štivo za početak dana!
Ovdje su iznesene neke valjane točke, ali još uvijek nisam uvjeren u važnost periodnog sustava elemenata.
Slažem se s tobom, Zach.
Periodni sustav je kamen temeljac kemije i tako ga treba tretirati.
Ne bih se mogao više složiti.
Ne slažem se, smatram da je poučavanje periodnog sustava na sadašnji način zastarjelo i treba ga revidirati.
Shvaćam zašto bi ga neki mogli smatrati zastarjelim, ali doista je ključan za znanstveni razvoj.
Shvaćam što govoriš, ali se ne slažem u potpunosti.
Iako razumijem važnost periodnog sustava, teško je tvrditi da je trenutni obrazovni sustav prikladan.
Pokrenula si važnu stvar, Erin.