As pessoas confundem Etanol e Ácido Etanóico por causa da semelhança em seus nomes. Exceto por isso, o único elo comum entre ambos é o seu estado físico. Ambos estão na forma líquida e são incolores. Além desses dois fatores, ambos os ácidos apresentam muitas diferenças.
O etanol é simplesmente o álcool que é um líquido inflamável e volátil e também uma fonte alternativa de combustível. É uma substância psicoativa como droga recreativa e ingrediente ativo em bebidas alcoólicas.
Ao contrário, o ácido etanóico é o ácido carboxílico que sucede ao ácido fórmico. Globalmente, sua demanda é de até 6.5 milhões de toneladas por ano.
Sua densidade, cheiro, sabor, pontos de ebulição e fusão, tudo difere um do outro. A fórmula molecular do etanol é C2H5OH, e o ácido etanóico é CH3COOH.
Principais lições
- O etanol é um álcool com a fórmula química C2H5OH, enquanto o ácido etanóico é um ácido carboxílico com CH3COOH.
- O etanol é um líquido incolor com um leve odor comumente usado como combustível e solvente. Ao mesmo tempo, o ácido etanóico é um líquido incolor com forte odor comumente utilizado na produção de vinagre.
- O etanol tem um ponto de ebulição mais baixo que o ácido etanóico, tornando-o mais fácil de evaporar e menos ácido que o ácido etanóico.
Etanol x Ácido Etanóico
O etanol, também conhecido como álcool etílico, é um líquido incolor e inflamável comumente usado como solvente, combustível e em bebidas alcoólicas. Sua fórmula química é C2H5OH. O ácido etanóico, também conhecido como ácido acético, é um líquido límpido e incolor que possui um odor forte e pungente. Sua fórmula química é CH3COOH.

Tabela de comparação
| Parâmetros de comparação | Etanol | Ácido Etanóico |
|---|---|---|
| Nome IUPAC | O nome da União Internacional de Química Pura e Aplicada (IUPAC) do Etanol é o mesmo que é chamado. | O nome da União Internacional de Química Pura e Aplicada (IUPAC) de um ácido etanóico é um ácido acético. |
| Fórmulas Moleculares | Sua fórmula molecular é C2H5OH | Sua fórmula molecular é CH3COOH. |
| Densidade | 0.789 g / cm3 | 1.05 g / cm3 |
| Odour | Tem um cheiro agradável de perfume. | Tem um odor pungente ou com cheiro de vinagre. |
| Gosto | É ardente e amargo. | É azedo. |
| Pontos de Ebulição | Tem um ponto de ebulição de 78.37 ℃ ou 173.1 ℉. | Tem um ponto de ebulição de 117.9 ℃ ou 244.2 ℉. |
| Pontos de fusão | Tem um ponto de fusão de -114.1 ℃ ou -173.5 ℉. | Tem um ponto de fusão de 16.6 ℃ ou 61.9 ℉. |
| Grupo funcional | Possui álcool (-OH) como grupo funcional. | Possui ácido carboxílico (-OOH) como grupo funcional. |
| Existência de outros Grupos | Grupos etil e hidroxila existem no etanol. | Grupos metil e carboxila existem no etanol. |
| O teste do papel de tornassol | Ele exibe um 7.33 pEscala H em uma concentração. | Apresenta 2 a 4 pEscala H em uma concentração. |
| NaHCO3 Test | Não reage com bicarbonato de sódio. | Reage com bicarbonato de sódio e libera CO2 gás. |
| Teste de Páscoa | Forma Éster somente após reagir com a presença do ácido etanóico. | Forma Éster após reagir com a presença do ácido sulfúrico. |
| Massa molar | X | X |
| usado Para | Pode ser usado como agente esterilizante ou para fazer bebidas alcoólicas. | Pode ser usado como limpador de banheiro ou para fazer vinagre. |
O que é etanol?
O nome da União Internacional de Química Pura e Aplicada (IUPAC) do Etanol é o mesmo que é chamado.
Sua fórmula molecular é 'C2H5OH' e sua densidade é 0.789 g/cm3. Tem um sabor amargo e ardente e um sabor agradável perfume-como odor. Pode ser usado como agente esterilizante ou para fazer bebidas alcoólicas.
A massa molar deste ácido é 46.07 g/mol. O ponto de fusão do etanol é -114.1 ℃ ou -173.5 ℉. E seu ponto de ebulição é 78.37 ℃ ou 173.1 ℉. Durante a fermentação, o etanol se forma usando leveduras como Saccharomyces cerevisiae ou Schizo-saccharomyces.
O teste do papel tornassol exibe uma escala de 7.33 pH (potencial de hidrogênio). Não reage com bicarbonato de sódio. Forma Éster somente após reação com a presença do ácido etanóico. Possui álcool (-OH) como grupo funcional. Além disso, existem grupos etil e hidroxila.

O que é Ácido Etanóico?
O nome da União Internacional de Química Pura e Aplicada (IUPAC) de um ácido etanóico é um ácido acético. Tem sabor azedo e odor pungente ou com cheiro de vinagre. Sua fórmula molecular é 'CH3COOH' e sua densidade é de 1.05 g/cm3. Pode ser usado como limpador de banheiro ou para fazer vinagre.
Ele exibe uma escala de 2-4 pH (potencial de hidrogênio) no teste de papel tornassol. Reage com bicarbonato de sódio e libera CO2 gás. Também forma éster após reação com a presença de ácido sulfúrico.
Possui ácido carboxílico (-OOH) como grupo funcional. Além disso, existem grupos Metil e Carboxil.
A massa molar desse ácido é 60.052 g/mol. Durante a fermentação, as bactérias Acetobacter formam ácido etanóico. Quando o ácido etanóico passa através do líquido de cal, torna-se opaco e torna-se CO2 gás. Seu ponto de ebulição é 17.9 ℃ ou 244.2 ℉. E o ponto de fusão é 16.6 ℃ ou 61.9 ℉.
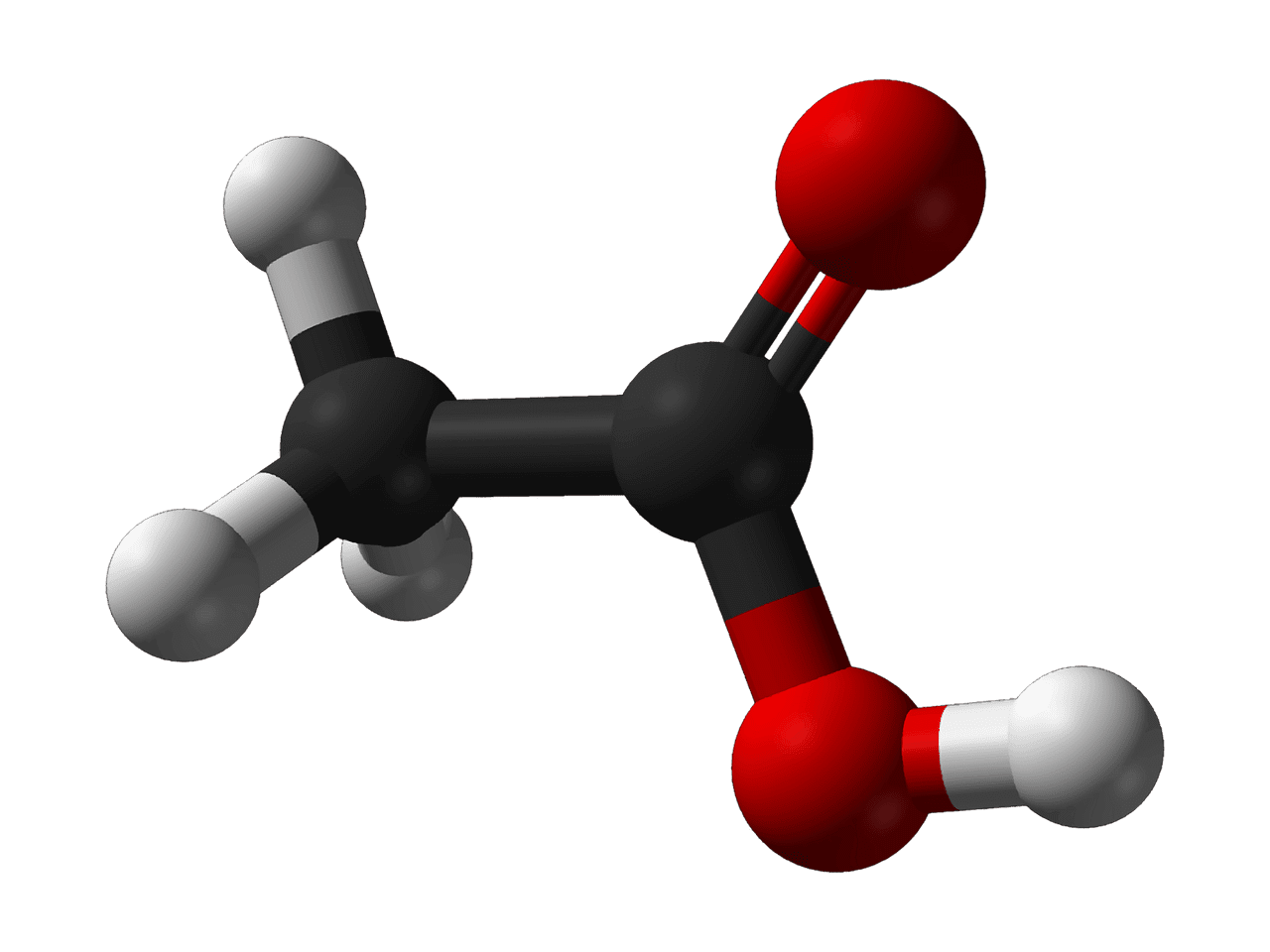
Principais diferenças entre etanol e ácido etanóico
- A fórmula molecular do etanol é C2H5OH, enquanto o ácido etanóico é CH3COOH.
- 0.789 g/cm3 é a densidade do etanol, enquanto 1.05 g/cm3 é o ácido etanóico.
- O primeiro tem um cheiro agradável de perfume. Pelo contrário, o segundo tem um odor pungente ou com cheiro de vinagre.
- O etílico tem um gosto pouco ardente e amargo. O ácido acético tem gosto azedo.
- O ponto de ebulição do etanol é 78.37 ℃ ou 173.1 ℉. Por outro lado, o ácido etanóico é de 117.9 ℃ ou 244.2 ℉.
- O ponto de fusão do primeiro é -114.1 ℃ ou -173.5 ℉. Por outro lado, o segundo é de 16.6 ℃ ou 61.9 ℉.
- O anterior tem o álcool (-OH) como grupo funcional. Ao contrário, o seguinte tem um ácido carboxílico (-OOH).
- O etanol exibe uma escala de pH de 7.33 no teste do papel tornassol, enquanto o ácido etanóico exibe uma escala de pH de 2 a 4.
- O primeiro não reage com o bicarbonato de sódio. Por outro lado, o último reage e libera CO2 gás.
- A massa molar do etanol é 46.07 g/mol, enquanto a massa molar do ácido etanóico é 60.052 g/mol.
- https://pubs.acs.org/doi/abs/10.1021/je300810p
- https://www.sciencedirect.com/science/article/pii/S0378775301010679
- https://www.sciencedirect.com/science/article/pii/S0022328X04004668
Este artigo foi escrito por: Supriya Kandekar
Última atualização: 11 de junho de 2023

Piyush Yadav passou os últimos 25 anos trabalhando como físico na comunidade local. Ele é um físico apaixonado por tornar a ciência mais acessível aos nossos leitores. Ele é bacharel em Ciências Naturais e pós-graduado em Ciências Ambientais. Você pode ler mais sobre ele em seu página bio.

Este post é uma lufada de ar fresco, oferecendo conhecimentos perspicazes sobre etanol e ácido etanóico.
Com certeza, é informativo e esclarecedor.
Esta informação é crucial para os entusiastas da química que desejam aprofundar seus conhecimentos.
Como alguém que adora química, aprecio a profundidade desta explicação.
Como alguém com grande interesse em química, considero este artigo uma fonte excepcional de informações.
Na verdade, é uma explicação bem articulada e completa do assunto.
Que bom que esse post existe, muita gente não conhece o contraste entre o Etanol e o Ácido Etanóico.
Com certeza, os detalhes científicos ajudam os leitores a entender.
Este artigo é um excelente recurso para estudantes e profissionais da área de química.
A análise aprofundada diferencia este artigo dos outros.
Certamente, oferece conhecimentos valiosos que contribuem para uma compreensão mais profunda do tema.
A postagem diferencia efetivamente entre etanol e ácido etanóico usando evidências científicas.
Concordo, é raro encontrar conteúdo tão bem pesquisado.
O conteúdo informativo é uma prova da experiência do autor no assunto.
Agradeço a natureza detalhada e objetiva deste post.
A comparação cientificamente precisa fornece informações valiosas.
Considero a tabela de comparação detalhada e as principais conclusões muito úteis e esclarecedoras.
A clareza das informações aqui apresentadas é louvável.
Concordo, este post dá uma visão holística das diferenças entre o etanol e o ácido etanóico.
Este é um artigo muito informativo que esclarece qualquer dúvida sobre a diferença entre Etanol e Ácido Etanóico.
Finalmente, entendo a distinção entre os dois graças a este artigo.
Eu concordo, isso é explicado claramente de forma científica.
A explicação detalhada fornecida aqui é altamente benéfica e enriquecedora.
Com certeza, aumenta a compreensão do leitor sobre o assunto.