Terminologie jako prvky a atomy se často používají při studiu chemie a někdy i fyziky. Jak se však předmět vyvíjí a stává se stále složitějším, význam pojmů se může snadno zaměnit.
Key Takeaways
- Prvky nelze chemickou cestou rozložit na jednodušší látky. Atomy jsou zároveň nejmenší částicí prvku, která si zachovává chemické vlastnosti tohoto prvku.
- Prvky mají jedinečná atomová čísla, která definují jejich vlastnosti a umístění v periodické tabulce, zatímco atomy mají protony, elektrony a neutrony, které určují jejich chování a interakce.
- Prvky se mohou spojovat za vzniku sloučenin, ale atomy téhož prvku nelze dále rozkládat, aniž by se změnily chemické vlastnosti látky.
Prvky vs. atomy
Prvky a atomy se liší, protože složka je nejjednodušší formou látky tvořené atomy. Aspekt je klasifikován v závislosti na jeho atomovém čísle. Subatomární částice se spojují a vytvářejí atomy, které se spojují a vytvářejí prvek. Později se prvky spojují a vytvářejí molekuly.

Na rozdíl od chemických sloučenin nelze chemické prvky rozdělit na jednodušší látky žádnou chemickou metodou. V periodické tabulce prvků jsou prvky systematizovány podle jejich atomového čísla.
Atom je nejmenší část konvenční hmoty, která vytváří chemický prvek. Atom se skládá ze subatomárních částic. Jednoduše řečeno, atomy jsou stavebními kameny pro skládání prvků.
Srovnávací tabulka
| Parametry srovnání | Prvky | Atomy |
|---|---|---|
| Velikost | Větší než atomy | Velmi malý (není vidět ani pod mikroskopem) |
| Počet typů | Existuje celkem 118 prvků. | V přírodě existuje přibližně 92 druhů atomů. |
| Složení | Konkrétní prvek se skládá pouze z jednoho konkrétního typu atomu. | Atomy se skládají ze subatomárních částic. Jsou to protony, elektrony a neutrony. |
| Když se spojí | Prvky se spojují a vytvářejí nové chemické reakce. | Když se atomy spojí, vytvoří molekulu. |
| Hmotnost | Těžší než konkrétní atom. | Extrémně lehký (relativní hmotnost je 1 AMU) |
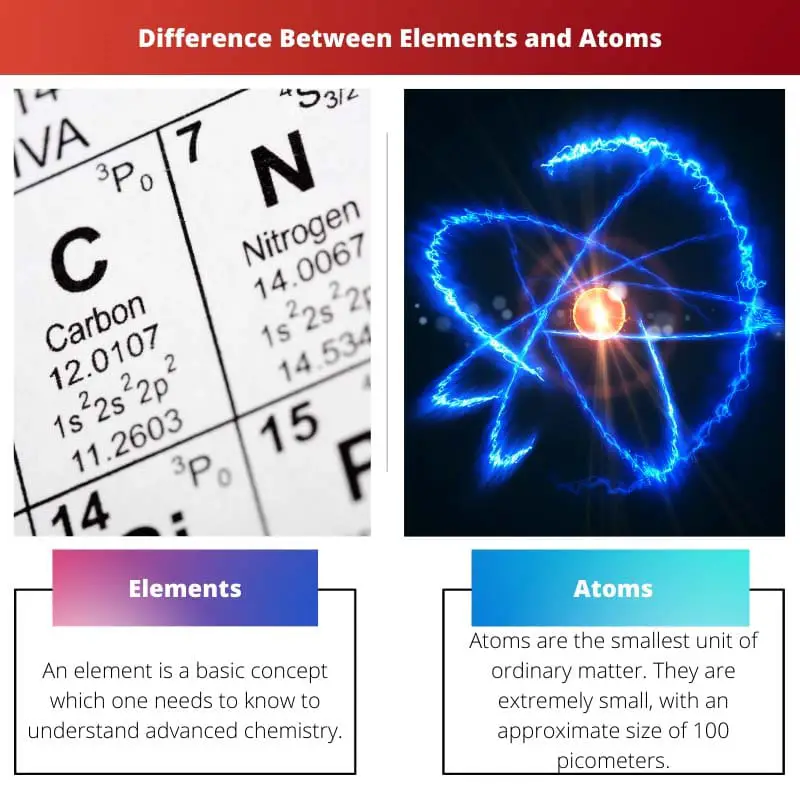
Co jsou Prvky?
Element je základní koncept, který člověk musí znát, aby porozuměl pokročilé chemii. Ve svých atomových jádrech je prvek složen pouze z atomů, které obsahují stejný počet protonů.
Chemické prvky nelze žádnou chemickou metodou rozdělit na jednodušší prvky nebo látky. Ten je připisován atomovému číslu, reprezentovanému symbol "Z.'
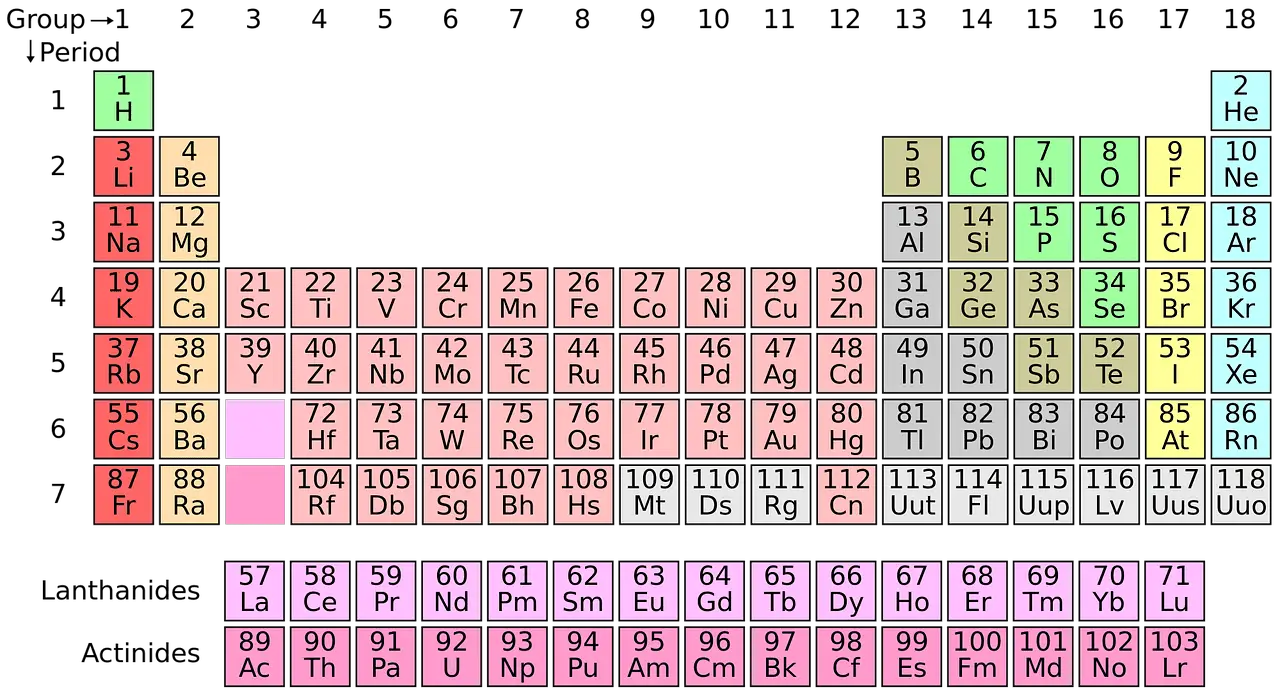
Moderní chemie hodně závisí na dobové tabulce. Všechny objevené prvky jsou kategorizovány a systematicky uspořádány v periodické tabulce. Tento koncept vymyslel ruský chemik Dmitrij Mendělejev v roce 1869.
Charakteristiky prvku jsou zodpovědné za jeho fyzikální stav při pokojové nebo průměrné teplotě. Může být buď v plynném stavu nebo v pevném nebo kapalném stavu.
Celkem existuje přibližně 118 typů prvků.
Několik příkladů prvků je následujících:
- Vodík
- Uhlík
- Neon
- Magnézium
- hliník
- Bor
Co jsou atomy?
Atomy jsou nejmenší jednotkou běžné hmoty. Jsou malinké, s přibližnou velikostí 100 pikometrů. Atom je také extrémně lehký. Relativně váha druhého jmenovaného je relativně 1AMU.
Jádro se skládá z jednoho nebo více protonů a několika neutronů. Existuje pouze jedna výjimka z tohoto pravidla: vodík, který nemá žádné neutrony. Jádro tvoří 99.94 % hmotnosti atomu.
Protony mají kladný elektrický náboj, elektrony obsahují záporné elektrické množství a neutrony nemají žádnou elektrickou kontrolu. Atom je elektricky neutrální, když je počet protonů a elektronů stejný.
V přírodě existuje 92 různých typů atomů.
Primární koncept a představa že hmota obsahuje drobné nedělitelné částice jsou prastaré. Historie atomů sahá až do starověku Indie a Řecka.

Hlavní rozdíly mezi prvky a atomy
- Když se spojí více než jeden prvek, vytvoří novou chemickou reakci, jejímž výsledkem je nový prvek. Když se spojí více než jeden atom (udržení různých látek konstantní), vytvoří molekulu.
- Hmotnost prvku je těžší ve srovnání s hmotností atomu, zatímco v případě atomů je atom extrémně lehký. Relativní hmotnost druhého jmenovaného je přibližně 1 AMU.
- https://books.google.com/books?hl=en&lr=&id=EvTI-ouH3SsC&oi=fnd&pg=PP1&dq=elements&ots=pQ5TOAfsJ3&sig=LBL5oWU1-cH9p_y8JPtdmdjok7g
- https://pubs.acs.org/doi/pdf/10.1021/ar00109a003
Poslední aktualizace: 11. června 2023

Piyush Yadav strávil posledních 25 let prací jako fyzik v místní komunitě. Je to fyzik, který je zapálený pro zpřístupnění vědy našim čtenářům. Je držitelem titulu BSc v přírodních vědách a postgraduálního diplomu v oboru environmentální vědy. Více si o něm můžete přečíst na jeho bio stránka.

Hluboké vysvětlení usnadnilo pochopení rozdílů mezi prvky a atomy a přidalo nesmírnou vzdělávací hodnotu.
Detailní porovnávání prvků a atomů se ukázalo jako vzdělávací přínos.
Jasné a podrobné srovnání prvků a atomů usnadnilo pochopení jejich rozdílů a slouží jako skvělý učební nástroj.
Učení se o rozdílech mezi prvky a atomy z tohoto článku bylo docela poučné a poučné.
Díky informativnímu obsahu o prvcích a atomech je srovnání těchto dvou pojmů zcela jasné a srozumitelné.
Tento článek poskytl komplexní a informativní podrobné srovnání mezi prvky a atomy a poskytl neocenitelný vhled do jejich příslušných charakteristik a chování.
Jsem ohromen jasným srovnáním rozdílů mezi prvky a atomy, které bylo uvedeno v tomto článku.
Článek má velkou vzdělávací hodnotu, zejména pro ty, kteří se živě zajímají o vědu a chemii.
To je rozhodně cenný zdroj pro každého, kdo se zajímá o poznání prvků a atomů.
Ukázalo se, že má hodnotu pro pochopení základního vědeckého konceptu prvků a atomů.
Komplexní srovnání prvků a atomů je poučné a nabízí lepší pochopení těchto vědeckých pojmů.
Hluboký ponor do porovnávání prvků a atomů poskytl cennou vzdělávací zkušenost, která usnadňuje pochopení těchto vědeckých pojmů.
Tento článek uspěl v poskytnutí zasvěceného a komplexního srovnání mezi prvky a atomy, což je velmi přínosné pro vzdělávací účely a pochopení vědeckých konceptů.
Vzdělávací hodnota tohoto článku srovnání prvků a atomů je skutečně chvályhodná.
Komplexní podrobnosti o klíčových aspektech prvků vs atomů jsou velmi užitečné pro lepší pochopení těchto pojmů.