Le mot ion fait référence à un atome chargé négativement ou positivement, tandis que les isotopes d'un élément sont différentes variations de ses atomes. Bien qu'ils soient liés aux atomes de l'élément, les ions et les isotopes diffèrent largement de nombreuses manières.
Faits marquants
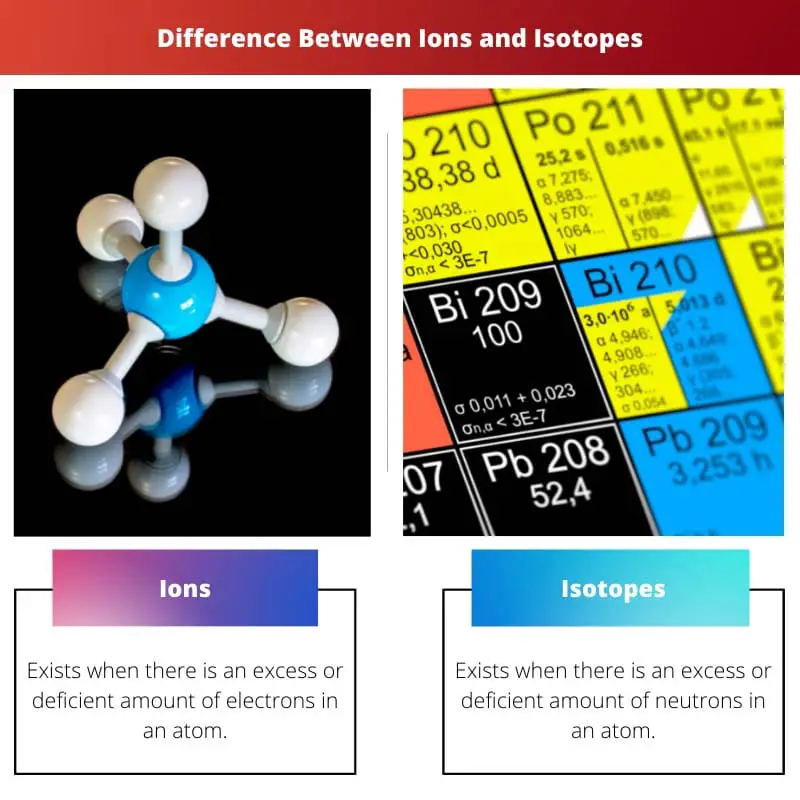
- Les ions se forment lorsque les atomes gagnent ou perdent des électrons, ce qui donne une particule chargée, tandis que les isotopes ont le même nombre de protons mais des neutrons différents.
- Les ions présentent des propriétés chimiques différentes en raison de leur charge, tandis que les isotopes ont des propriétés chimiques similaires mais des propriétés physiques différentes.
- Les isotopes peuvent être radioactifs, émettant des radiations lors de leur désintégration, tandis que les ions ne présentent pas de radioactivité.
Ions vs isotopes
Les ions sont des atomes qui ont plus ou moins d'électrons que les protons parce qu'ils ont gagné ou perdu des électrons. Un ion peut avoir une charge positive ou négative. Les isotopes sont des atomes qui sont du même élément avec le même nombre de protons mais un nombre différent de neutrons dans leurs noyaux.

Le mot ion fait référence à des atomes chargés négativement ou positivement. Ils existent lorsque les électrons sont insuffisants ou excessifs dans un atome. L'excédent ou le déficit montant détermine la charge positive ou négative des atomes.
Le nombre de protons dans tous les atomes d'un élément particulier est le même, mais le nombre de neutrons peut différer. Pour cette raison, un élément a plusieurs isotopes qui ont des propriétés chimiques et des comportements similaires.
Tableau de comparaison
| Paramètres de comparaison | ions | Les isotopes |
|---|---|---|
| Existence | Il existe lorsqu'un atome a une quantité excessive ou insuffisante d'électrons. | Il existe lorsqu'un atome a une quantité excessive ou insuffisante de neutrons. |
| Nomenclature | Dérivé du mot grec « iov » qui signifie « aller ». | Dérivé des mots grecs "isos" et "topos", signifiant "au même endroit". |
| Classification | Ils sont soit atomiques après être constitués d'un seul atome, soit moléculaires après être constitués de plusieurs atomes. | Ils sont principalement classés en deux types - instables et stables. |
| Définition | Fait référence aux atomes chargés négativement ou positivement. | Désigne les différentes variations d'atomes dans un élément. |
| Nommé par | Le physicien anglais Michael Faraday. | Suggéré par Margaret Todd à Frederick Soddy. |
Que sont les ions?
Le mot ion fait référence à un atome chargé soit négativement soit positivement, et le mot provient du mot grec "iov", qui signifie "aller". Michael Faraday, un physicien anglais, a inventé le terme.
La quantité insuffisante ou excessive d'électrons dans un atome détermine la charge positive et négative de l'atome. Par conséquent, l'atome aura une charge positive lorsqu'il y aura un excès d'électrons.
Les ions sont largement classés en atomiques et moléculaires. Les ions constitués d'un seul atome sont classés en ions atomiques ou monoatomiques.
Que sont les isotopes ?
Le mot isotopiquement d'un élément fait référence aux différentes variations d'atomes, et le mot provient des mots grecs « isos » et « topos », signifiant « au même endroit ».
Les isotopes existent principalement lorsqu'un atome contient une quantité excessive ou insuffisante de neutrons. Le nombre de protons dans tous les atomes d'un élément particulier est le même, mais le nombre de neutrons peut différer.
Les isotopes sont classés de manière significative en isotopes stables et instables. Par conséquent, les isotopes stables sont naturellement ceux qui ne se désintègrent pas.
Principales différences entre les ions et les isotopes
- Les ions peuvent être moléculaires ou atomiques, tandis que les isotopes peuvent être instables ou stables.
- Les ions existent principalement lorsqu'un atome a une quantité insuffisante ou excessive d'électrons. D'autre part, les isotopes existent principalement lorsqu'un atome a une quantité excessive ou insuffisante de neutrons.
- https://www.sciencedirect.com/science/article/abs/pii/S088329271000140X
- https://pubs.acs.org/doi/pdf/10.1021/ja00543a009
Dernière mise à jour : 11 juin 2023

Piyush Yadav a passé les 25 dernières années à travailler comme physicien dans la communauté locale. C'est un physicien passionné par l'idée de rendre la science plus accessible à nos lecteurs. Il est titulaire d'un baccalauréat en sciences naturelles et d'un diplôme d'études supérieures en sciences de l'environnement. Vous pouvez en savoir plus sur lui sur son page bio.


La façon dont les ions et les isotopes diffèrent est fascinante.
En effet, Rclark. Leurs différences sont fascinantes.
Je trouve intéressant que la différence entre les isotopes et les ions réside dans leurs propriétés physiques et non dans leurs propriétés chimiques.
Exactement, Phoebe33. Leurs différences sont assez étonnantes.
Cet article fournit une compréhension complète des ions et des isotopes.
Je n'avais jamais connu l'origine du mot « ion » auparavant.
Oui, Oscar Ross, c'est assez fascinant.
Je n'ai jamais su que les ions avaient des propriétés chimiques différentes en raison de leur charge.
En effet, Fiona Stevens. C'est assez fascinant.
J'ai appris quelque chose de nouveau grâce à ce post.
Cette comparaison des ions et des isotopes est très informative.
Je suis d'accord, Hwalsh. Cet article est très instructif.
Les principales différences entre les ions et les isotopes sont claires et bien expliquées.
En effet, John Bennett. Explications très claires.