Terminologie come Elementi e Atomi sono spesso usate durante lo studio della Chimica e talvolta della Fisica. Tuttavia, man mano che l'argomento avanza e diventa sempre più complicato, i significati dei termini possono essere facilmente confusi.
Punti chiave
- Gli elementi non possono essere scomposti in sostanze più semplici con mezzi chimici. Allo stesso tempo, gli atomi sono la particella più piccola di un elemento che conserva le proprietà chimiche di quell'elemento.
- Gli elementi hanno numeri atomici univoci che ne definiscono le proprietà e la posizione nella tavola periodica, mentre gli atomi hanno protoni, elettroni e neutroni che ne determinano il comportamento e le interazioni.
- Gli elementi possono combinarsi per formare composti, ma gli atomi dello stesso elemento non possono essere scomposti ulteriormente senza modificare le proprietà chimiche della sostanza.
Elementi contro gli atomi
Elementi e atomi differiscono perché un componente è la forma più semplicistica di una sostanza composta da atomi. Un aspetto è classificato in base al suo numero atomico. Le particelle subatomiche si combinano per formare atomi, che si fondono per creare un elemento. Successivamente, gli elementi si combinano per formare molecole.

A differenza dei composti chimici, gli elementi chimici non possono essere segmentati in sostanze più semplici con alcun metodo chimico. Nella tavola periodica degli elementi, gli elementi sono sistematizzati dal loro numero atomico.
Un atomo è la più piccola frazione di materia convenzionale che crea un elemento chimico. Un atomo è composto da particelle subatomiche. Per dirla in parole semplici, gli atomi sono i mattoni per comporre gli elementi.
Tavola di comparazione
| Parametri di confronto | Elementi | atomi |
|---|---|---|
| Taglia | Più grande degli atomi | Molto piccolo (non si vede nemmeno al microscopio) |
| Numero di tipi | Ci sono, in totale, 118 elementi. | Ci sono circa 92 tipi di atomi disponibili in natura. |
| Composizione | Un elemento specifico è costituito da un solo particolare tipo di atomo. | Gli atomi sono composti da particelle subatomiche. Sono protoni, elettroni e neutroni. |
| Quando si combinano | Gli elementi si combinano per formare nuove reazioni chimiche. | Quando gli atomi si combinano, formano una molecola. |
| Peso | Più pesante di un particolare atomo. | Estremamente leggero (il peso relativo è di 1 AMU) |
Cosa sono gli elementi?
Un elemento è un concetto fondamentale che bisogna conoscere per comprendere la chimica avanzata. Nei suoi nuclei atomici, un elemento è composto solo da atomi che contengono lo stesso numero di protoni.
Gli elementi chimici non possono essere suddivisi in elementi o sostanze più semplicistici utilizzando alcun metodo chimico. Quest'ultimo è attribuito al numero atomico, rappresentato dal simbolo 'Z.'
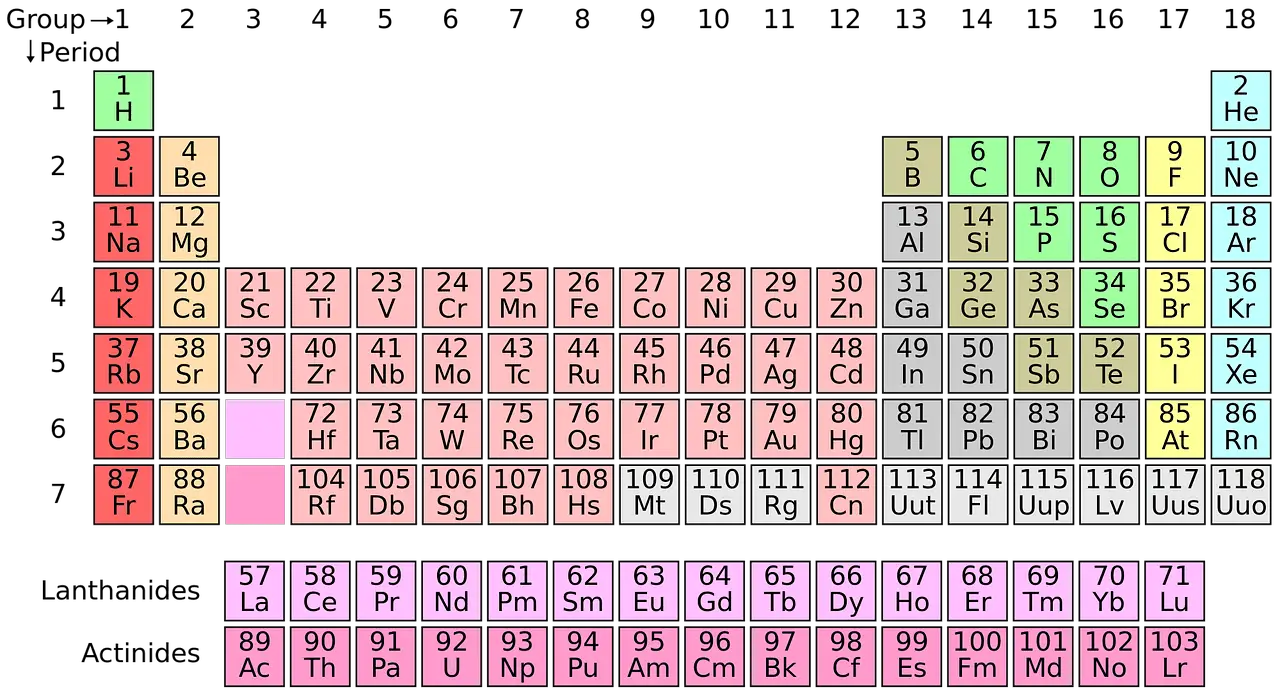
La chimica moderna dipende molto dalla tavola periodica. Tutti gli elementi scoperti sono classificati e sistematicamente organizzati nella tavola periodica. Questo concetto è stato ideato dal Russo chimico Dmitri Mendeleev nel 1869.
Le caratteristiche di un elemento sono responsabili del suo stato fisico a temperatura ambiente o media. Può essere allo stato gassoso o solido o liquido.
Ci sono circa 118 tipi di elementi in totale.
Alcuni esempi di elementi sono i seguenti:
- Idrogeno
- Carbonio
- Neon
- Magnesio
- Alluminio
- Boro
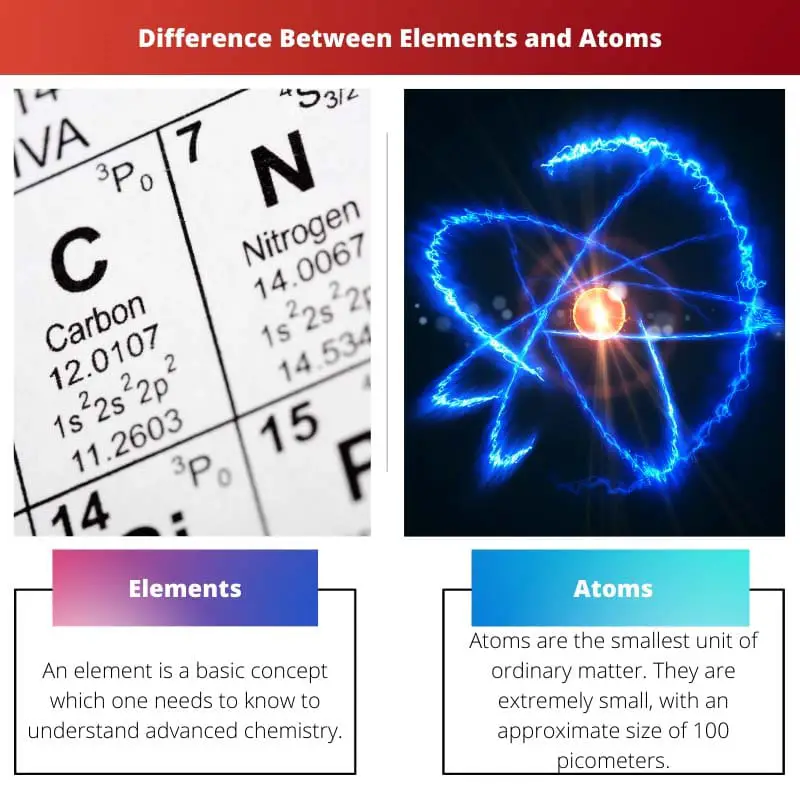
Cosa sono gli atomi?
Gli atomi sono l'unità più piccola della materia ordinaria. Sono piccoli, con una dimensione approssimativa di 100 picometri. Inoltre, un atomo è estremamente leggero. Relativamente il peso di quest'ultimo è relativamente 1AMU.
Il nucleo è composto da uno o più protoni e diversi neutroni. C'è solo un'eccezione a questa regola: l'idrogeno, che non ha neutroni. Il nucleo rappresenta il 99.94% della massa di un atomo.
I protoni possiedono una carica elettrica positiva, gli elettroni contengono una quantità elettrica negativa e i neutroni non hanno controllo elettrico. Un atomo è elettricamente neutro quando il numero di protoni e di elettroni è uguale.
In natura esistono 92 diversi tipi di atomi.
Il concetto primario e nozione che la materia comprenda minuscole particelle indivisibili sono antiche. La storia degli atomi risale ai tempi antichi dell'India e della Grecia.

Principali differenze tra elementi e atomi
- Quando più di un elemento si combina, formano una nuova reazione chimica risultante in un nuovo elemento. Quando più di un atomo si combinano (mantenendo costanti varie questioni), formano una molecola.
- Il peso dell'elemento è più pesante rispetto a quello dell'atomo, mentre, nel caso degli atomi, quest'ultimo è leggerissimo. Il peso relativo di quest'ultimo è di circa 1 AMU.
- https://books.google.com/books?hl=en&lr=&id=EvTI-ouH3SsC&oi=fnd&pg=PP1&dq=elements&ots=pQ5TOAfsJ3&sig=LBL5oWU1-cH9p_y8JPtdmdjok7g
- https://pubs.acs.org/doi/pdf/10.1021/ar00109a003
Ultimo aggiornamento: 11 giugno 2023

Piyush Yadav ha trascorso gli ultimi 25 anni lavorando come fisico nella comunità locale. È un fisico appassionato di rendere la scienza più accessibile ai nostri lettori. Ha conseguito una laurea in scienze naturali e un diploma post-laurea in scienze ambientali. Puoi leggere di più su di lui sul suo pagina bio.

Le spiegazioni approfondite hanno reso più facile cogliere le differenze tra elementi e atomi, aggiungendo un immenso valore educativo.
Il confronto dettagliato di elementi e atomi si è rivelato una risorsa educativa.
Il confronto chiaro e dettagliato di elementi e atomi ha reso più facile comprenderne le differenze, fungendo da ottimo strumento di apprendimento.
Imparare a conoscere le variazioni tra elementi e atomi da questo articolo è stato piuttosto approfondito ed educativo.
Il contenuto informativo sugli elementi e sugli atomi ha reso il confronto tra i due concetti abbastanza chiaro e comprensibile.
Questo articolo ha fornito un confronto dettagliato completo e informativo tra elementi e atomi e ha fornito una visione inestimabile delle loro rispettive caratteristiche e comportamenti.
Sono impressionato dal chiaro confronto delle differenze tra elementi e atomi fornito in questo articolo.
L'articolo ha un grande valore educativo, soprattutto per coloro che hanno un vivo interesse per la scienza e la chimica.
Questa è sicuramente una risorsa preziosa per chiunque sia interessato a conoscere elementi e atomi.
Si è rivelato utile per comprendere il concetto scientifico fondamentale di elementi e atomi.
Il confronto completo di elementi e atomi è stato illuminante, offrendo una migliore comprensione di questi concetti scientifici.
L'approfondimento del confronto tra elementi e atomi ha fornito una preziosa esperienza educativa, facilitando la comprensione di questi concetti scientifici.
Questo articolo è riuscito a fornire un confronto approfondito e completo tra elementi e atomi, che è di grande beneficio per scopi didattici e per la comprensione di concetti scientifici.
Il valore educativo del confronto tra elementi e atomi di questo articolo è davvero encomiabile.
I dettagli completi sui punti chiave degli elementi rispetto agli atomi sono molto utili per una migliore comprensione di questi concetti.