在学习化学和有时学习物理时经常使用元素和原子等术语。 然而,随着学科的发展和复杂化,术语的含义很容易混淆。
关键精华
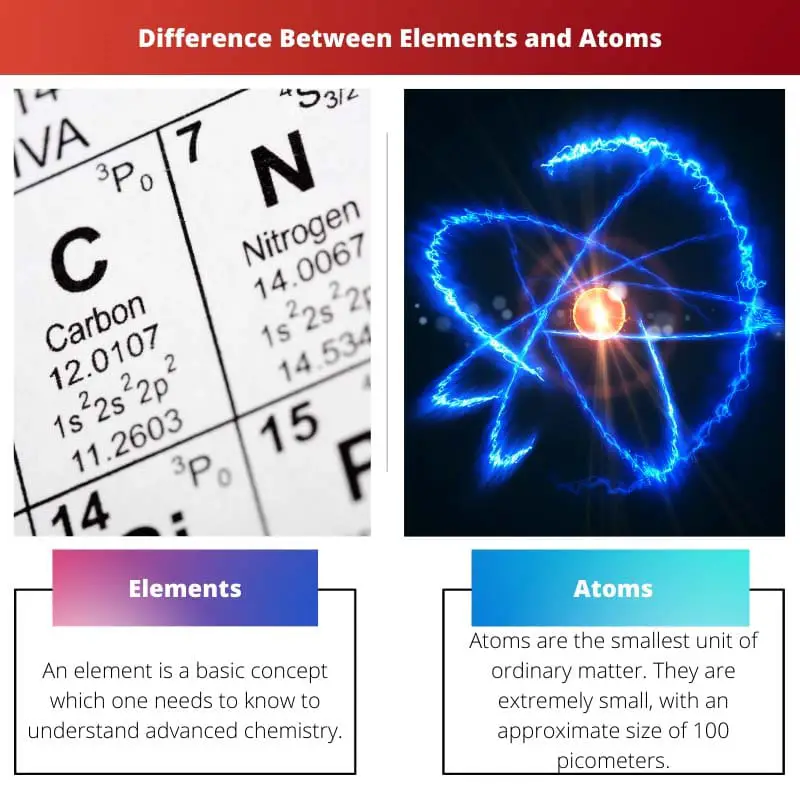
- 元素不能通过化学方法分解成更简单的物质。 同时,原子是元素中保留该元素化学性质的最小粒子。
- 元素具有独特的原子序数,定义了它们的属性和在元素周期表中的位置,而原子具有决定其行为和相互作用的质子、电子和中子。
- 元素可以结合形成化合物,但同一元素的原子不能在不改变物质化学性质的情况下进一步分解。
元素 与原子
元素和原子不同,因为组件是由原子组成的物质的最简单形式。 一个方面根据其原子序数进行分类。 亚原子粒子结合形成原子,原子结合形成元素。 后来,元素结合形成分子。

与化合物不同,化学元素不能通过任何化学方法分割成更简单的物质。 在元素周期表中,元素按其原子序数系统化。
原子是产生化学元素的常规物质的最小部分。 原子由亚原子粒子组成。 简单来说,原子是组成元素的基石。
对比表
| 比较参数 | 元素 | 原子 |
|---|---|---|
| 尺寸 | 比原子还大 | 非常小(在显微镜下甚至无法看到) |
| 种类数 | 总共有 118 个元素。 | 自然界中大约有 92 种可用的原子。 |
| 组成成分 | 特定元素仅由一种特定类型的原子组成。 | 原子由亚原子粒子组成。 它们是质子、电子和中子。 |
| 当他们结合 | 元素结合形成新的化学反应。 | 当原子结合时,它们形成分子。 |
| 重量 | 比特定原子重。 | 极轻(相对重量为 1 AMU) |
什么是元素?
元素是理解高等化学所必须知道的基本概念。 在其原子核中,元素仅由包含相同数量质子的原子组成。
不能使用任何化学方法将化学元素划分为更简单的元素或物质。 后者归于原子序数,由 符号 “Z.'
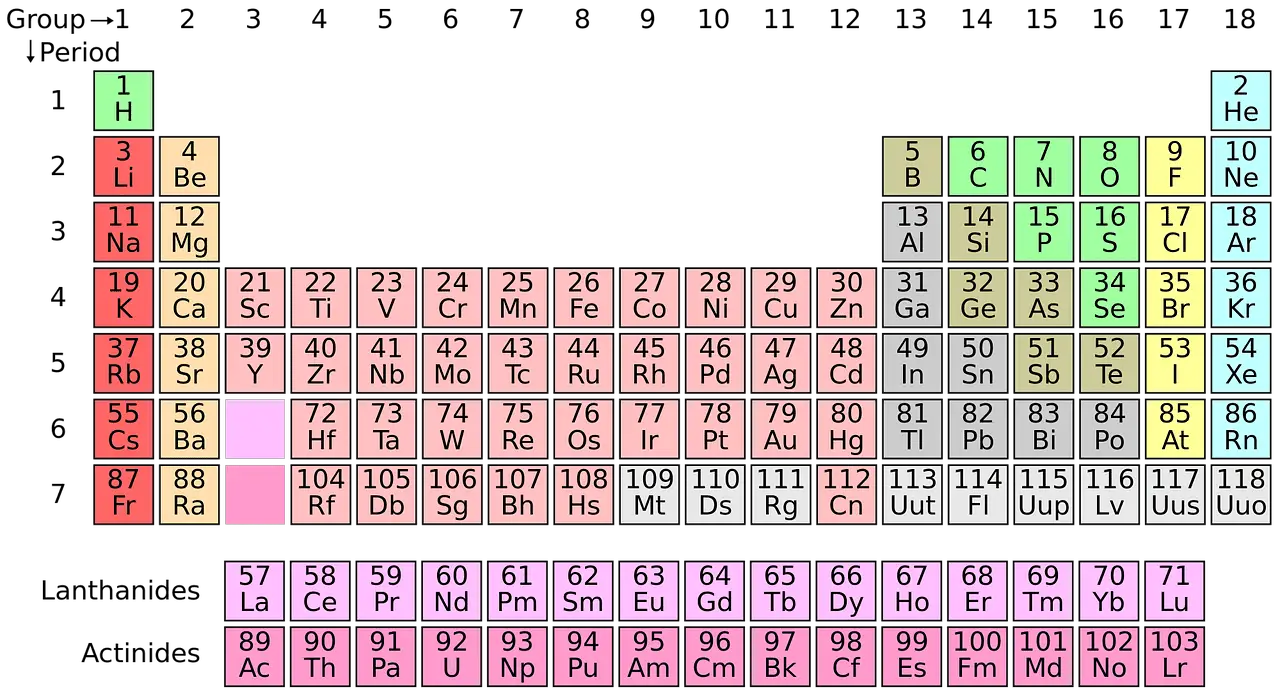
现代化学在很大程度上取决于周期表。 所有发现的元素都被分类并系统地组织在元素周期表中。 这个概念是由 俄语 1869 年,化学家德米特里·门捷列夫 (Dmitri Mendeleev)。
元素的特性决定了它在室温或平均温度下的物理状态。 它可以是气态,也可以是固态或液态。
总共有大约 118 种元素。
元素的几个例子如下:
- 氢
- 碳
- 氖
- 镁
- 铝
- 硼
什么是原子?
原子是普通物质的最小单位。 它们很小,大约有 100 皮米。 此外,原子的重量非常轻。 相对后者的权重是1AMU。
原子核由一个或多个质子和若干个中子组成。 这条规则只有一个例外:氢,它没有中子。 核心占原子质量的99.94%。
质子带正电荷,电子带负电荷,中子不带电。 当质子数和电子数相等时,原子呈电中性。
自然界中有 92 种不同类型的原子。
基本概念和 概念 物质由不可分割的微小粒子组成是古老的。 原子的历史可以追溯到古代印度和希腊。

元素和原子之间的主要区别
- 当不止一种元素结合时,它们会形成一种新的化学反应,从而产生一种新元素。 当多个原子结合时(保持各种物质不变),它们就形成了一个分子。
- 与原子的重量相比,元素的重量更重,而对于原子,后者非常轻。 后者的相对重量约为 1 AMU。
- https://books.google.com/books?hl=en&lr=&id=EvTI-ouH3SsC&oi=fnd&pg=PP1&dq=elements&ots=pQ5TOAfsJ3&sig=LBL5oWU1-cH9p_y8JPtdmdjok7g
- https://pubs.acs.org/doi/pdf/10.1021/ar00109a003
最后更新时间:11 年 2023 月 XNUMX 日

Piyush Yadav 在过去的 25 年里一直在当地社区担任物理学家。 他是一位物理学家,热衷于让我们的读者更容易理解科学。 他拥有自然科学学士学位和环境科学研究生文凭。 你可以在他的网站上阅读更多关于他的信息 生物页面.

深入的解释使人们更容易掌握元素和原子之间的差异,增加了巨大的教育价值。
元素和原子的详细比较已被证明是一项教育资产。
元素和原子的清晰详细的比较使人们更容易理解它们的差异,是一个很好的学习工具。
从这篇文章中了解元素和原子之间的差异是非常有洞察力和教育意义的。
关于元素和原子的信息内容使这两个概念之间的比较变得非常清晰易懂。
本文对元素和原子进行了全面且内容丰富的详细比较,并对它们各自的特征和行为提供了宝贵的见解。
本文对元素和原子之间差异的清晰比较给我留下了深刻的印象。
这篇文章具有很大的教育价值,特别是对于那些对科学和化学有浓厚兴趣的人来说。
对于任何有兴趣了解元素和原子的人来说,这绝对是宝贵的资源。
事实证明,它对于理解元素和原子的基本科学概念具有价值。
元素和原子的全面比较具有启发性,可以更好地理解这些科学概念。
深入研究元素和原子的比较提供了宝贵的教育经验,使人们更容易理解这些科学概念。
本文成功地提供了元素和原子之间富有洞察力和全面的比较,这对于教育目的和理解科学概念非常有益。
这篇文章对元素和原子的比较的教育价值确实值得称赞。
有关元素与原子的关键要点的全面详细信息对于更好地理解这些概念非常有帮助。