Vzhledem k tomu, že mezi pojmy frakční destilace a jednoduchá destilace existuje mnoho zmatků, mnoho lidí to považuje za stejný termín s jiným názvem.
Jedná se o proces, při kterém jsou chemické sloučeniny součástí varu na teplotu, ze které se odpaří jedna nebo více frakcí směsi. Je to metoda, která používá k frakcionaci destilaci.
Metoda může být použita k rozdělení kapaliny s rozdílem alespoň padesáti stupňů v teplotě varu. Destilace vody je jedním příkladem jednoduché destilace.
Key Takeaways
- Frakční destilace odděluje složky směsi na základě různých bodů varu pomocí frakcionační kolony.
- Jednoduchá destilace zahrnuje zahřívání směsi a shromažďování páry, což je ideální pro separaci látek s výrazně odlišnými body varu.
- Frakční destilace je účinnější pro směsi s blízkými body varu, zatímco jednoduchá destilace vyhovuje směsím s velkými rozdíly v bodech varu.
Frakční destilace vs jednoduchá destilace
Při jednoduché destilaci se oddělí dvě kapaliny s výrazně odlišnými body varu. Když se kapalina s nižším bodem varu vypařuje jako první, druhá kapalina je ponechána ke kondenzaci. Pomocí trubice se frakční destilací oddělují kapaliny se stejným bodem varu.

Srovnávací tabulka
| Parametr srovnání | Frakční destilace | Jednoduchá destilace |
|---|---|---|
| Význam | Frakční destilace je proces rozdělování směsi na její části. | Jednoduchá destilace je proces oddělení dvou kapalin s různými body varu. |
| Bod varu | Frakční destilací lze oddělit směs, která má body varu blízko sebe. | Jednoduchá destilace může oddělit směs padesát stupňů rozdílu v jejich varu. |
| Příklad | K rafinaci ropy se používá frakční destilace. | K čištění mořské vody se používá jednoduchá destilace. |
| Používá se pro | Pokud jde o případ použití, frakční destilace využívá složité zařízení s frakcionační kolonou. | Když už mluvíme o použitém případu, jednoduchá destilace využívá složité zařízení s frakcionační kolonou. |
| Opakování | Při frakční destilaci se tento proces musí provést mnohokrát, aby se získala čistá složka. | Jednoduchá destilace je, když poprvé získáme čisté složky. |
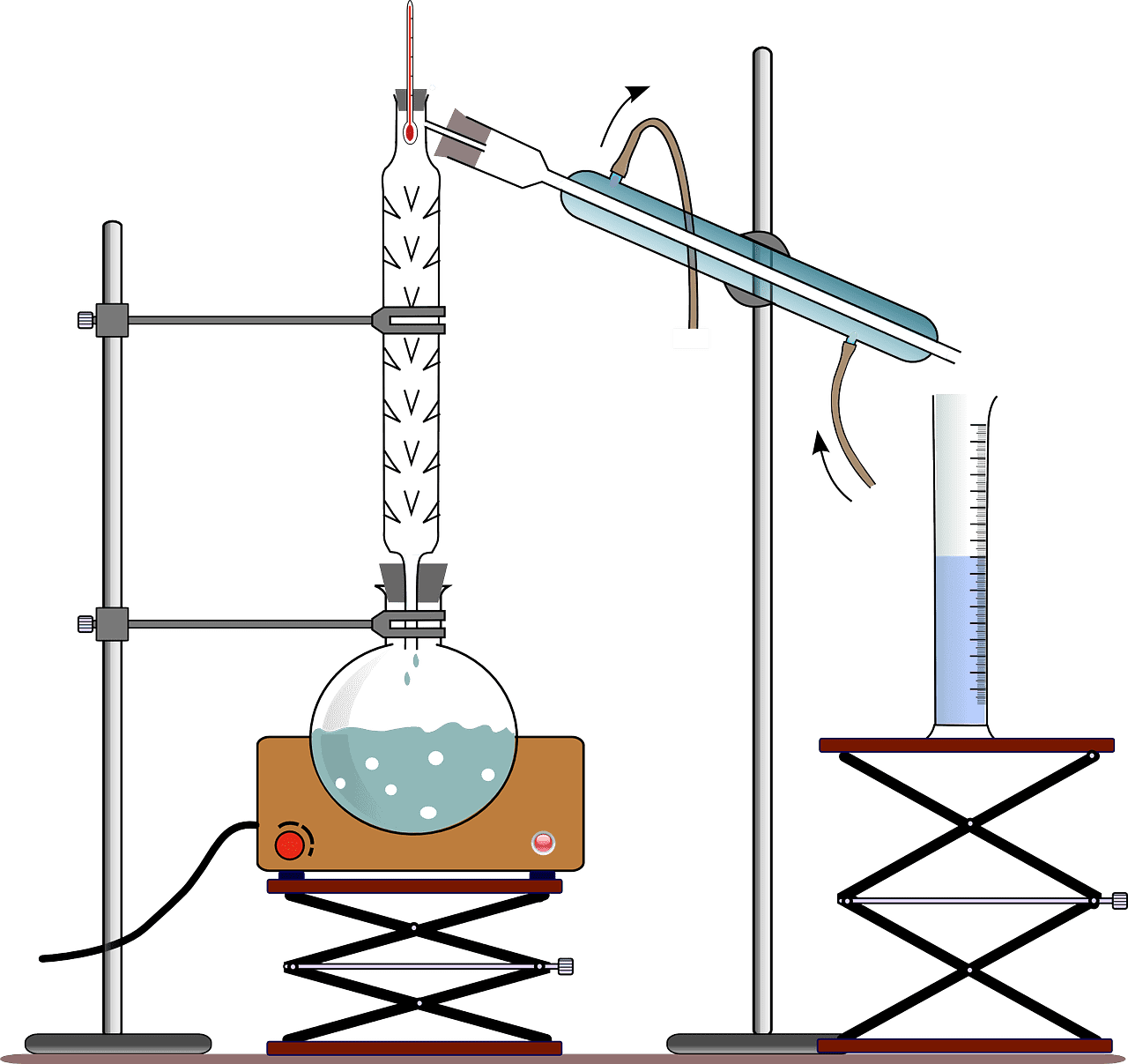
Co je frakční destilace?
Federální destilace odděluje chemické sloučeniny od sebe, když je rozdíl teplot varu menší než čtyřicet stupňů.
Tento proces zajišťuje, že se kondenzace učí do konce kondenzátor co nejdříve. Jedním příkladem frakční destilace je ropa rozdělená na různé složky.
Frakční destilace využívá frakcionační kolonu, protože kapalná směs má podobný bod varu. Frakcionační kolona působí jako překážka vzestupu plyn.
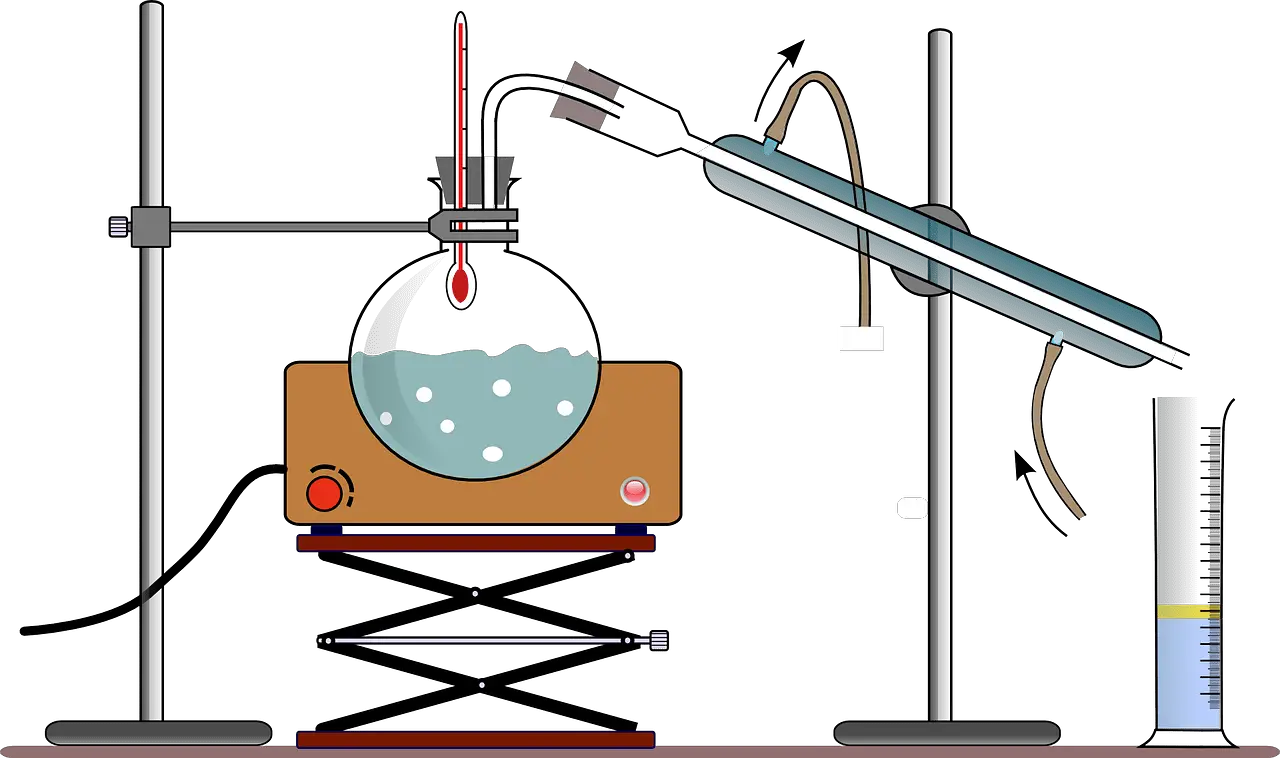
Co je jednoduchá destilace?
Jednoduchá destilace je metoda dělení dvou složek, které mají různé teploty varu. Dokáže rozdělit kapaliny s nejméně padesáti stupni různými body varu.
Rafinované sloučeniny se zahřejí a přemění na kondenzaci při relativně nízkých teplotách 2 nebo 3 stupňů Celsia; při pohledu na teplotu destilační baňky je možné ovlivnit dobré rozdělení ve sloučenině.
Tento proces jednoduché destilace bude pokračovat, dokud se původní směs neoddělí. Jednoduchá destilace je nejlepší pro kapalinu s jiným bodem varu.
Hlavní rozdíly mezi Frakční destilace a jednoduchá destilace
- Jak jednoduché, tak frakční destilační procesy jsou všechny o rozdělení různých vlastností kapalin.
- Pokud mají dvě nebo více kapalin navzájem blízkou teplotu varu, pak je můžeme oddělit frakční destilací; na druhé straně jednoduchá destilace je proces oddělování kapaliny, který má padesátistupeň rozdíl v bodu varu.
- https://aocs.onlinelibrary.wiley.com/doi/abs/10.1007/BF02667433
- https://pubs.acs.org/doi/pdf/10.1021/ac60061a012
Poslední aktualizace: 11. června 2023

Piyush Yadav strávil posledních 25 let prací jako fyzik v místní komunitě. Je to fyzik, který je zapálený pro zpřístupnění vědy našim čtenářům. Je držitelem titulu BSc v přírodních vědách a postgraduálního diplomu v oboru environmentální vědy. Více si o něm můžete přečíst na jeho bio stránka.

Článek poskytuje jasný rozdíl mezi metodami frakční a jednoduché destilace.
Přehlednost ve srovnání je chvályhodná.
Rozdíl je jistě efektivně objasněn.
Rozdíl mezi těmito dvěma destilačními metodami je v článku dobře definován.
Srovnání je samozřejmě jasně formulováno.
Zajímavý článek, ale mohl se ponořit hlouběji do vědeckých nuancí metod.
Vědecké složitosti mohly být prozkoumány důkladněji.
Souhlasím, větší vědecká hloubka by srovnání přinesla přidanou hodnotu.
Článek je napsán poměrně zjednodušeně.
Ano, ocenil by se podrobnější přístup.
Srovnání mohlo být prezentováno poutavějším způsobem.
Souhlasím, poutavější prezentace by článek vylepšila.
Článek postrádá poutavý obsah.
Tento článek přesně shrnuje rozdíly a použití frakční a jednoduché destilace, zajímavé čtení.
Vskutku! Poskytuje jasné pochopení tématu.
Zajímavý pohled na srovnání mezi metodou frakční a jednoduché destilace.
Ano, praktické příklady jsou docela užitečné při objasňování pojmů.
Použití praktických příkladů usnadňuje pochopení.
Informativní článek, který poskytuje podrobné srovnání metod frakční a jednoduché destilace.
Detailní srovnání metod je chvályhodné.
Uvedené příklady dodávají srovnání hloubku.
V článku chybí vědecký přístup k vysvětlení.
Vědecké principy mohly být skutečně vysvětleny jasněji.
Článek neposkytuje vyčerpávající vysvětlení rozdílů.
Souhlasím, postrádá to hloubku a důkladnost.