Organska kemija je najraznovrsnije i najvažnije područje studija. Ne samo da olakšava razumijevanje života, već nas vodi i do kemije koja je uključena u formiranje čestica na niskoj razini.
Spojevi u organskoj kemiji reagiraju s različitim atomima, reagensima i drugim spojevima kako bi formirali potpuno drugačiji proizvod s drugačijim karakteristikama nego prije.
Ugljikovi lanac jedna je od primarnih baza identifikacije u organskoj kemiji, a lanac tvori okruglu kružnu strukturu formiranjem specifičnih veza.
Benzenov prsten tvori najvažniji spoj, prstenastog oblika sa 6 atoma ugljika. Atomi ugljika dalje su vezani s atomima vodika.
Zamjenom sljedećih atoma vodika s različitim funkcionalnim skupinama nastaje drugačiji spoj.
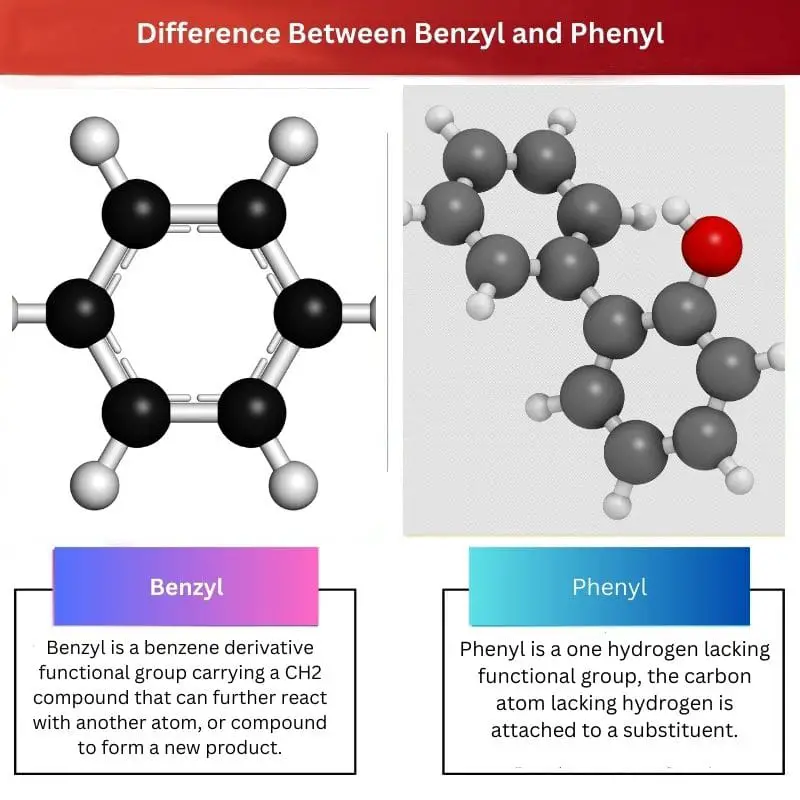
Benzil i fenil pokazuju sličnost u strukturi budući da oba imaju strukturu u obliku prstena, to jest benzena, ali ipak tvore različite funkcionalne skupine.
Ključni za poneti
- Benzil je kemijski supstituent iz toluena, koji se sastoji od fenilnog prstena vezanog za CH2 skupinu (C6H5CH2-).
- Fenil je kemijski supstituent sastavljen od benzenskog prstena bez jednog atoma vodika (C6H5-), koji se može vezati s drugim atomima ili skupinama.
- Ključna razlika između benzila i fenila leži u njihovoj molekularnoj strukturi: benzil sadrži dodatnu CH2 skupinu, dok je fenil samo benzenski prsten minus jedan vodik.
Benzil protiv fenila
Benzil je kemijski spoj koji sadrži benzenski prsten vezan metilnom skupinom. Dolazi prije organske skupine kako bi pokazao prisutnost određene skupine. Fenil je kemijski spoj uključen u benzenski prsten bez dodatnih supstituenata.

Tabela za usporedbu
| Parametar usporedbe | Benzil | Fenil |
|---|---|---|
| Definicija | Benzil je funkcionalna skupina derivata benzena koja nosi CH2 spoj koji može dalje reagirati s drugim atomom ili spoj za stvaranje novog produkta. | Fenil je funkcionalna skupina s jednim vodikom, atom ugljika bez vodika vezan je za supstituent. |
| Molekularna formula | Molekularna formula benzila je C6H5CH2 | Molekulska formula fenila je C6H5 |
| Reaktivnost | Reaktivnost je visoka zbog slabe veze između CH atoma. | Energija potrebna za kidanje CH veze je vrlo visoka, a reaktivnost je niska. |
| skraćenica | Bn se koristi u terminologiji dok radi i reagira s drugim spojevima. | Skraćeno je Ph. |
| Prednost | Opsežno se koriste kao zaštitna skupina za karboksilne kiseline. | Koriste se u medicini i također za zaustavljanje oksidacije i redukcije. |
Što je Benzyl?
Benzil je derivat benzena s nekoliko izmjena. Prsten je skraćeno "Bn."
To je funkcionalna skupina, dakle odgovorna za kemijska svojstva molekula koje tvore.
Kemijski sastav benzila sastoji se od atoma ugljika i vodika raspoređenih u nizu vezanom za CH2 skupina.
Kemijska formula je C6H5CH2; prema tome, benzil je izveden iz toluena koji je C6H5CH3, tvoreći monovalentni radikal.
Veze ugljika i vodika nisu jake. Stoga je vanjska energija potrebna za kidanje veze niska, oko 90 Kcal/mol, i dalje se mijenja za metilne i etilne CH veze.
Reaktivnost je visoka zbog slabe energije veze; spojevi koje on stvara su benzil metil, benzilamin itd.
Koriste se u organskoj znanosti za zaštitu karboksilnih kiselina i alkohola.
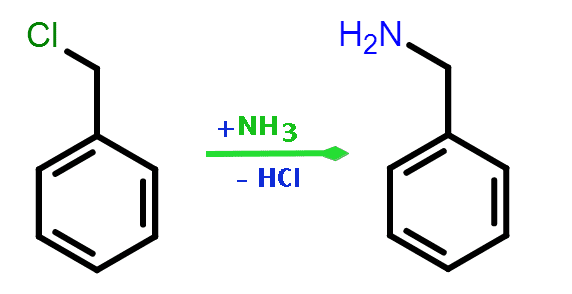
Što je Phenyl?
Skraćeno kao Ph, fenil je derivat cikličke funkcionalne skupine benzenskog prstena i posjeduje određena svojstva slična onima benzena.
Molekularna težina je 77g mol-1, a formula je C6H5.
Zbog nedostatka jednog atoma vodika, benzen fenil može se lako povezati sa sljedećim atomom, molekulom ili drugom fenilnom skupinom.
Energija potrebna za prekid veze vrlo je visoka zbog jake atomske veze; potrebna energija za prekid veze je 113 Kcal/mol; varira s vezama stvorenim s različitim atomima; na primjer, s vezanim metilom, energija disocijacije je 105 Kcal/mol, dok je s etilom potrebna energija 101 Kcal/mol.
Reaktivnost fenila je vrlo niska zbog jake veze ugljika i vodika. Poput benzena, čak je i fenil sp2 hibridiziran.
Svojstva fenila mijenjaju se s promjenom supstituenata; supstituent može biti donor ili elektroni i također se povući.
U medicinske svrhe koriste se spojevi s fenilom kao funkcionalnom skupinom. Alergije i problemi povezani s kolesterolom mogu se liječiti atorvastatinom i fenilom koji sadrži feksofenadin.
Fenil se također svakodnevno koristi kao kućno dezinfekcijsko sredstvo i za sanitarne svrhe u domu, školama, hotelima ili bilo gdje gdje je to potrebno.
Glavne razlike između benzila i fenila
- Glavna razlika između benzila i fenila je da je benzil izravno izveden iz toluena i da mu nedostaje atom vodika. Fenil je benzenski prsten bez atoma vodika; obje su funkcionalne skupine.
- Kemijska formula benzila je C6H5CH2, dok je kod fenila C6H5
- Benzil je reaktivan organski spoj zbog niske energije disocijacije između vezanih atoma ugljika i vodika, ali je veza u fenilu jača i stoga manje reaktivna.
- U benzilu, energija potrebna za kidanje CH veza je morate 90 kcal/mol, dok je za fenil potrebna vrlo visoka energija za raskid veze, potrebna energija je 113 kcal/mol.
- Benzil je skraćeno Bn, dok je fenilni spoj pojednostavljen na Ph.for. Na primjer, benzil alkohol je predstavljen kao BnOH, dok se benzen može predstaviti kao PhH.
- https://www.sciencedirect.com/science/article/pii/S1386142512006051
- https://www.sciencedirect.com/science/article/pii/S0031942205004206
Zadnje ažuriranje: 11. lipnja 2023

Piyush Yadav proveo je posljednjih 25 godina radeći kao fizičar u lokalnoj zajednici. On je fizičar koji strastveno želi učiniti znanost dostupnijom našim čitateljima. Posjeduje diplomu prirodnih znanosti i poslijediplomski studij znanosti o okolišu. Više o njemu možete pročitati na njegovom bio stranica.


Razjašnjenje ključnih razlika između benzila i fenila ključno je za svakoga tko se bavi kemijskim istraživanjem i razvojem farmaceutskih supstanci.
Doista, razumijevanje ovih nijansi ključno je za istraživače i znanstvenike koji teže značajnom doprinosu u području kemijske znanosti.
Apsolutno, uvidi dobiveni takvim usporedbama ključni su za poticanje inovacija i napretka u organskoj kemiji i otkrivanju lijekova.
Praktične implikacije benzila i fenila u svakodnevnim proizvodima i ljekovitim tvarima naglašavaju važnost organske kemije u našem svakodnevnom životu.
Apsolutno, prožimajući utjecaj organske kemije u raznim domenama naglašava njenu temeljnu važnost u modernom društvu.
Razlika između benzila i fenila i njihovih odgovarajućih svojstava daje neprocjenjiv uvid u kemijsku reaktivnost i primjenu ovih spojeva.
Doista, precizno razumijevanje ovih razlika ključno je pri radu s organskim spojevima i razvoju novih proizvoda.
Smatram da je fascinantno kako male razlike u molekularnim strukturama mogu rezultirati tako raznolikim karakteristikama spojeva. Doista, organska kemija je uistinu zadivljujuća.
To je poput rješavanja složene zagonetke u kojoj je svaki spoj jedinstveni dio koji se uklapa u širu sliku organske kemije. Zaista očaravajuće.
Praktična korisnost benzila i fenila u raznim sferama znanosti i medicine dokaz je nezamjenjivosti organske kemije u unapređenju ljudskog znanja i dobrobiti.
Apsolutno, doprinosi organske kemije područjima od farmaceutskih proizvoda do znanosti o materijalima doista su izvanredni i dalekosežni.
Nijansirane razlike između benzila i fenila i njihove primjene primjer su složenosti i zamršenosti organske kemije.
Doista, dubina razumijevanja potrebna za shvaćanje ovih suptilnosti govori o sofisticiranosti organske kemije kao znanstvene discipline.
Pedantna usporedba između benzila i fenila pruža sveobuhvatno razumijevanje njihovih jedinstvenih karakteristika i primjena u kemijskoj sintezi i medicinskoj kemiji.
Doista, ove detaljne usporedbe su neprocjenjive za istraživače i znanstvenike koji rade u domeni organske kemije i farmacije.
Visoka reaktivnost benzila zbog njegove slabije energije veze i niska reaktivnost fenila koja se pripisuje njegovoj jakoj atomskoj vezi uvjerljivi su aspekti koje treba razmotriti u organskoj sintezi i farmaceutskim primjenama.
Doista, praktične implikacije ovih svojstava u razvoju medicinskih spojeva i farmaceutskih supstanci ne mogu se podcijeniti.
Apsolutno, značaj ovih razlika u razinama reaktivnosti ključan je za razumijevanje funkcionalnosti različitih kemijskih spojeva u primjenama u stvarnom svijetu.
Složenost i raznolikost organske kemije ne prestaju me iznenađivati. Zamršenost molekularnih struktura i razina reaktivnosti doista ga čine nezamjenjivim područjem proučavanja u modernoj znanosti.
Apsolutno, dubina razumijevanja potrebna za razumijevanje nijansi organske kemije dokaz je značaja ovog područja.
Korištenje benzila i fenila u različitim poljima, kao što je zaštita karboksilnih kiselina ili u medicinskim primjenama, pokazuje svestranu prirodu ovih kemijskih skupina.
Apsolutno, višestruke uloge benzila i fenila čine ih sastavnim komponentama organske kemije i farmaceutskih istraživanja.
Svakako, prilagodljivost ovih spojeva u različitim područjima znanosti i medicine pokazuje njihovu nezamjenjivost.