Terminologije poput elemenata i atoma često se koriste tijekom studija kemije, a ponekad i fizike. Međutim, kako predmet napreduje i postaje sve kompliciraniji, značenja pojmova mogu se lako zbuniti.
Ključni za poneti
- Elementi se ne mogu kemijskim putem rastaviti na jednostavnije tvari. Ujedno, Atomi su najmanje čestice nekog elementa koje zadržavaju kemijska svojstva tog elementa.
- Elementi imaju jedinstvene atomske brojeve koji definiraju njihova svojstva i položaj u periodnom sustavu, dok atomi imaju protone, elektrone i neutrone koji određuju njihovo ponašanje i interakcije.
- Elementi se mogu kombinirati u spojeve, ali atomi istog elementa ne mogu se dalje razgraditi bez promjene kemijskih svojstava tvari.
Elementi protiv atoma
Elementi i atomi se razlikuju jer je komponenta najjednostavniji oblik tvari sačinjene od atoma. Aspekt se klasificira ovisno o njegovom atomskom broju. Subatomske čestice spajaju se u atome, koji se spajaju i stvaraju element. Kasnije se elementi spajaju u molekule.

Za razliku od kemijskih spojeva, kemijski elementi se ne mogu niti jednom kemijskom metodom segmentirati u jednostavnije tvari. U periodnom sustavu elemenata elementi su sistematizirani prema svom atomskom broju.
Atom je najsitniji djelić konvencionalne materije koji stvara kemijski element. Atom se sastoji od subatomskih čestica. Jednostavnim riječima, atomi su građevni blokovi za sastavljanje elemenata.
Tabela za usporedbu
| Parametri usporedbe | Elementi | atomi |
|---|---|---|
| Veličina | Veći od atoma | Vrlo mali (ne može se vidjeti ni pod mikroskopom) |
| Broj vrsta | Ukupno ima 118 elemenata. | U prirodi postoje približno 92 vrste atoma. |
| Sastav | Određeni element sastoji se od samo jedne određene vrste atoma. | Atomi se sastoje od subatomskih čestica. Oni su protoni, elektroni i neutroni. |
| Kad se spoje | Elementi se spajaju stvarajući nove kemijske reakcije. | Kada se atomi spoje, formiraju molekulu. |
| Težina | Teži od određenog atoma. | Izuzetno lagan (relativna težina je 1 AMU) |
Što su Elementi?
Element je temeljni koncept koji čovjek mora znati da bi razumio naprednu kemiju. U svojim atomskim jezgrama, element se sastoji samo od atoma koji sadrže isti broj protona.
Kemijski elementi ne mogu se podijeliti na jednostavnije elemente ili tvari niti jednom kemijskom metodom. Potonji se pripisuje atomskom broju, predstavljenom s simbol 'Z.'
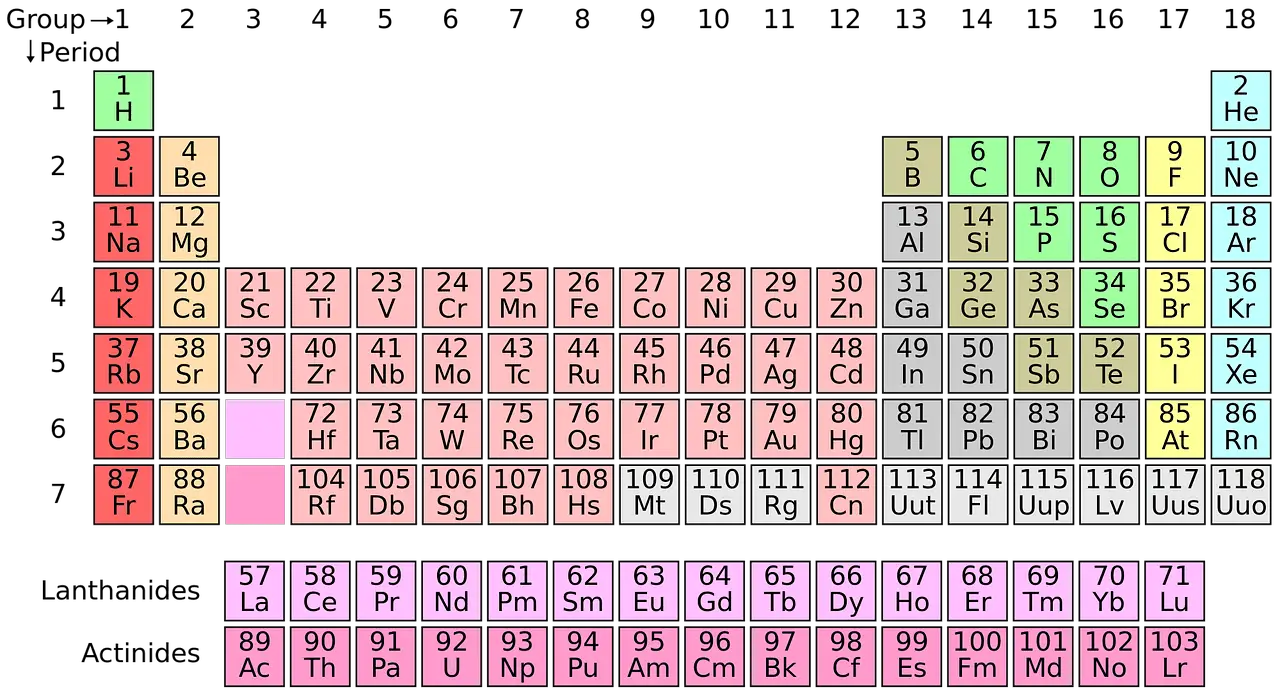
Moderna kemija uvelike ovisi o periodnoj tablici. Svi otkriveni elementi kategorizirani su i sustavno organizirani u periodnom sustavu. Ovaj koncept je osmislio ruski kemičar Dmitrij Mendeljejev 1869.
Karakteristike elementa odgovorne su za njegovo fizičko stanje na sobnoj ili prosječnoj temperaturi. Može biti u plinovitom stanju, krutom ili tekućem.
Ukupno postoji oko 118 vrsta elemenata.
Nekoliko primjera elemenata su sljedeći:
- Vodik
- ugljen
- neon
- Magnezij
- Aluminij
- Bor
Što su Atomi?
Atomi su najmanja jedinica obične materije. Sićušni su, veličine približno 100 pikometara. Također, atom je izuzetno male težine. Relativna težina potonjeg je relativno 1AMU.
Jezgra se sastoji od jednog ili više protona i nekoliko neutrona. Postoji samo jedna iznimka od ovog pravila: vodik, koji nema neutrone. Na jezgru otpada 99.94% mase atoma.
Protoni posjeduju pozitivan električni naboj, elektroni sadrže negativan električni naboj, a neutroni nemaju električnu kontrolu. Atom je električki neutralan kada je broj protona i elektrona jednak.
U prirodi postoje 92 različite vrste atoma.
Primarni koncept i pojam da se materija sastoji od sićušnih nedjeljivih čestica drevni su. Povijest atoma seže u staro doba Indije i Grčke.

Glavne razlike između elemenata i atoma
- Kada se više od jednog elementa kombinira, oni tvore novu kemijsku reakciju koja rezultira novim elementom. Kada se više od jednog atoma spoji (održavajući različite tvari konstantnima), oni formiraju molekulu.
- Težina elementa veća je u usporedbi s težinom atoma, dok je, u slučaju atoma, potonji iznimno lagan. Relativna težina potonjeg je približno 1 AMU.
- https://books.google.com/books?hl=en&lr=&id=EvTI-ouH3SsC&oi=fnd&pg=PP1&dq=elements&ots=pQ5TOAfsJ3&sig=LBL5oWU1-cH9p_y8JPtdmdjok7g
- https://pubs.acs.org/doi/pdf/10.1021/ar00109a003
Zadnje ažuriranje: 11. lipnja 2023

Piyush Yadav proveo je posljednjih 25 godina radeći kao fizičar u lokalnoj zajednici. On je fizičar koji strastveno želi učiniti znanost dostupnijom našim čitateljima. Posjeduje diplomu prirodnih znanosti i poslijediplomski studij znanosti o okolišu. Više o njemu možete pročitati na njegovom bio stranica.

Detaljna objašnjenja olakšala su shvaćanje razlika između elemenata i atoma, dodajući golemu obrazovnu vrijednost.
Detaljna usporedba elemenata i atoma pokazala se kao obrazovna vrijednost.
Jasna i detaljna usporedba elemenata i atoma olakšala je razumijevanje njihovih razlika, služeći kao odličan alat za učenje.
Učenje o varijacijama između elemenata i atoma iz ovog članka bilo je prilično pronicljivo i poučno.
Informativni sadržaj o elementima i atomima učinio je usporedbu između ta dva pojma sasvim jasnom i razumljivom.
Ovaj je članak pružio sveobuhvatnu i informativnu detaljnu usporedbu između elemenata i atoma te je dao neprocjenjiv uvid u njihove značajke i ponašanja.
Impresioniran sam jasnom usporedbom razlika između elemenata i atoma koja je navedena u ovom članku.
Članak ima veliku edukativnu vrijednost, posebice za one koji imaju veliki interes za znanost i kemiju.
Ovo je definitivno vrijedan izvor za svakoga tko je zainteresiran za učenje o elementima i atomima.
Pokazalo se vrijednim u razumijevanju temeljnog znanstvenog koncepta elemenata i atoma.
Sveobuhvatna usporedba elemenata i atoma bila je prosvjetljujuća, nudeći bolje razumijevanje ovih znanstvenih koncepata.
Duboko poniranje u usporedbu elemenata i atoma pružilo je vrijedno obrazovno iskustvo, olakšavajući razumijevanje ovih znanstvenih koncepata.
Ovaj članak je uspio pružiti pronicljivu i sveobuhvatnu usporedbu između elemenata i atoma, što je vrlo korisno za obrazovne svrhe i razumijevanje znanstvenih koncepata.
Edukativna vrijednost usporedbe elemenata i atoma u ovom članku doista je hvale vrijedna.
Sveobuhvatne pojedinosti o ključnim zaključcima elemenata u odnosu na atome vrlo su korisne za bolje razumijevanje ovih koncepata.