Terminologi seperti Unsur dan Atom sering digunakan saat mempelajari Kimia dan terkadang Fisika. Namun, seiring kemajuan subjek dan semakin rumit, arti dari istilah-istilah tersebut dapat dengan mudah membingungkan.
Pengambilan Kunci
- Unsur tidak dapat diuraikan menjadi zat yang lebih sederhana dengan cara kimia. Pada saat yang sama, Atom adalah partikel terkecil dari suatu unsur yang mempertahankan sifat kimia unsur tersebut.
- Unsur memiliki nomor atom unik yang menentukan sifat dan lokasinya pada tabel periodik, sedangkan Atom memiliki proton, elektron, dan neutron yang menentukan perilaku dan interaksinya.
- Unsur dapat bergabung membentuk senyawa, tetapi atom dari unsur yang sama tidak dapat dipecah lebih lanjut tanpa mengubah sifat kimia zat tersebut.
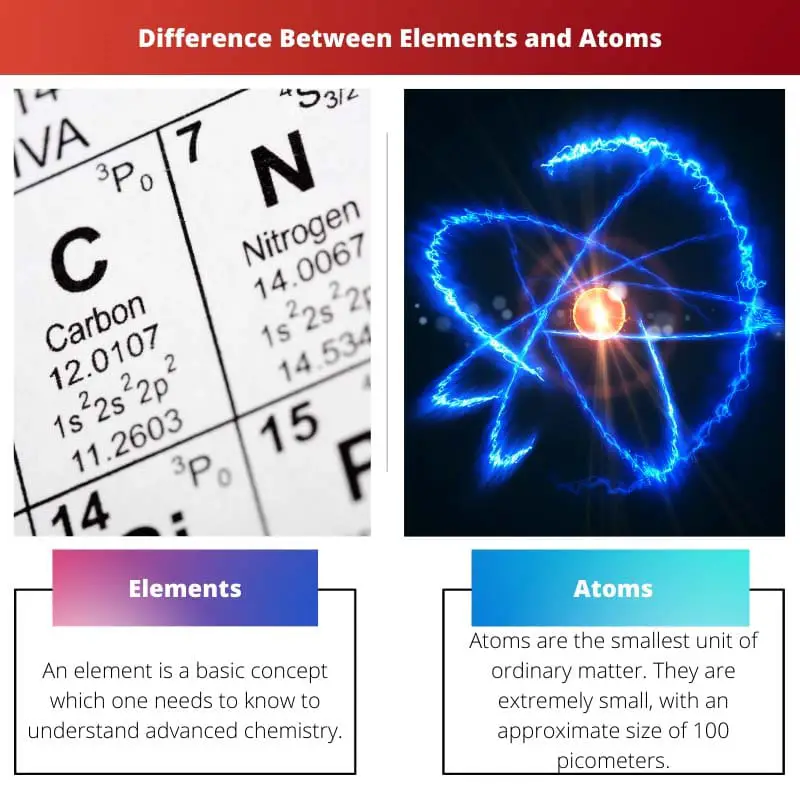
Elemen vs. Atom
Unsur dan Atom berbeda karena komponen adalah bentuk paling sederhana dari suatu zat yang terdiri dari atom. Suatu aspek diklasifikasikan tergantung pada nomor atomnya. Partikel subatomik bergabung membentuk atom, yang bergabung untuk menciptakan suatu unsur. Kemudian, unsur-unsur bergabung membentuk molekul.

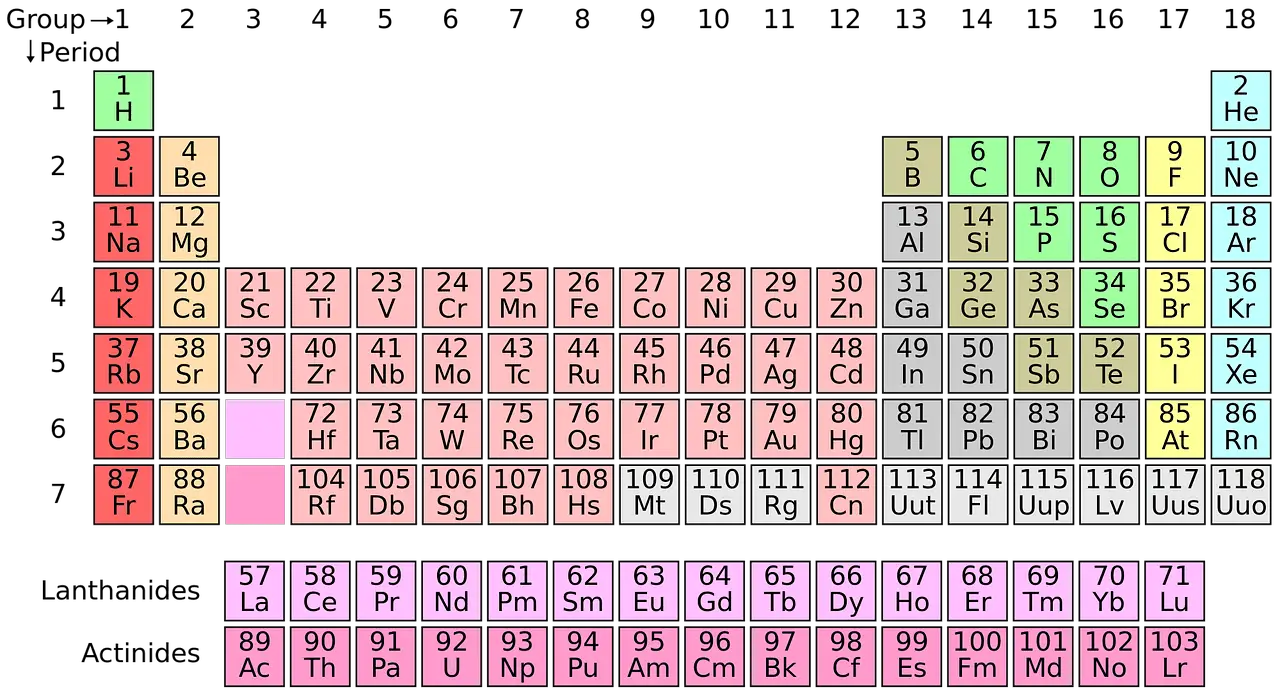
Tidak seperti senyawa kimia, unsur kimia tidak dapat dibagi menjadi zat yang lebih sederhana dengan metode kimia apa pun. Dalam tabel periodik unsur, unsur-unsur disistematisasikan berdasarkan nomor atomnya.
Atom adalah fraksi terkecil dari materi konvensional yang menciptakan unsur kimia. Sebuah atom terdiri dari partikel subatomik. Sederhananya, atom adalah blok bangunan untuk menyusun elemen.
Tabel perbandingan
| Parameter Perbandingan | Elemen | Atom |
|---|---|---|
| Ukuran | Lebih besar dari atom | Sangat kecil (bahkan tidak dapat dilihat di bawah mikroskop) |
| Jumlah jenis | Ada, secara total, 118 elemen. | Ada sekitar 92 jenis atom yang tersedia di alam. |
| Komposisi | Unsur tertentu hanya terdiri dari satu jenis atom tertentu. | Atom terdiri dari partikel subatomik. Mereka adalah proton, elektron, dan neutron. |
| Ketika mereka bergabung | Elemen bergabung untuk membentuk reaksi kimia baru. | Ketika atom bergabung, mereka membentuk molekul. |
| Berat | Lebih berat dari atom tertentu. | Sangat Ringan (Berat relatif adalah 1 AMU) |
Apa itu Elemen?
Unsur adalah konsep dasar yang harus diketahui untuk memahami kimia tingkat lanjut. Dalam inti atomnya, suatu unsur hanya terdiri dari atom-atom yang mengandung jumlah proton yang sama.
Unsur kimia tidak dapat dibagi menjadi unsur atau zat yang lebih sederhana menggunakan metode kimia apa pun. Yang terakhir dikaitkan dengan nomor atom, diwakili oleh simbol 'Z.'
Kimia modern sangat bergantung pada tabel periode. Semua unsur yang ditemukan dikategorikan dan diatur secara sistematis dalam tabel periodik. Konsep ini dikembangkan oleh Rusia kimiawan Dmitri Mendeleev pada tahun 1869.
Karakteristik suatu unsur bertanggung jawab atas keadaan fisiknya pada suhu kamar atau rata-rata. Itu bisa dalam bentuk gas atau padat atau cair.
Ada sekitar 118 jenis elemen secara total.
Beberapa contoh elemen adalah sebagai berikut:
- Hidrogen
- Karbon
- Neon
- Magnesium
- Aluminium
- Boron
Apa itu Atom?
Atom adalah unit terkecil dari materi biasa. Mereka kecil, dengan perkiraan ukuran 100 pikometer. Juga, sebuah atom berbobot sangat ringan. Relatif bobot yang terakhir relatif 1AMU.
Inti terdiri dari satu atau lebih proton dan beberapa neutron. Hanya ada satu pengecualian untuk aturan ini: Hidrogen, yang tidak memiliki neutron. Inti menyumbang 99.94% dari massa atom.
Proton memiliki muatan listrik positif, elektron mengandung jumlah listrik negatif, dan neutron tidak memiliki kontrol listrik. Sebuah atom netral secara listrik ketika jumlah proton dan elektronnya sama.
Ada 92 jenis atom di alam.
Konsep utama dan gagasan materi itu terdiri dari partikel-partikel kecil yang tak terpisahkan adalah kuno. Sejarah atom kembali ke zaman kuno India dan Yunani.

Perbedaan Utama Antara Unsur dan Atom
- Ketika lebih dari satu unsur bergabung, mereka membentuk reaksi kimia baru yang menghasilkan unsur baru. Ketika lebih dari satu atom bergabung (menjaga berbagai hal konstan), mereka membentuk sebuah molekul.
- Berat unsur lebih berat jika dibandingkan dengan berat atom, sedangkan dalam kasus atom, yang terakhir sangat ringan. Bobot relatif yang terakhir kira-kira 1 AMU.
- https://books.google.com/books?hl=en&lr=&id=EvTI-ouH3SsC&oi=fnd&pg=PP1&dq=elements&ots=pQ5TOAfsJ3&sig=LBL5oWU1-cH9p_y8JPtdmdjok7g
- https://pubs.acs.org/doi/pdf/10.1021/ar00109a003
Terakhir Diperbarui : 11 Juni 2023

Piyush Yadav telah menghabiskan 25 tahun terakhir bekerja sebagai fisikawan di masyarakat setempat. Dia adalah fisikawan yang bersemangat membuat sains lebih mudah diakses oleh pembaca kami. Dia memegang gelar BSc dalam Ilmu Pengetahuan Alam dan Diploma Pasca Sarjana dalam Ilmu Lingkungan. Anda dapat membaca lebih lanjut tentang dia di nya halaman bio.

Penjelasan mendalam membuatnya lebih mudah untuk memahami perbedaan antara unsur dan atom, sehingga menambah nilai pendidikan yang sangat besar.
Perbandingan detail unsur dan atom telah terbukti menjadi aset pendidikan.
Perbandingan unsur dan atom yang jelas dan mendetail mempermudah pemahaman perbedaannya, sehingga berfungsi sebagai alat pembelajaran yang hebat.
Mempelajari perbedaan antara unsur dan atom dari artikel ini cukup mendalam dan mendidik.
Konten informatif tentang unsur dan atom membuat perbandingan kedua konsep tersebut cukup jelas dan mudah dipahami.
Artikel ini telah memberikan perbandingan rinci yang komprehensif dan informatif antara unsur dan atom, serta memberikan wawasan yang sangat berharga mengenai karakteristik dan perilaku masing-masing unsur.
Saya terkesan dengan perbandingan jelas perbedaan antara unsur dan atom yang disajikan dalam artikel ini.
Artikel ini memiliki nilai pendidikan yang tinggi, terutama bagi mereka yang memiliki minat terhadap sains dan kimia.
Ini jelas merupakan sumber berharga bagi siapa pun yang tertarik mempelajari unsur dan atom.
Ini telah terbukti bermanfaat dalam memahami konsep ilmiah dasar tentang unsur dan atom.
Perbandingan komprehensif unsur dan atom telah memberikan pencerahan, menawarkan pemahaman yang lebih baik tentang konsep-konsep ilmiah ini.
Mendalami perbandingan unsur dan atom telah memberikan pengalaman pendidikan yang berharga, sehingga memudahkan pemahaman konsep-konsep ilmiah tersebut.
Artikel ini berhasil memberikan perbandingan yang mendalam dan komprehensif antara unsur dan atom, sehingga sangat bermanfaat untuk tujuan pendidikan dan pemahaman konsep ilmiah.
Nilai edukasi perbandingan unsur dan atom dalam artikel ini sungguh terpuji.
Detail komprehensif tentang intisari unsur vs atom sangat membantu untuk pemahaman yang lebih baik tentang konsep-konsep ini.