มีความแตกต่างที่สำคัญมากมายระหว่างพันธะโควาเลนต์และไฮโดรคาร์บอน เคมี การศึกษาเกี่ยวกับสาร – องค์ประกอบและสารประกอบ เริ่มต้นด้วยพื้นฐานของพันธะระหว่างอะตอมและโมเลกุลสองอะตอม
บทความนี้จะอธิบายความแตกต่างระหว่างพันธะไฮโดรเจนและโควาเลนต์และวิธีการก่อตัว เราจะดูพันธะเคมีทั้งสองประเภท ประเภทปฏิสัมพันธ์ทำให้โมเลกุลโควาเลนต์แตกต่างจากโมเลกุลไฮโดรคาร์บอน
ประเด็นที่สำคัญ
- พันธะไฮโดรเจนก่อตัวขึ้นระหว่างโมเลกุลเมื่ออะตอมไฮโดรเจนเกิดพันธะกับอะตอมที่มีอิเล็กโทรเนกาติตีสูง พันธะโควาเลนต์แบ่งอิเล็กตรอนระหว่างอะตอมภายในโมเลกุล
- พันธะไฮโดรเจนอ่อนกว่าพันธะโควาเลนต์ โดยให้ปฏิกิริยาชั่วคราวและผันกลับได้
- พันธะไฮโดรเจนมีส่วนช่วยในโครงสร้างและหน้าที่ของโมเลกุลทางชีววิทยา พันธะโควาเลนต์เป็นพื้นฐานของโครงสร้างโมเลกุล
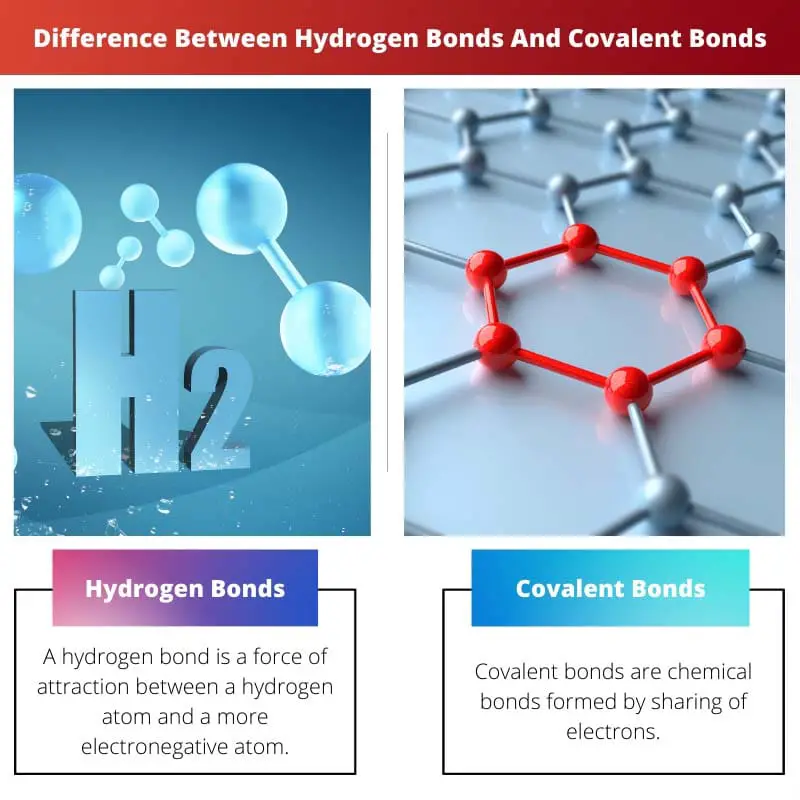
พันธะไฮโดรเจนกับพันธะโควาเลนต์
พันธะไฮโดรเจนเกิดขึ้นเมื่ออะตอมไฮโดรเจนที่มีประจุบวกทำปฏิกิริยากับอะตอมที่มีประจุไฟฟ้า ทำให้เกิดพันธะที่ค่อนข้างอ่อนกว่าพันธะโควาเลนต์ที่เกี่ยวข้องกับการแบ่งปันอิเล็กตรอน พันธะเหล่านี้จำเป็นต่อคุณสมบัติเฉพาะตัวของน้ำ พันธะโควาเลนต์เป็นรากฐานของโมเลกุลส่วนใหญ่

พันธะไฮโดรเจนสามารถเป็นได้ทั้งภายในโมเลกุลหรือระหว่างโมเลกุล พลังงานที่เกี่ยวข้องกับพันธะไฮโดรเจนจะแตกต่างกันไปขึ้นอยู่กับรูปทรงและสภาพแวดล้อมของอะตอม
มันเป็นพันธะที่อ่อนแอกว่าปฏิสัมพันธ์ของ van der Waals ซึ่งเกิดขึ้นในโมเลกุลอินทรีย์และอนินทรีย์ ตัวอย่างพันธะไฮโดรเจนบางส่วน ได้แก่ กรดซาลิไซลิก H2O (น้ำ) เมทิลแอลกอฮอล์ น้ำตาล ฯลฯ
พันธะโควาเลนต์เป็นรูปแบบหนึ่งของแรงระหว่างโมเลกุล พวกมันถูกสร้างขึ้นเมื่ออะตอมตั้งแต่สองอะตอมขึ้นไปใช้อิเล็กตรอนร่วมกันเพื่อเติมเต็มเปลือกอิเล็กตรอนชั้นนอกสุด พันธะโควาเลนต์มีความแข็งแรงกว่าพันธะไฮโดรเจนมากและมีเสถียรภาพสูง
ตารางเปรียบเทียบ
| พารามิเตอร์ของการเปรียบเทียบ | พันธะไฮโดรเจน | พันธะโควาเลนต์ |
|---|---|---|
| พวกเขาคืออะไร? | พันธะไฮโดรเจนเป็นแรงดึงดูดระหว่างอะตอมของไฮโดรเจนกับอะตอมที่มีประจุไฟฟ้าลบมากกว่า | พันธะโควาเลนต์เป็นพันธะเคมีที่เกิดจากการใช้อิเล็กตรอนร่วมกัน |
| กองกำลัง | แรงระหว่างโมเลกุลและแรงภายในโมเลกุล | แรงระหว่างโมเลกุล |
| ความแข็งแรง | มันถูกสร้างขึ้นระหว่างสองอะตอม | พันธะโควาเลนต์นั้นแข็งแกร่งกว่าพันธะไฮโดรเจนมาก |
| ก่อตัวขึ้นระหว่าง | พันธะไฮโดรเจนเกิดขึ้นระหว่างสองอะตอมของสองโมเลกุลที่แตกต่างกัน | เกิดขึ้นระหว่างสองอะตอม |
| ตัวอย่าง | กรดซาลิไซลิก น้ำ กลูโคส ฯลฯ | มีเทน คาร์บอนมอนอกไซด์ เป็นต้น |
พันธะไฮโดรเจนคืออะไร?
พันธะไฮโดรเจนคือแรงดึงดูดทางไฟฟ้าระหว่างสองอะตอม มันถูกสร้างขึ้นเมื่ออะตอมไฮโดรเจนเกิดพันธะโควาเลนต์กับบิตที่มีอิเล็กโตรเนกาติวิตีมากกว่าอีกบิตหนึ่ง เช่น ออคเต็ตหรือหมู่
ส่วนใหญ่แล้ว โมเลกุลที่มีประจุไฟฟ้าลบจะเป็นทั้งออกซิเจน ไนโตรเจน หรือฟลูออรีน ในกรณีส่วนใหญ่ อะตอมที่มีอิเล็กโทรเนกาติตีมากกว่าที่มีอิเล็กตรอนคู่เดียวเรียกว่าตัวรับ
พันธะไฮโดรเจนเป็นแรงดึงดูดที่แข็งแกร่งระหว่างอะตอมที่มีประจุบวกบางส่วนและมีประจุบวก เป็นพันธบัตรที่แข็งแกร่งที่สุดในบรรดาพันธบัตรทุกประเภทที่รู้จัก ความผูกพันเหล่านี้พบได้ในหลายๆ แห่ง สารประกอบโควาเลนต์ แต่อ่อนแอกว่าโควาเลนต์
ธรรมชาติของอิเลคโตรเนกาติตีของอะตอมไฮโดรเจนจะเชื่อมโมเลกุลทั้งสองเข้าด้วยกัน น้ำจึงสามารถเคลื่อนที่ระหว่างอนุภาคและสร้างสารประกอบเคมีที่เสถียรได้ เช่น เมื่อกระดาษเปียกติดกัน
พันธะไฮโดรเจนเกิดขึ้นระหว่างสองโมเลกุลที่มีไฮโดรเจนชนิดเดียวกัน
พันธะ CH เกิดขึ้นเมื่อคาร์บอน 2 อะตอมกลายเป็น อิเล็ก ผูกพัน.
ในพันธะผู้ให้/ตัวรับ ผู้ให้โปรตอนคืออะตอมของอิเลคโตรเนกาติวิตี้ และผู้รับโปรตอนคืออะตอมที่ไม่มีพันธะโควาเลนต์กับไฮโดรเจน อะตอมไฮโดรเจนในคู่เบสถูกยึดเข้าด้วยกันโดยพันธะไฮโดรเจน
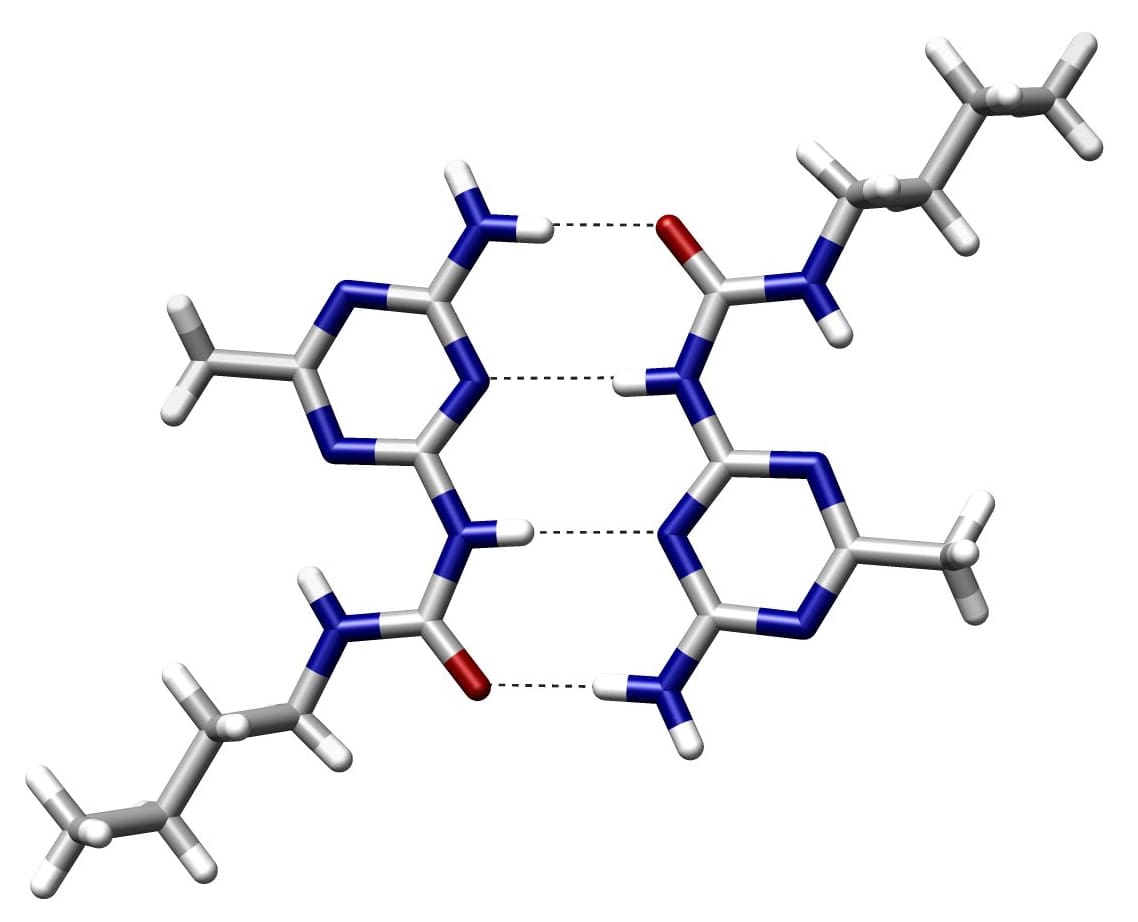
พันธะโควาเลนต์คืออะไร?
อะตอม XNUMX อะตอมใช้คู่อิเล็กตรอนร่วมกันเพื่อสร้างพันธะโควาเลนต์ คู่อิเล็กตรอนเหล่านี้เรียกว่าคู่พันธะ พันธะโควาเลนต์ถูกสร้างขึ้นจากความสมดุลระหว่างแรงดึงดูดและแรงผลัก
นี่คือตัวอย่างบางส่วน. เพื่อแสดงให้เห็น นี่คือสมการทางเคมี อ่านต่อเพื่อค้นพบวิทยาศาสตร์ที่อยู่เบื้องหลังพวกเขา ตัวอย่างที่ง่ายที่สุดของพันธะโควาเลนต์คือการใช้อิเล็กตรอนคู่ร่วมกัน
กระบวนการพันธะเกี่ยวข้องกับการแบ่งปันอิเล็กตรอนระหว่างอะตอมสองอะตอมที่ต่างกัน เนื่องจากอิเล็กตรอนแบ่งปันพลังงาน จึงสามารถมีพลังงานต่ำกว่าอะตอมอื่นๆ พวกเขาพัวพันเมื่อศูนย์กลางดึงดูดกัน
“อิเล็กตรอนที่ใช้ร่วมกันจะลดพลังงานของอะตอมอื่นลง สิ่งนี้เรียกว่า "สมดุล" ปรากฏการณ์นี้เป็นเรื่องปกติและสามารถใช้เพื่อติดตามความคืบหน้าและระบุบทเรียนที่สำคัญได้” อิเล็กตรอนที่ใช้ร่วมกันลดพลังงานของอะตอมอื่น สิ่งนี้เรียกว่า "สมดุล" ปรากฏการณ์นี้เป็นเรื่องปกติและสามารถใช้เพื่อติดตามความคืบหน้าและระบุบทเรียนที่สำคัญได้
กระบวนการแบ่งปันอิเล็กตรอนส่งผลให้พลังงานลดลง อิเล็กตรอนที่ใช้อะตอมร่วมกับอิเล็กตรอนตัวอื่นจะสูญเสียพลังงาน อยู่ในสถานะนี้ที่พันธะโควาเลนต์ก่อตัวขึ้น
อิเล็กตรอนระหว่างจุดดึงดูดสองแห่งมีพลังงานต่ำกว่าอิเล็กตรอนระหว่างจุดเป็นกลางสองแห่ง พลังของอะตอมเดี่ยวจะเพิ่มขึ้นในโมเลกุลหากใช้ร่วมกันในระดับพลังงานที่สูงกว่า
ความแตกต่างหลักระหว่างพันธะไฮโดรเจนกับพันธะโควาเลนต์
- พันธะไฮโดรเจนแข็งแรงกว่าพันธะโควาเลนต์เพียง 1/10 เท่า
- พันธะไฮโดรเจนเป็นพันธะระหว่างโมเลกุลและระหว่างโมเลกุล ในทางกลับกัน พันธะโคเวเลนต์คือพันธะเคมีระหว่างโมเลกุล
- พันธะไฮโดรเจนเกิดขึ้นระหว่างสองอะตอมของสองโมเลกุลที่แตกต่างกัน พันธะโควาเลนต์เกิดขึ้นระหว่างสองอะตอม
- พันธะไฮโดรเจนเป็นแรงดึงดูด พันธะโควาเลนต์เป็นพันธะเคมี
- พันธะไฮโดรเจนมีความเสถียรต่ำเมื่อเทียบกับพันธะโควาเลนต์
- https://scripts.iucr.org/cgi-bin/paper?a12816
- https://pubs.acs.org/doi/pdf/10.1021/ja01130a013
- https://aip.scitation.org/doi/abs/10.1063/1.3159673
อัพเดตล่าสุด : 29 มิถุนายน 2023

Piyush Yadav ใช้เวลา 25 ปีที่ผ่านมาทำงานเป็นนักฟิสิกส์ในชุมชนท้องถิ่น เขาเป็นนักฟิสิกส์ที่มีความหลงใหลในการทำให้ผู้อ่านของเราเข้าถึงวิทยาศาสตร์ได้มากขึ้น เขาสำเร็จการศึกษาระดับปริญญาตรีสาขาวิทยาศาสตร์ธรรมชาติและประกาศนียบัตรบัณฑิตสาขาวิทยาศาสตร์สิ่งแวดล้อม คุณสามารถอ่านเพิ่มเติมเกี่ยวกับเขาได้จากเขา หน้าไบโอ.


คำอธิบายทางวิทยาศาสตร์มีความชัดเจนและแม่นยำ สิ่งนี้ช่วยให้ฉันเข้าใจแนวคิดนี้ได้ดีขึ้น
อธิบายการเปรียบเทียบพันธะไฮโดรเจนและโควาเลนต์ได้ดี บทความดีๆ!
ใช่ ฉันเห็นด้วยอย่างยิ่ง เป็นประโยชน์สำหรับนักศึกษาและผู้สนใจวิชาเคมี
บทความนี้นำเสนอการวิเคราะห์เชิงลึกเกี่ยวกับความแตกต่างระหว่างพันธะไฮโดรเจนและโควาเลนต์
ผู้เขียนทำหน้าที่ได้อย่างยอดเยี่ยมในการอธิบายแนวคิดพร้อมตัวอย่างที่เกี่ยวข้อง เป็นเรื่องที่น่ายกย่อง
การอ่านบทความนี้มีคุณค่าอย่างแท้จริง ฉันได้รับข้อมูลเชิงลึกและความรู้อันมีค่าจากการเปรียบเทียบที่ให้ไว้ที่นี่
ฉันคาดหวังว่าจะมีหลักฐานทางวิทยาศาสตร์อีกเล็กน้อยเพื่อสนับสนุนบางประเด็นที่กล่าวถึง ดี แต่ไม่ดี