Хвороба Альцгеймера є прогресуючим нейродегенеративним захворюванням. Це одна з основних причин старечої деменції. Основний механізм захворювання все ще неясний і підлягає подальшим науковим дослідженням, але дві найпопулярніші гіпотези в розумінні хвороби Альцгеймера – це амілоїдна та тау-гіпотеза.
Ключові винесення
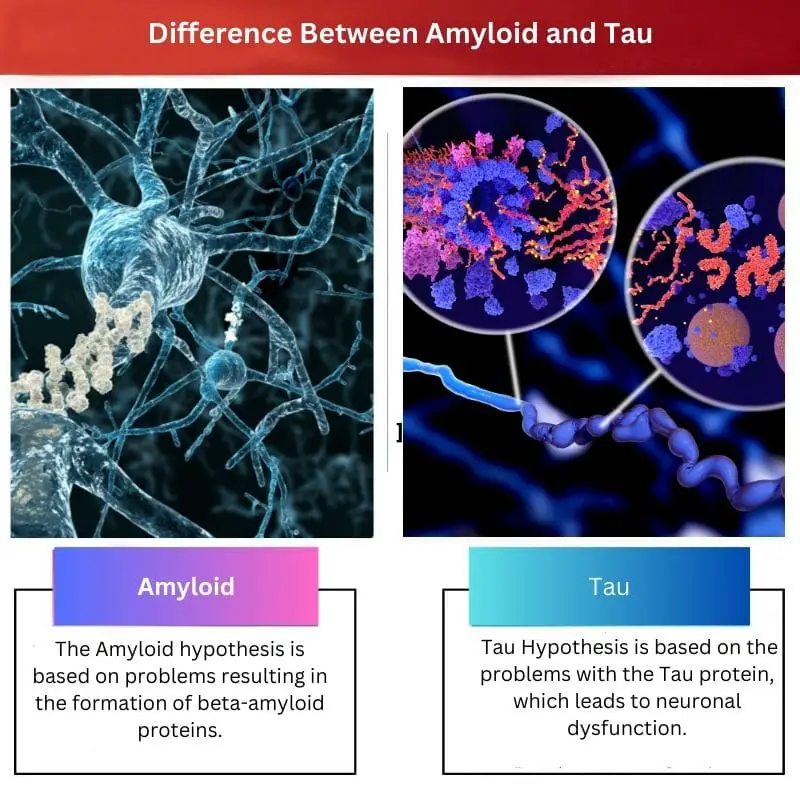
- Амілоїд відноситься до білкових відкладень, які утворюють бляшки в мозку, тоді як тау-білки утворюють нейрофібрилярні клубки в клітинах мозку.
- І амілоїд, і тау пов'язані з хворобою Альцгеймера, але вони відіграють різні ролі в її прогресуванні.
- Сучасні методи лікування хвороби Альцгеймера націлені на амілоїд, але останні дослідження показують, що націлювання на тау може бути більш ефективним для уповільнення когнітивного зниження.
Амілоїд проти тау
І амілоїд, і тау є аномальними білковими відкладеннями, які виявляються в мозку при хворобі Альцгеймера. Це нерозчинні білки, які складаються з компактних волокон. Амілоїд відкладається поза клітинами головного мозку, а тау знаходиться всередині нейронних клітин. Амілоїд утворює бляшки, тоді як тау утворює клубки.
Таблиця порівняння
| Параметри порівняння | Амілоїд | Тау |
|---|---|---|
| Тип білка | Бета-амілоїдний білок | Тау білок |
| Уражена ділянка мозку | З’єднання клітин головного мозку | Електричні та хімічні сигнали клітин мозку |
| Симптоми | Втрата пам'яті | Втрата пам'яті, зміни в поведінці |
| Причинний фактор | Заміна активності альфа-секретази на бета-секретазу. | Гіперфосфорилювання білка тау |
| Характеристики Hallmark | Амілоїдні бляшки | Нейрофібрилярні клубки |
Що таке амілоїд?
Гіпотеза про амілоїд є однією з найбільш досліджених гіпотез у спробах знайти лікування для лікування хвороби Альцгеймера. Зазвичай білок-попередник амілоїду розщеплюється під дією альфа- та гамма-секретази, утворюючи нешкідливі розчинні пептиди.
Однак мутації в генах, що кодують білок-попередник амілоїду та пресенілін, який є компонентом гамма-секретази, пов’язані з підвищеною схильністю до утворення довших амілоїдних фрагментів, які агрегують разом, утворюючи фібрили та олігомери.
Ці фібрили та олігомери є нейротоксичними і, отже, відповідальними за смерть нейронів. Ці олігомери також запускають каскад подій, які ще більше руйнують нейронні клітини. Одним із шляхів є активація кінази, яка викликає можливе гіперфосфорилювання білка тау та призводить до подальшого руйнування нейронів.
Амілоїдна гіпотеза ще більше посилюється її зв'язком із раннім початком хвороби Альцгеймера у людей із синдромом Дауна. Оскільки ген білка-попередника амілоїду розташований на 21 хромосомі, додаткова копія 21st хромосом у людей із синдромом Дауна доведено, що будь-які проблеми з числом хромосом або їх мутаціями є сильним причинним фактором хвороби Альцгеймера.
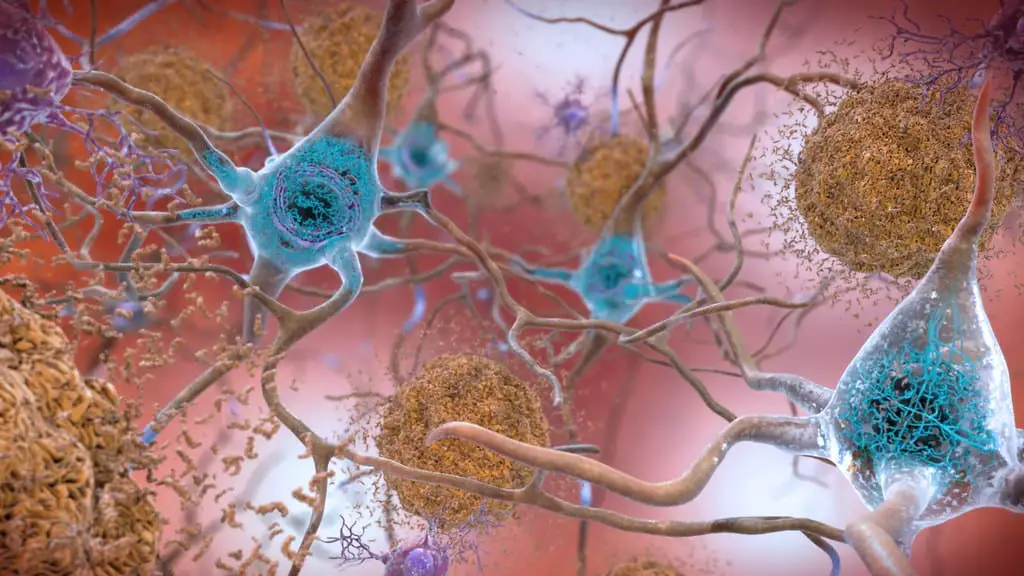
Що таке Тау?
З іншого боку, гіпотеза Тау була досліджена порівняно недавно як основна причина хвороби Альцгеймера після того, як випробування з боротьби з утворенням бета-амілоїдних білків не дали обнадійливих результатів.
Крім того, нейрофібрилярні клубки внаслідок агрегації тау-білків можна побачити у пацієнтів слабоумство але без бета-амілоїдної патології. Крім того, амілоїдні бляшки можна побачити у людей без нейродегенеративних дефектів, однак цього не можна сказати про тих, хто має нейрофібрилярні клубки, оскільки патологія тау-білка тісно корелює з тяжкістю та прогресуванням хвороби Альцгеймера.
Гіпотеза Тау також стверджує, що патологія Тау передує будь-якій бета-амілоїдній патології та є основною причиною хвороби Альцгеймера. Тау-білок відповідає за стабільність мікротрубочок, що забезпечує транспортування поживних речовин всередині нейронних клітин і цілісність загальної структури клітини.
Зміна тау-білка шляхом гіперфосфорилювання призводить до агрегацій тау-білка в клубки, що руйнує мікротрубочки та порушує постачання поживними речовинами та структуру клітини, що призводить до загибелі нейронів. Ці клубки можуть далі рухатися по аксонах і порушувати роботу інших нейронних клітин, що призводить до функціональної втрати частин нервової системи, викликаючи хворобу Альцгеймера.
The clinical trials targeting Tau proteins have not yet shown desirable results however, the hypothesis is fairly recently studied, so not enough clinical data is available as of yet.
Основні відмінності між амілоїдом і тау
- Амілоїдна гіпотеза базується на проблемах, що призводять до утворення бета-амілоїдних білків, що розглядається як тригерна точка в каскаді подій, що призводять до хвороби Альцгеймера, тоді як гіпотеза Тау базується на проблемах з білком Тау, який призводить до дисфункції нейронів.
- Гіпотеза про амілоїд базується на його сильному зв’язку з проблемами з хромосомою 21, оскільки будь-яка мутація або додаткова копія хромосоми призведе до раннього розвитку хвороби Альцгеймера, тоді як гіпотеза Тау припускає тісний зв’язок нейрофібрилярних клубків із тяжкістю та прогресування захворювання.
- Довгий час гіпотеза про амілоїд вважалася основною причиною, яка може спровокувати події, що викликають хворобу Альцгеймера, і тому її досліджували довше порівняно з гіпотезою Тау, яка лише нещодавно розглядалася як основна причина, а не наступний результат амілоїдна гіпотеза.
- Вважається, що бета-амілоїдна патологія викликає деменцію у пацієнтів; однак патологія Тау, крім деменції, також показала свій вплив на поведінкові зміни у пацієнтів, які страждають на хворобу Альцгеймера.
- Бета-амілоїдні фібрили видно позаклітинно у формі бляшок, які відкладаються в різних областях мозку, тоді як клубки тау присутні внутрішньоклітинні у формі нейрофібрилярних клубків.
- https://movementdisorders.onlinelibrary.wiley.com/doi/epdf/10.1002/mds.22594
- https://reader.elsevier.com/reader/sd/pii/S0002944017300809?token=8632CB1A71421C8D29E8BCF80F18C7897E9B686E1DAB508B6203782D87488A0C6ACAC8608FEA76A420108571CA668350&originRegion=eu-west-1&originCreation=20221101051336
Останнє оновлення: 27 липня 2023 р

Піюш Ядав провів останні 25 років, працюючи фізиком у місцевій громаді. Він фізик, який прагне зробити науку доступнішою для наших читачів. Він має ступінь бакалавра природничих наук і диплом аспіранта з екології. Ви можете прочитати більше про нього на його біо сторінка.

