يتم وصف نوعين من ردود الفعل بكلمات Endergonic و exergonic. تحدث العديد من التفاعلات الكيميائية والبيولوجية باستمرار داخل وخارج جسم الإنسان.
تستخدم هذه المقالة جدولًا وصفيًا للتمييز بين الفروق الأساسية والمتقدمة بين التفاعلين لسهولة التعلم والفهم من قبل المبتدئين والمتحمسين للمواد الكيميائية.
الوجبات السريعة الرئيسية
- تطلق التفاعلات المفرطة الطاقة ، بينما تمتص التفاعلات العصبية الطاقة من محيطها.
- تفاعلات الطاقة المفرطة لها تغير سلبي في طاقة جيبس الحرة ، في حين أن تفاعلات الطاقة المفرطة يكون لها تأثير إيجابي.
- تكون تفاعلات Endergonic غير عفوية ، في حين أن تفاعلات exergonic تكون عفوية في ظل ظروف معينة.
التفاعلات الخارجية مقابل ردود الفعل Endergonic
طارد للطاقة التفاعلات هي تفاعلات كيميائية يكون فيها التغير في الطاقة الحرة سالباً، أو يكون هناك إطلاق صافي للطاقة الحرة ويشير إلى تفاعل تلقائي. التفاعلات الداخلية هي تفاعلات يكون فيها التغير المعياري في الطاقة الحرة إيجابيًا، ويلزم وجود قوة دافعة للقيام بذلك.

يُعرف التفاعل الذي يولد طاقة حرة باسم تفاعل "طارد للطاقة". نظرًا لأن هذا التفاعل ينتج طاقة بدلاً من استهلاكها ، فقد يحدث من تلقاء نفسه ، دون تدخل قوى أخرى.
التفاعلات الخارجية في الكيمياء الحيوية ، وكذلك الكيمياء الحرارية ، هي تلك التي يكون فيها التغيير في الطاقة الحرة سالبًا (ناقص القيمة العددية).
هذه ليست ردود أفعال لا إرادية غير تلقائية. للبدء ، يحتاجون إلى مجهود أو إدخال قوة - بشكل أساسي في شكل طاقة.
يتمثل الدور الشائع للتفاعل المندفع للطاقة في تحرير الطاقة من جزيئات الكربوهيدرات أو أي جزيء غذائي مفترض ، مما يسمح للمخلوقات بالازدهار دون الاعتماد فقط على ضوء الشمس للحصول على الطاقة.
جدول المقارنة
| معلمات المقارنة | التفاعلات الخارجية | ردود الفعل Endergonic |
|---|---|---|
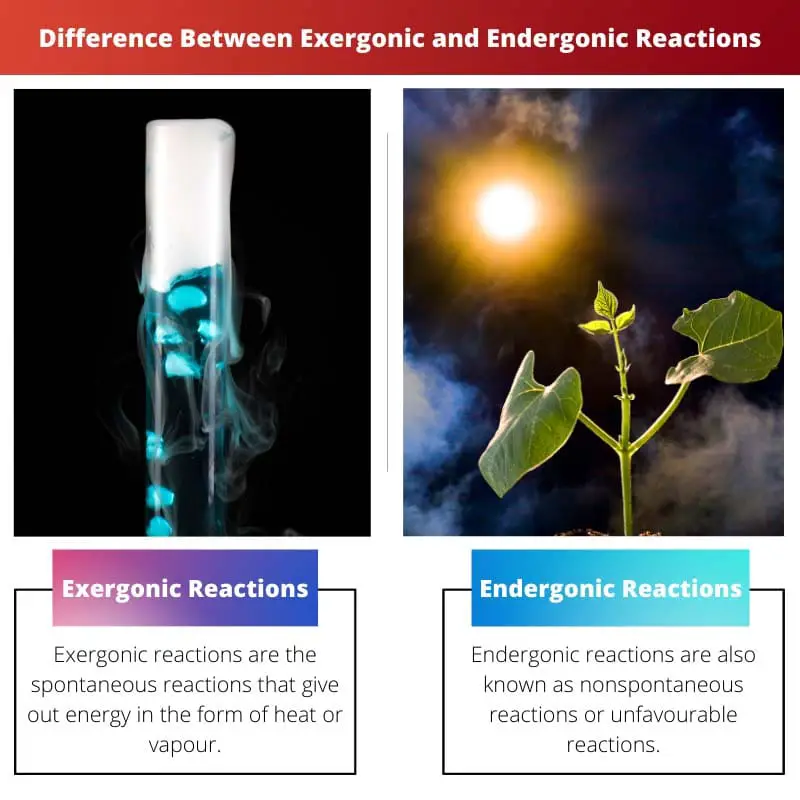
| تعريف | التفاعلات المفرطة هي التفاعلات العفوية التي تعطي طاقة في شكل حرارة أو بخار. | تُعرف تفاعلات Endergonic أيضًا باسم ردود الفعل غير التلقائية أو التفاعلات غير المواتية. يتطلب التفاعل طاقة أكثر مما تتلقاه |
| جيبس الطاقة الحرة | قيمة طاقة جيبس الحرة سالبة. | قيمة طاقة جيبس الحرة إيجابية. |
| مستوى الانتروبيا | يتم زيادة مستوى الانتروبيا في تفاعل نموذجي للطاقة. | يتم تقليل الانتروبيا في تفاعل مائي. |
| متطلبات الطاقة | يعطي الطاقة على شكل حرارة. | يستهلك الطاقة عبر المحيط لبدء التفاعل أو استمراره. |
| أمثلة | تفاعل الصوديوم والكلور لتكوين ملح الطعام والاحتراق والتألق الكيميائي. في هذا التفاعل يتم إطلاق الطاقة على شكل ضوء. | يعد التفاعل الكيميائي لعملية التمثيل الضوئي مثالًا جيدًا على التفاعلات الذاتية للطاقة. |
ما هي التفاعلات الخارجية؟
هي تفاعلات لا رجعة فيها تحدث بشكل طبيعي في البيئة. يشير مصطلح "عفوي" إلى شيء جاهز أو حريص على الحدوث مع القليل من التحفيز الخارجي أو بدونه.
عندما يتعرض الصوديوم للأكسجين في الغلاف الجوي ، على سبيل المثال ، سوف يحترق. مثال آخر على ردود الفعل المفرطة هو تدخين الخشب.
تحت درجة الحرارة والضغط القياسيين ، تكون طاقة جيبس الحرة صفرًا ، مما يشير إلى أنه يتم امتصاص حرارة أكثر من امتصاصها. هذه ردود لا يمكن عكسها.
تستخدم الكائنات الحية عمليات طاردة للطاقة لنقل الطاقة من "التخزين" في مكون واحد ، مثل الدهون أو السكر ، إلى حالة نشطة ، مثل ATP.
ما هي تفاعلات Endergonic؟
تُعرف العملية التي يتم فيها امتصاص الحرارة أو أي شكل من أشكال الطاقة باسم تفاعل الطاقة. هذا يعني أن التغيير الإجمالي في الطاقة الحرة إيجابي من الناحية الكيميائية.
لا يمكن أن تحدث العديد من العمليات في الطبيعة إلا إذا توفرت الطاقة الكافية من البيئة.
مساعدات الطاقة الخارجية في انحلال من هذه الروابط. الطاقة المنبعثة نتيجة لانكسار الرابطة تغذي التفاعل.
في حالة التفاعلات endergonic ، تكون طاقة جيبس الحرة موجبة (+) ، مما يشير إلى أن التفاعل ليس تلقائيًا.
الاختلافات الرئيسية بين تفاعلات Exergonic و Endergonic
- في تفاعلات طاردة للطاقة، تزداد الإنتروبيا، بينما في تفاعلات طاردة للطاقة، تقل الإنتروبيا.
- تكون طاقة منتجات التفاعل المولد للطاقة أكبر من طاقة المواد المتفاعلة، في حين أن طاقة المنتجات أقل من المواد المتفاعلة في حالة التفاعلات المولدة للطاقة.
- https://www.khanacademy.org/science/biology/energy-and-enzymes/free-energy-tutorial/a/gibbs-free-energy
- https://bio.libretexts.org/Bookshelves/Introductory_and_General_Biology/Book%3A_General_Biology_(Boundless)/6%3A_Metabolism/6.2%3A_Potential_Kinetic_Free_and_Activation_Energy/6.2A%3A__Free_Energy
آخر تحديث: 07 سبتمبر 2023

أمضى بيوش ياداف السنوات الخمس والعشرين الماضية في العمل كفيزيائي في المجتمع المحلي. إنه فيزيائي شغوف بجعل العلم في متناول قرائنا. وهو حاصل على بكالوريوس في العلوم الطبيعية ودبلوم دراسات عليا في علوم البيئة. يمكنك قراءة المزيد عنه على موقعه صفحة بيو.


تقدم هذه المقالة تحليلاً شاملاً للتفاعلات المولدة للطاقة والتفاعلات المولدة للطاقة، مع تسليط الضوء على أهميتها في التفاعلات الكيميائية والبيولوجية.
توفر هذه المقالة شرحًا ثاقبًا وشاملاً لتفاعلات الطاقة والطاقة. يعد جدول المقارنة والأمثلة مفيدًا بشكل خاص في فهم الاختلافات الرئيسية.
المقالة غنية بالمعلومات ومنظمة بشكل جيد. إن التمييز الواضح بين ردود الفعل المولدة للطاقة والتفاعلات المولدة للطاقة يجعل من السهل على القراء فهم المفاهيم.
إن توضيح المقال للتفاعلات المولدة للطاقة والتفاعلات المولدة للطاقة أمر يستحق الثناء، حيث يقدم فهمًا متقنًا للقراء حول العمليات الكيميائية والبيولوجية التي يحكمونها.
يشرح المقال ببراعة الانقسام بين ردود الفعل المولدة للطاقة والتفاعلات المولدة للطاقة، موضحًا آثارها في مختلف الظواهر الطبيعية.
إن شرح المقالة لتفاعلات الطاقة والتفاعلات المولدة للطاقة واضح جدًا وتثقيفي. تعتبر الأمثلة الواقعية المقدمة بمثابة رسوم توضيحية عملية، مما يساهم في فهم المفهوم بشكل أفضل.
إن المقارنة الشاملة بين ردود الفعل المولدة للطاقة والتفاعلات المولدة للطاقة جديرة بالثناء، مما يوضح التباينات الأساسية بدقة ووضوح.
يسلط جدول المقارنة التفصيلي الضوء بشكل فعال على التباينات الأساسية بين ردود الفعل المولدة للطاقة والتفاعلات المولدة للطاقة، مما يلبي احتياجات القراء ذوي مستويات مختلفة من الخبرة. استخدام الأمثلة الوصفية يعزز الفهم.