Periodická tabulka chemie je něco, co se po studentech vyžaduje, aby se zdlouhavě učili nazpaměť, aniž by vůbec znali skutečný motiv, který se ji naučil. Pro některé lidi je to jen téma zahrnuté v osnovách.
Ale ve skutečném smyslu je tato malá periodická tabulka mnohem důležitější než to; je to plán, který odemyká milion příležitostí pro vědce a výzkumníky po celém světě. Dmitrij Mendělejev je vynálezcem periodické tabulky.
Před ním se mnozí usilovně snažili uspořádat chemické prvky různými způsoby. Ale Dmitriho výsledek byl celosvětově přijat.
Ve vědeckých zkratkách se řádky označují jako období a sloupce jako skupiny.
Key Takeaways
- Periody jsou vodorovné řádky v periodické tabulce, které udávají počet elektronových obalů v atomech prvku, přičemž prvky ve stejném období mají podobnou atomovou strukturu.
- Skupiny jsou svislé sloupce v periodické tabulce, skládající se z prvků se stejným počtem elektronů ve vnějším obalu, což vede k podobným chemickým vlastnostem.
- Periody i skupiny organizují prvky v periodické tabulce, přičemž periody představují vodorovné řady založené na elektronových obalech a skupiny představující svislé sloupce na základě elektronů vnějšího obalu a chemických vlastností.
Období vs. skupina
Tečka je vodorovná řada, která jde z levé strany na pravou stranu periodické tabulky a elektronegativita se napříč ní zvyšuje. Skupina je vertikála sloupec která jde od vrcholu periodické tabulky dolů a elektronegativita se zvyšuje zdola nahoru.

Mendělejev během zařizování nechal pár řádků prázdných s dojmem, že v blízké budoucnosti vstoupí nějaké další prvky. A překvapivě jeden z prvků, který se do té mezery vešel, byl Gallium.
Srovnávací tabulka
| Parametr srovnání | Období | Skupina |
|---|---|---|
| Vedení | Periody jsou vodorovné řádky v moderní periodické tabulce | Skupiny jsou svislé sloupce, které procházejí horní částí periodické tabulky |
| Nemovitosti | Prvky v období nemají podobné vlastnosti. | Prvky v každé skupině mají některé podobné vlastnosti, ale ne identické vlastnosti. |
| Podobnost | Prvky ve stejném období mají stejný počet elektronového složení | Prvky v každé skupině mají stejný počet valenčních elektronů |
| Součet | V periodické tabulce je 7 period | Skupina obsahuje 18 prvků uspořádaných vertikálně v moderní periodické tabulce. |
| Elektronegativita | Zvyšuje se zleva doprava. | Ve skupině se zvyšuje zdola nahoru. |
Co je období?
Tečka je vodorovný řádek v periodické tabulce od krajní levé až po krajní pravou stranu. V současné době je v periodické tabulce 7 období.
Nové období začíná, když se s elektrony sčítá nová základní energetická hladina. Každý prvek v období bude mít pravděpodobně stejný počet atomových orbitalů.
Například – každý prvek v 1st období má pouze 1 orbitální pro jeho elektrony, 2nd perioda zahrnuje 2 orbitaly pro elektrony. Podobně se orbitaly sčítají, když se pohybujete v řadě dolů.
Velikost prvku se zmenšuje, když se pohybujete po určité periodě, protože počet elektronových obalů zůstává konstantní, ale počet protonů v jádře stoupá. To je důvod, proč je atom těžší, ale velikost se stále zmenšuje.
Při pohledu na periodickou tabulku byste v každém řádku viděli různé prvky. 1. období má pouze 2 prvky (1 a 18), 2. a 3. období má každý 8 prvků, 4. a 5. období má 18 prvků a 6. a 7. období má každý 32 prvků.
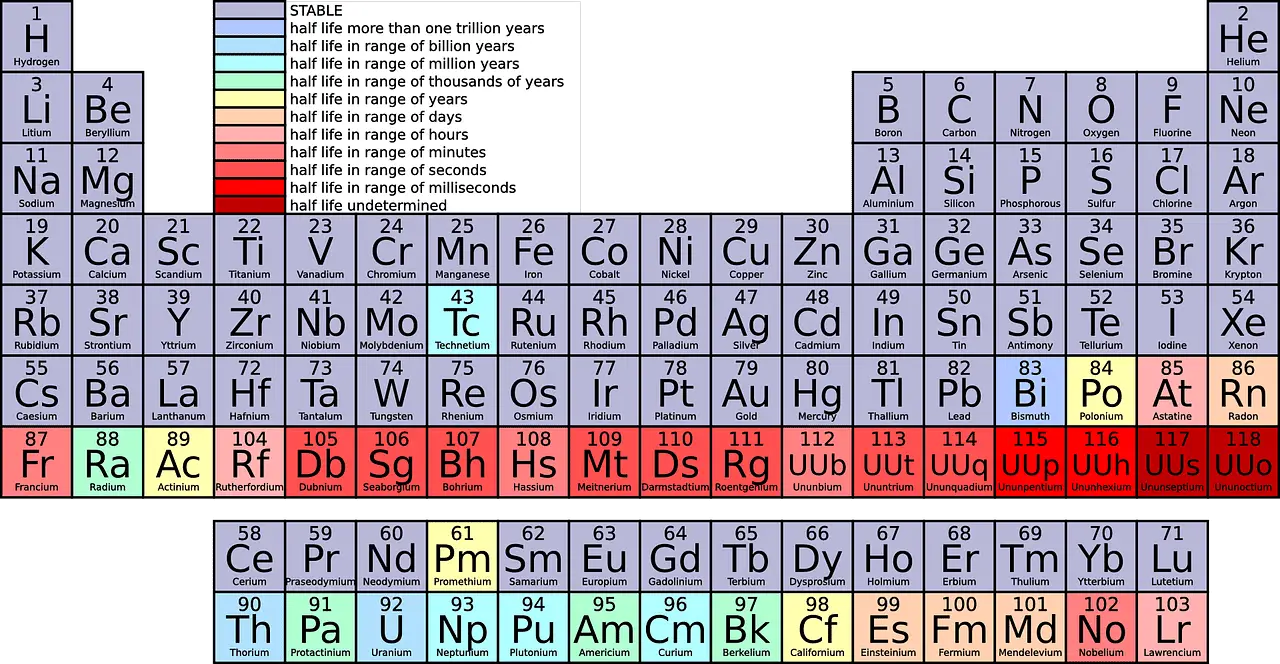
Co je skupina?
Při počítání shora dolů je v periodické tabulce 18 skupin. Všem skupinám jsou přidělena odlišná jména.
Skupiny jsou smíšené kategorie kovů, nekovů a polokovů, seskupené do skupin podle jejich podobných vlastností. Např. skupina 1 patří do rodiny lithia, klasifikované jako alkenové kovy.
Podobně má každá skupina v pruhu své příjmení. Prvky v příbuzné skupině mají podobné vlastnosti, protože mají stejný počet elektronů ve svých nejvzdálenějších obalech.
Velikost prvku se zvětšuje, když pohybujete libovolnou skupinou směrem dolů. Je to proto, že v jádře existuje velké množství protonů a neutronů.
Navíc další elektronový obal dělá atom těžší. Pro skupiny existují dva různé způsoby znázornění prvků.
Pochopení obou systémů číslování je nezbytné, protože periodická tabulka se objevuje v obou formátech. Ve Spojených státech používali k označení každého prvku ve skupině písmena A&B, ale bohužel to bylo pozorováno jako neuspořádaný systém číslování.
Aby se odstranil veškerý možný zmatek, Internacionála svaz of Pure and Applied Chemistry (IUPAC) Přišel s myšlenkou číslovat prvky jako (1,2, 3… 18). Oba systémy číslování jsou však přijatelné. Ale číslování IUPAC vypadá dobře organizované a přímočaré.
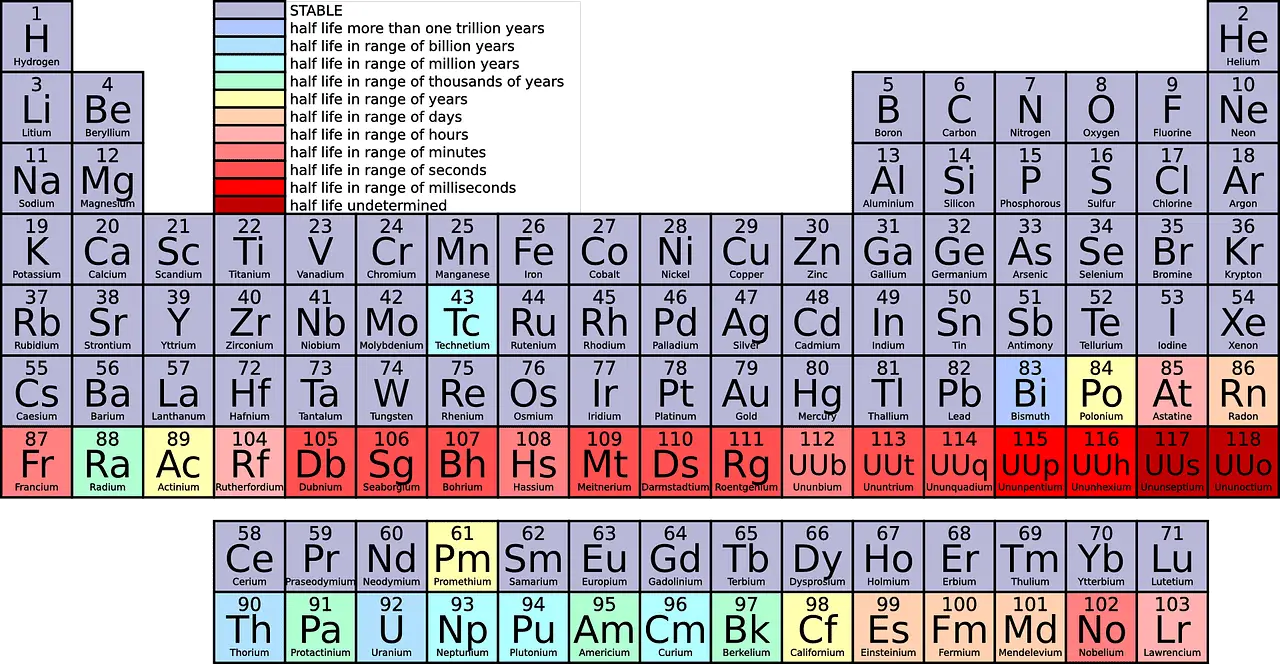
Hlavní rozdíly mezi Období a skupina
- pronájem: Skupiny jsou svislý sloupec, zatímco období jsou rovné řádky v periodické tabulce.
- Číslo: V periodické tabulce je celkem 18 skupin a 7 period, mezi nimiž jsou skupiny rozděleny do různých rodin a typů kovů.
- Chemické vlastnosti: Všechny prvky ve skupině mají analogické chemické nebo fyzikální vlastnosti, zatímco periody sdílejí stejnou elektronovou hierarchii.
- Úroveň energie: Jak jdeme po skupině shora dolů, energetická hladina elektronů se zvyšuje. Na druhou stranu v každé periodě zůstává energetická hladina elektronu stejná.
- Elektronegativita: Ta ve skupině klesá shora dolů a v období stoupá zleva doprava. Toto je zásadní úvaha při studiu periodické tabulky.

Poslední aktualizace: 11. června 2023

Piyush Yadav strávil posledních 25 let prací jako fyzik v místní komunitě. Je to fyzik, který je zapálený pro zpřístupnění vědy našim čtenářům. Je držitelem titulu BSc v přírodních vědách a postgraduálního diplomu v oboru environmentální vědy. Více si o něm můžete přečíst na jeho bio stránka.

Skvělý článek! To dává velký přehled o důležitosti periodické tabulky. Opravdu jsem si to užil!
Jsem velmi rád, že vám to pomohlo. Já taky!
Rozhodně by si to měl přečíst každý student přírodních věd.
Velmi informativní příspěvek. Měli bychom prosazovat lepší vzdělávání a porozumění vědeckým tématům.
To je přesně to, co potřebujeme.
To je jen další příklad zastaralých vzdělávacích standardů. Měli bychom studenty učit relevantnější témata.
Věřím, že je životně důležité, aby studenti porozuměli periodické tabulce.
To je kontroverzní názor, Joeli.
Myslím, že lidé podceňují hodnotu periodické tabulky. Měli bychom udělat více, abychom zlepšili naši výuku.
Rozhodně, toto je důležitý bod.
Myslím, že je opravdu zajímavé, že do tak zdánlivě jednoduché tabulky se vejde tolik cenných informací.
Ano, je to docela fascinující.
To je poučné. Periodická tabulka je podhodnocena.
Tohle bylo tolik potřebné čtení pro začátek mého dne!
Některé platné body jsou zde uvedeny, ale stále nejsem přesvědčen o důležitosti periodické tabulky.
Souhlasím s tebou, Zachu.
Periodická tabulka je základním kamenem chemie a tak by se s ní mělo zacházet.
Nemohl jsem souhlasit víc.
Nesouhlasím, domnívám se, že výuka periodické tabulky současným způsobem je zastaralá a měla by být revidována.
Chápu, proč by to některým mohlo připadat zastaralé, ale pro vědecký vývoj je to skutečně životně důležité.
Chápu, co říkáš, ale úplně nesouhlasím.
I když chápu důležitost periodické tabulky, je těžké tvrdit, že současný vzdělávací systém je adekvátní.
Vznesl jsi důležitý bod, Erin.