Kada element i spoj reagiraju jedan s drugim, dolazi do kemijske reakcije. I ova reakcija sama po sebi stvara potpuno novi proizvod.
Ova reakcija također mijenja raspored atoma u svakom elementu i spoju.
Stoga on ili apsorbira energiju ili je oslobađa, a to se radi kako bi došlo do promjena i reakcije.
Na temelju cijelog ovog postupka i zbivanja, kemijska reakcija se dalje dijeli na dva dijela - egzotermnu reakciju i endotermnu reakciju.
Ključni za poneti
- Egzotermna reakcija je kemijska reakcija koja oslobađa toplinu u okolinu, dok je endotermna reakcija kemijska reakcija koja apsorbira toplinu iz okoline.
- U egzotermnoj reakciji, energija oslobođena tijekom reakcije uglavnom je u obliku topline i svjetlosti, dok je u endotermnoj reakciji apsorbirana energija uglavnom u obliku topline.
- Izgaranje goriva primjer je egzotermne reakcije, dok je fotosinteza primjer endotermne reakcije.
Egzotermna vs endotermna reakcija
Razlika između egzotermne i endotermne reakcije je u tome što endotermna reakcija apsorbira energiju u obliku topline koja se apsorbira iz same okoline, dok egzotermna reakcija, s druge strane, oslobađa energiju u svojoj okolini. Primjer egzotermne reakcije može biti disanje, dok je primjer endotermne reakcije topljenje leda.

Egzotermna reakcija je oblik kemijske reakcije koja oslobađa energiju u okolnom okolišu kada se dogodi.
Energija koja se oslobađa tijekom egzotermne reakcije veća je od energije koja je potrebna za početak ili čak za izvođenje cijele kemijske reakcije.
Energija koja se oslobađa u okoliš uglavnom je u obliku topline ili svjetlosti.
Dvije su različite vrste kemijskih reakcija, a jedna od njih je endotermna reakcija, gdje se reaktanti koji su dio te kemijske reakcije uzimaju energiju iz okoline kako bi izveli reakciju, a ta energija je samo u obliku topline. Temperatura okoline se hladi kada se dogodi endotermna reakcija. Egzotermna reakcija je suprotna od endotermne reakcije.
Oboje su dijelovi kemijske reakcije.
Tabela za usporedbu
| Parametri usporedbe | Egzotermna reakcija | Endotermna reakcija |
|---|---|---|
| Definicija | Egzotermne reakcije su one reakcije u kojima se energija oslobađa u okolinu. Ako bilo koji proces zahtijeva zagrijavanje, drugi bi trebali otpuštati toplinu dok se odvijaju. Oni su poznati kao egzotermni. | Endotermne reakcije su one reakcije u kojima se energija apsorbira iz okoline. Endotermna reakcija je dio kemijske reakcije koja se odvija u okolišu. |
| Entalpija | U egzotermnoj reakciji promjena entalpije je negativna. | U endotermnoj reakciji promjena entalpije je pozitivna. |
| Oblik energije | U egzotermnoj reakciji, energija se oslobađa u mnogim oblicima - toplina, svjetlost, elektricitet itd. | U endotermnoj reakciji energija se oslobađa samo u obliku topline. |
| Primjer | Disanje. | Otapanje leda. |
| energija | Energija se oslobađa u okoliš u bilo kojem obliku u endotermnoj reakciji. | Energija se apsorbira iz okoline u endotermnoj reakciji. |
Što je egzotermna reakcija?
Egzotermna reakcija oslobađa svu toplinu u okolinu i istovremeno zamjenjuje slabe veze s jačima.
Postoji još jedan oblik reakcije nazvan egzergonski reakcija, s kojom se brka i egzotermna reakcija. Međutim, vrlo jaka egzotermna reakcija može se nazvati egzergonskom, ali ne uvijek.
Uglavnom, ako bilo koji proces zahtijeva toplinu, drugi bi trebali otpuštati toplinu dok se odvijaju. Oni su poznati kao egzotermni.
Na primjer, para koja nije ništa drugo nego plinoviti oblik vode kondenzira se, a toplina se oslobađa u okolnom okolišu. Slično, kada se voda u svom tekućem obliku smrzava, toplina se oslobađa u okoliš.
Tekuća voda je morala imati energiju u sebi da postane para, ali ta se energija uopće ne gubi u okolišu.

Što je endotermna reakcija?
Porast entalpije nije ništa drugo nego endotermna reakcija sustava. Endotermna reakcija je dio kemijske reakcije koja se odvija u okolišu.
Govoreći o bilo kojem zatvorenom sustavu, ono što reakcija uzrokuje u okolini je da apsorbira Termalna energija iz svoje okoline koja zapravo nije ništa drugo nego toplina prenesena u isti sustav reakcije tijekom procesa.
Kada dođe do endotermne reakcije, okolina oko nje se hladi, a to je zbog razloga što se toplinska energija apsorbira u reakciji.
Endotermna reakcija nije velika ili izvanredna reakcija. Zapravo, to može biti i jednostavan kemijski proces, na primjer - otapanje amonijevog nitrata u vodi, ili čak bilo koji fizički proces koji zahtijeva oslobađanje topline, poput topljenja leda. Oboje su dijelovi kemijske reakcije. Stoga, u svakom od ovih pojmova, prefiks riječi ovisi o toplini, bilo da izlazi ili se oslobađa.
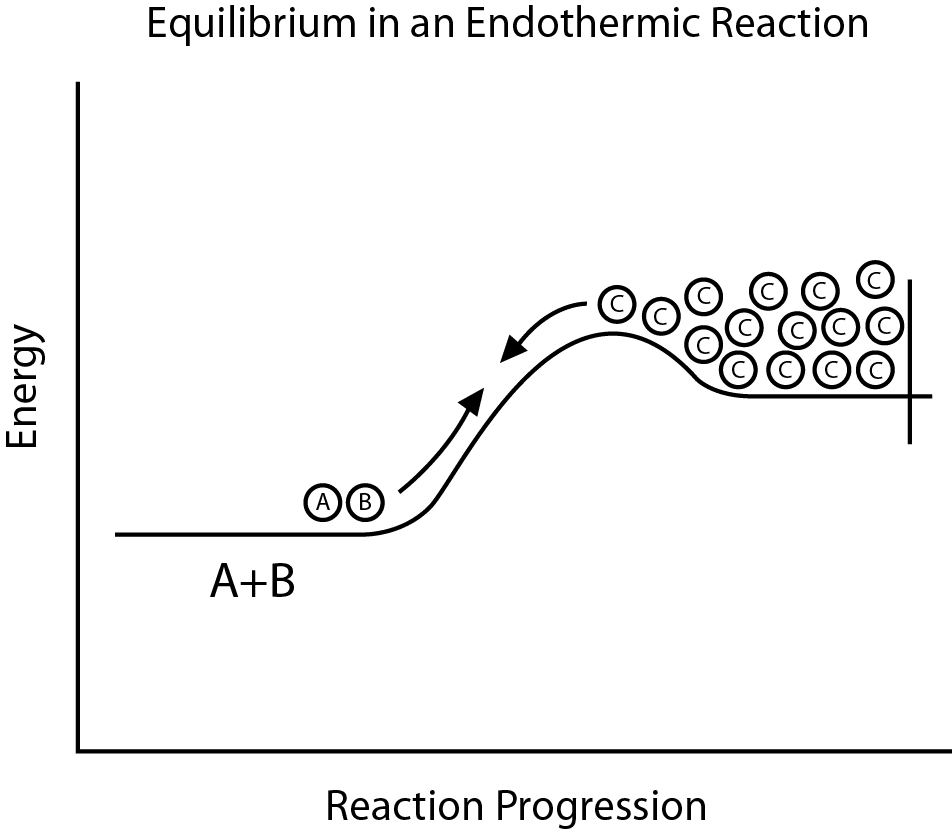
Glavne razlike između egzotermne i endotermne reakcije
- Glavna razlika između egzotermne i endotermne reakcije je u tome što su egzotermne reakcije one reakcije koje oslobađaju energiju u okolini kada se dogodi, dok su endotermne reakcije, s druge strane, one koje apsorbiraju energiju iz okolnog okoliša kako bi se mogle izvesti.
- Promjena entalpije je negativna u egzotermnoj reakciji, dok je u endotermnoj reakciji promjena entalpije pozitivna.
- Energija se može osloboditi u bilo kojem obliku, recimo toplina, svjetlost, elektricitet itd., kada se odvija egzotermna reakcija, ali u endotermnoj reakciji energija se oslobađa u samo jednom jedinom obliku, a to je zagrijavanje.
- Primjer egzotermne reakcije bilo bi disanje, dok bi primjer endotermne reakcije bilo topljenje leda.
- U endotermnoj reakciji energija se oslobađa u okolinu, dok se u endotermnoj reakciji energija apsorbira iz okoline.
- https://www.nature.com/articles/s41563-020-00851-x
- https://www.sciencedirect.com/science/article/pii/0010218080900176
Zadnje ažuriranje: 15. kolovoza 2023

Piyush Yadav proveo je posljednjih 25 godina radeći kao fizičar u lokalnoj zajednici. On je fizičar koji strastveno želi učiniti znanost dostupnijom našim čitateljima. Posjeduje diplomu prirodnih znanosti i poslijediplomski studij znanosti o okolišu. Više o njemu možete pročitati na njegovom bio stranica.


Detaljno objašnjenje egzotermnih i endotermnih reakcija u članku korisno je za studente i sve one koje zanima kemija.
Smatram da je sadržaj dobro strukturiran i informativan, pružajući jasno razumijevanje kako se te reakcije javljaju.
U članku se vrlo jasno i koncizno objašnjava pojam egzotermnih i endotermnih reakcija. To je izvrstan izvor za svakoga tko želi dublje razumjeti ove koncepte.
To svakako pruža čvrst temelj za razumijevanje ovih temeljnih kemijskih reakcija.
Ovaj članak učinkovito objašnjava koncepte egzotermnih i endotermnih reakcija, pružajući jasne primjere i temeljitu usporedbu njihovih svojstava.
Članak je vrijedan izvor za stjecanje dubljeg razumijevanja egzotermnih i endotermnih reakcija u kemiji.
To je dobro napisano djelo koje zadire u složenost egzotermnih i endotermnih reakcija, što ga čini zanimljivim štivom.
Članak pruža sveobuhvatan pregled egzotermnih i endotermnih reakcija, promičući čitateljevo razumijevanje složenih procesa uključenih u kemijske reakcije.
Smatram da su primjeri egzotermnih i endotermnih reakcija osobito korisni u razjašnjavanju razlika između njih dvoje.
Detaljni primjeri i usporedna tablica jasno pokazuju razlike između egzotermnih i endotermnih reakcija, omogućujući bolje razumijevanje njihovih svojstava.
Praktični primjeri navedeni u članku podržavaju sveobuhvatno razumijevanje egzotermnih i endotermnih reakcija.
Logičan tijek članka pomaže da se sažeto ocrtaju ključni pojmovi koji podupiru egzotermne i endotermne reakcije.
Cijenim temeljitu usporedbu između egzotermnih i endotermnih reakcija, što olakšava razumijevanje razlika i primjene svake vrste reakcije.
Članak učinkovito prikazuje bit egzotermnih i endotermnih reakcija, pružajući dragocjene uvide u njihovo značenje.
Članak briljantno razrađuje egzotermne i endotermne reakcije, ističući njihovo značenje u razumijevanju kemijskih procesa.
Vrlo zanimljiv članak koji objašnjava razlike između egzotermnih i endotermnih reakcija, kao i kako se odvijaju kemijske reakcije. Navedeni primjeri su vrlo ilustrativni.
Uživao sam čitajući ovaj članak, sjajno je osvježenje osnovnih načela kemije.
Slažem se, to je vrlo iscrpno i prosvjetljujuće objašnjenje.
Ovaj članak nudi pronicljivo istraživanje egzotermnih i endotermnih reakcija, pridonoseći dubljem razumijevanju ovih temeljnih kemijskih fenomena.
Opsežna pokrivenost članka egzotermnim i endotermnim reakcijama omogućuje čitateljima da učinkovitije shvate složenost kemijskih reakcija.
Članak nudi dobro organizirano i pronicljivo objašnjenje egzotermnih i endotermnih reakcija, pružajući vrijedno iskustvo učenja.
Dubinska analiza prijenosa toplinske energije u egzotermnim i endotermnim reakcijama uvelike doprinosi razumijevanju ovih temeljnih kemijskih procesa.