Studējot ķīmiju un dažreiz arī fiziku, bieži tiek lietotas tādas terminoloģijas kā elementi un atomi. Tomēr, tēmai attīstoties un kļūstot arvien sarežģītākai, terminu nozīmes var viegli sajaukt.
Atslēgas
- Elementus nevar sadalīt vienkāršās vielās ar ķīmiskiem līdzekļiem. Tajā pašā laikā atomi ir mazākā elementa daļiņa, kas saglabā šī elementa ķīmiskās īpašības.
- Elementiem ir unikāli atomu skaitļi, kas nosaka to īpašības un atrašanās vietu periodiskajā tabulā, savukārt atomiem ir protoni, elektroni un neitroni, kas nosaka to uzvedību un mijiedarbību.
- Elementi var apvienoties, veidojot savienojumus, bet viena un tā paša elementa atomus nevar tālāk sadalīt, nemainot vielas ķīmiskās īpašības.
Elementi pret atomiem
Elementi un atomi atšķiras, jo sastāvdaļa ir visvienkāršākā vielas forma, kas sastāv no atomiem. Aspekts tiek klasificēts atkarībā no tā atomu skaita. Subatomiskās daļiņas apvienojas, veidojot atomus, kas saplūst, veidojot elementu. Vēlāk elementi apvienojas, veidojot molekulas.

Atšķirībā no ķīmiskajiem savienojumiem ķīmiskos elementus nevar segmentēt vienkāršākās vielās ar jebkādu ķīmisku metodi. Periodiskajā elementu tabulā elementi ir sistematizēti pēc to atomu skaita.
Atoms ir mazākā parastās vielas daļa, kas rada ķīmisku elementu. Atoms sastāv no subatomiskām daļiņām. Vienkāršiem vārdiem sakot, atomi ir elementu veidošanas bloki.
Salīdzināšanas tabula
| Salīdzināšanas parametri | Elementi | Atomi |
|---|---|---|
| Izmēri | Lielāks par atomiem | Ļoti mazs (pat mikroskopā nevar redzēt) |
| Veidu skaits | Kopumā ir 118 elementi. | Dabā ir pieejami aptuveni 92 veidu atomi. |
| Sastāvs | Konkrēts elements sastāv tikai no viena noteikta veida atoma. | Atomi sastāv no subatomiskām daļiņām. Tie ir protoni, elektroni un neitroni. |
| Kad tie apvienojas | Elementi apvienojas, veidojot jaunas ķīmiskas reakcijas. | Kad atomi apvienojas, tie veido molekulu. |
| svars | Smagāks par konkrētu atomu. | Īpaši viegls (relatīvais svars ir 1 AMU) |
Kas ir elementi?
Elements ir pamatjēdziens, kas jāzina, lai saprastu progresīvu ķīmiju. Savos atomu kodolos elements sastāv tikai no atomiem, kas satur vienādu skaitu protonu.
Ķīmiskos elementus nevar sadalīt vienkāršotākos elementos vai vielās, izmantojot nevienu ķīmisku metodi. Pēdējais tiek attiecināts uz atomskaitli, ko apzīmē ar simbols "Z.'
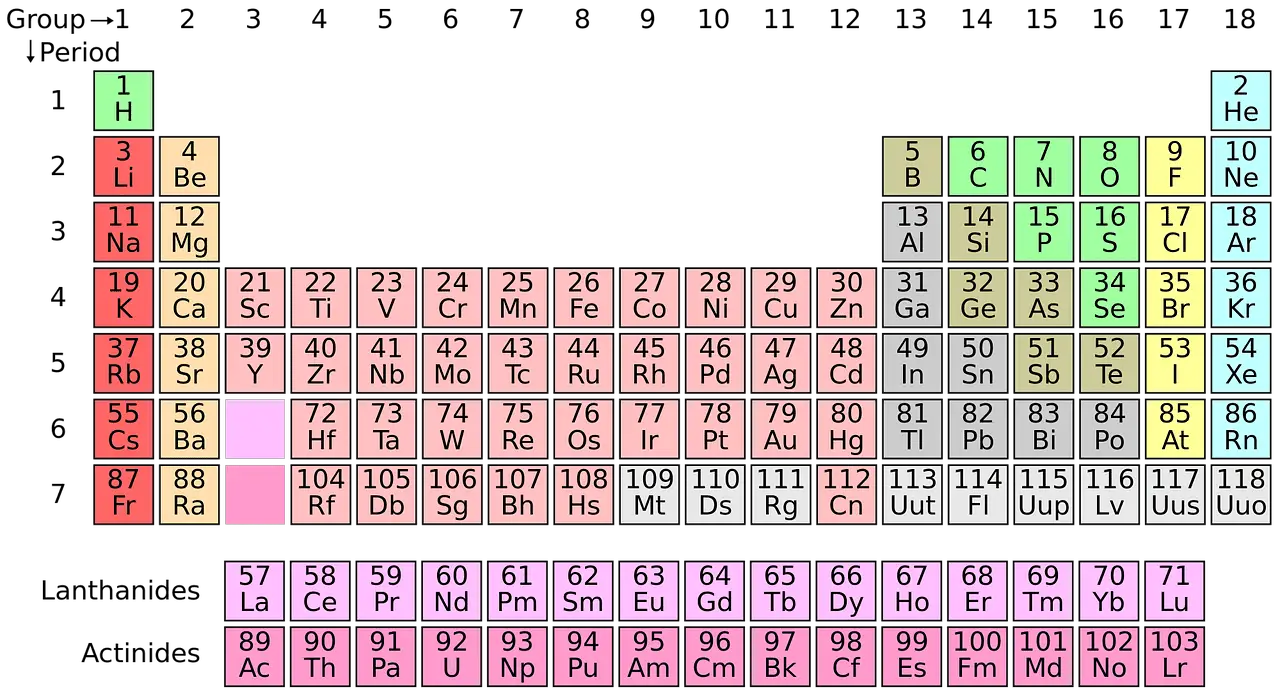
Mūsdienu ķīmija lielā mērā ir atkarīga no periodu tabulas. Visi atklātie elementi tiek klasificēti un sistemātiski sakārtoti periodiskajā tabulā. Šo koncepciju izstrādāja krievu ķīmiķis Dmitrijs Mendeļejevs 1869. gadā.
Elementa raksturlielumi ir atbildīgi par tā fizisko stāvokli istabas vai vidējā temperatūrā. Tas var būt gan gāzveida, gan ciets vai šķidrs.
Kopumā ir aptuveni 118 elementu veidi.
Daži elementu piemēri ir šādi:
- Ūdeņradis
- Ogleklis
- Neons
- magnijs
- alumīnijs
- bors
Kas ir atomi?
Atomi ir mazākā parastās vielas vienība. Tie ir niecīgi, to aptuvenais izmērs ir 100 pikometri. Turklāt atoms ir ļoti viegls. Relatīvi pēdējās svars ir nosacīti 1AMU.
Kodols sastāv no viena vai vairākiem protoniem un vairākiem neitroniem. Šim noteikumam ir tikai viens izņēmums: ūdeņradis, kuram nav neitronu. Kodols veido 99.94% no atoma masas.
Protoniem ir pozitīvs elektriskais lādiņš, elektroni satur negatīvu elektrisko daudzumu, un neitroniem nav elektriskās vadības. Atoms ir elektriski neitrāls, ja protonu un elektronu skaits ir vienāds.
Dabā ir 92 dažādu veidu atomi.
Primārais jēdziens un jēdziens Tas, ka matērija sastāv no sīkām nedalāmām daļiņām, ir sena. Atomu vēsture aizsākās senos Indijas un Grieķijas laikos.

Galvenās atšķirības starp elementiem un atomiem
- Ja vairāk nekā viens elements apvienojas, tie veido jaunu ķīmisku reakciju, kā rezultātā rodas jauns elements. Kad apvienojas vairāk nekā viens atoms (turot dažādas vielas nemainīgas), tie veido molekulu.
- Elementa svars ir smagāks, salīdzinot ar atomu, bet atomu gadījumā pēdējais ir ārkārtīgi viegls. Pēdējā relatīvais svars ir aptuveni 1 AMU.
- https://books.google.com/books?hl=en&lr=&id=EvTI-ouH3SsC&oi=fnd&pg=PP1&dq=elements&ots=pQ5TOAfsJ3&sig=LBL5oWU1-cH9p_y8JPtdmdjok7g
- https://pubs.acs.org/doi/pdf/10.1021/ar00109a003
Pēdējo reizi atjaunināts: 11. gada 2023. jūnijā

Pijušs Jadavs pēdējos 25 gadus ir pavadījis, strādājot par fiziķi vietējā sabiedrībā. Viņš ir fiziķis, kurš aizrautīgi cenšas padarīt zinātni pieejamāku mūsu lasītājiem. Viņam ir bakalaura grāds dabaszinātnēs un pēcdiploma diploms vides zinātnē. Vairāk par viņu varat lasīt viņa vietnē bio lapa.


Padziļinātie skaidrojumi ir ļāvuši vieglāk uztvert atšķirības starp elementiem un atomiem, pievienojot milzīgu izglītojošu vērtību.
Detalizēts elementu un atomu salīdzinājums ir izrādījies izglītojošs līdzeklis.
Skaidrais un detalizētais elementu un atomu salīdzinājums ir atvieglojis to atšķirību izpratni, kalpojot kā lielisks mācību līdzeklis.
Mācīšanās par atšķirībām starp elementiem un atomiem no šī raksta ir bijusi diezgan saprotama un izglītojoša.
Informatīvais saturs par elementiem un atomiem ir padarījis abu jēdzienu salīdzinājumu diezgan skaidru un saprotamu.
Šis raksts ir sniedzis visaptverošu un informatīvu detalizētu elementu un atomu salīdzinājumu un sniedzis nenovērtējamu ieskatu to attiecīgajās īpašībās un uzvedībā.
Mani pārsteidz šajā rakstā sniegtais skaidrais elementu un atomu atšķirību salīdzinājums.
Rakstam ir liela izglītojoša vērtība, īpaši tiem, kam ir liela interese par zinātni un ķīmiju.
Tas noteikti ir vērtīgs resurss ikvienam, kas vēlas uzzināt par elementiem un atomiem.
Tas ir izrādījies vērtīgs elementu un atomu fundamentālās zinātniskās koncepcijas izpratnē.
Visaptverošais elementu un atomu salīdzinājums ir bijis izglītojošs, piedāvājot labāku izpratni par šiem zinātniskajiem jēdzieniem.
Dziļa iegremdēšanās elementu un atomu salīdzināšanā ir sniegusi vērtīgu izglītojošu pieredzi, atvieglojot šo zinātnisko jēdzienu izpratni.
Šajā rakstā ir izdevies sniegt ieskatu un visaptverošu elementu un atomu salīdzinājumu, kas ir ļoti noderīgs izglītības nolūkos un zinātnisko koncepciju izpratnei.
Šī raksta elementu un atomu salīdzinājuma izglītojošā vērtība ir patiesi slavējama.
Visaptveroša informācija par elementu un atomu galvenajām iezīmēm ir ļoti noderīga, lai labāk izprastu šos jēdzienus.