Molekulas un elementi sastāv no atomiem. Atomi ir mazākā vienība, ko nevar vienkāršot mazākos materiālos. Elementi ir atvasināti no atoma īpašībām. Atomi veido molekulu un elementu pamatu.
Ir svarīgi precīzi nošķirt molekulas un elementus, lai izpētītu to īpašības un raksturu.
Atslēgas
- Elements ir tīra atomu viela ar vienādu protonu skaitu.
- Molekula apvieno divus vai vairākus atomus, ko satur ķīmiskās saites.
- Elementus nevar sadalīt vienkāršākās vielās, savukārt molekulas var sadalīt to veidojošos atomos.
Molekula pret elementu
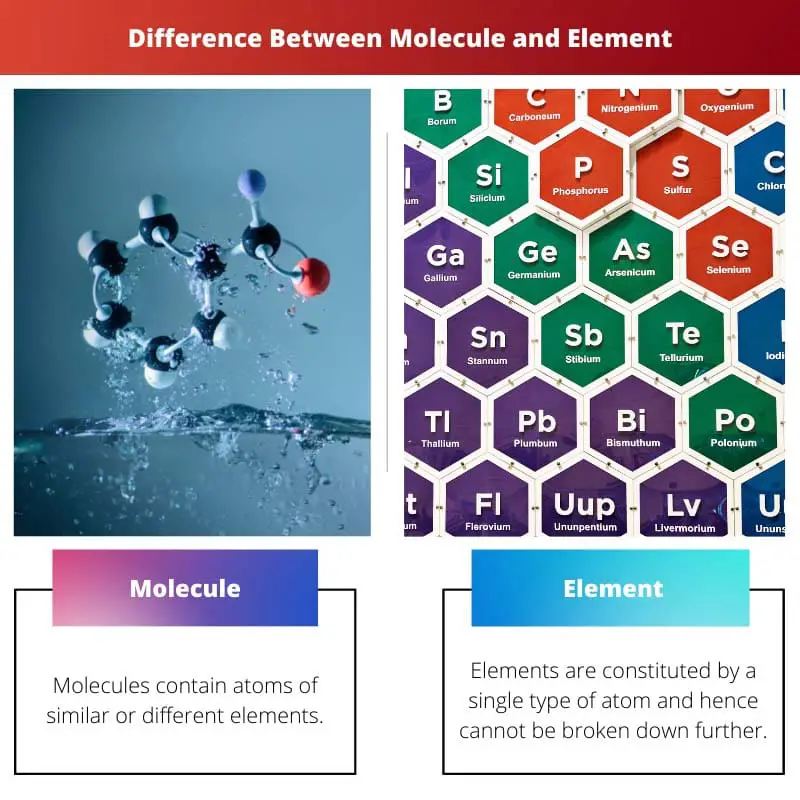
Atšķirība starp molekulām un elementiem slēpjas to īpašībās un veidošanā. Molekulas sastāv no diviem vai vairākiem atomiem, kas veido līdzīgu vai atšķirīgu elementu ķīmiskās saites. No otras puses, elementiem ir dažādi veidojumi. Tos veido viens atoms. Tās nevar būt brālis vienkāršākām vielām, jo tās pastāv tīrā veidā.

Molekulas veidojas, ķīmiski savienojoties diviem vai vairākiem atomiem. Ķīmiskās saites veidojas elektronu apmaiņas rezultātā. Kad elementu atomi savienojas viens ar otru, tie rada molekulas.
Dažu elementu atomi var būt viegli savienojami, piemēram, ar hloru, savukārt daži var būt grūti savienojami, piemēram, ar argonu.
Elements sastāv no viena veida atoma. Elementu daļiņas var būt mākslīgas vai mākslīgas. Dažādi atomu izvietojumi var radīt dažādas šī elementa versijas.
Piemēram, lai gan dimanta un grafīts ir oglekļa alotropi, pēc izskata tie ir diezgan atšķirīgi. Tiem ir tāda pati ķīmiskā struktūra, bet atšķirīgas ķīmiskās īpašības.
Salīdzināšanas tabula
| Salīdzināšanas parametri | molekula | Elements |
|---|---|---|
| Atomi | Molekulas satur līdzīgu vai dažādu elementu atomus. | Elementus veido viena veida atomi, un tāpēc tos nevar sadalīt tālāk. |
| Dalīšana | To var sadalīt tālāk, izmantojot ķīmiskos līdzekļus. | To nekādā gadījumā nevar sadalīt tālāk. |
| Saites | Tie veido vai nu jonu, vai kovalentās saites. | Tās var veidot dažāda veida saites atkarībā no stabilitātes un elektroniskās konfigurācijas. |
| Biedri | Tas sastāv no diviem vai vairākiem atomiem, kas saistīti viens ar otru. | Pašlaik ir 115 ķīmiskie elementi. |
| Piemēri | Tā piemēri ir ūdens, oglekļa-d-oksīds, ozons utt. | Tā piemēri ir slāpeklis, varš, cinks, skābeklis utt. |
Kas ir molekula?
Vārds molekula attiecas uz atomiem, kurus satur spēcīgas ķīmiskas saites. To izmērs atšķiras atkarībā no savienotajiem atomiem. Dažas molekulas veido divi līdzīgi atomi, bet citas - sarežģītas saites.
- Divi līdzīga elementa atomi: Skābeklis (O2), ko veido divi skābekļa atomi
- Trīs līdzīga elementa atomi: Ozons(03), ko veido trīs skābekļa atomi
- Sarežģīta savienošana: Oglekļa dioksīds (CO2), veidojas, saistot vienu oglekļa atomu un divus skābekļa atomus
Molekulas var veidot vai nu kovalentās saites, vai jonu saites. Kovalentā saite ir pazīstama arī kā dalīta saite. Kovalentajās saitēs atomi dalās ar saviem elektroniem, turpretim jonu saitēs atoms savu elektronu ziedo citam atomam.
Atsevišķs elements netiek uzskatīts par molekulu. Piemēram, viens skābekļa (O) vai oglekļa (C) elements nav molekula. Molekulas veidojas, kad divi vai vairāki atomi veido ķīmisko saiti.
Dažas izplatītas molekulas ir ozons, ūdens, glikoze utt.
Molekulas tiek sadalītas, pamatojoties uz vairākām kategorijām, no kurām dažas ir homonukleāras un heteronukleāras molekulas, organiskas vai neorganiskas molekulas, divatomiskas, trīsatomiskas vai poliatomiskas molekulas utt.

Kas ir elements?
Elementi ir tīras vielas, kuras nevar sadalīt vai sadalīt tālāk vienkāršākā vielā. Tie var attiekties uz atomiem, kuru kodolā ir līdzīgs protonu skaits. Tie var atšķirties pēc masas un neitroniem.
Ja atomiem, kas satur līdzīgus elementus, ir noteikts neitronu skaits, tos sauc par izotopi.
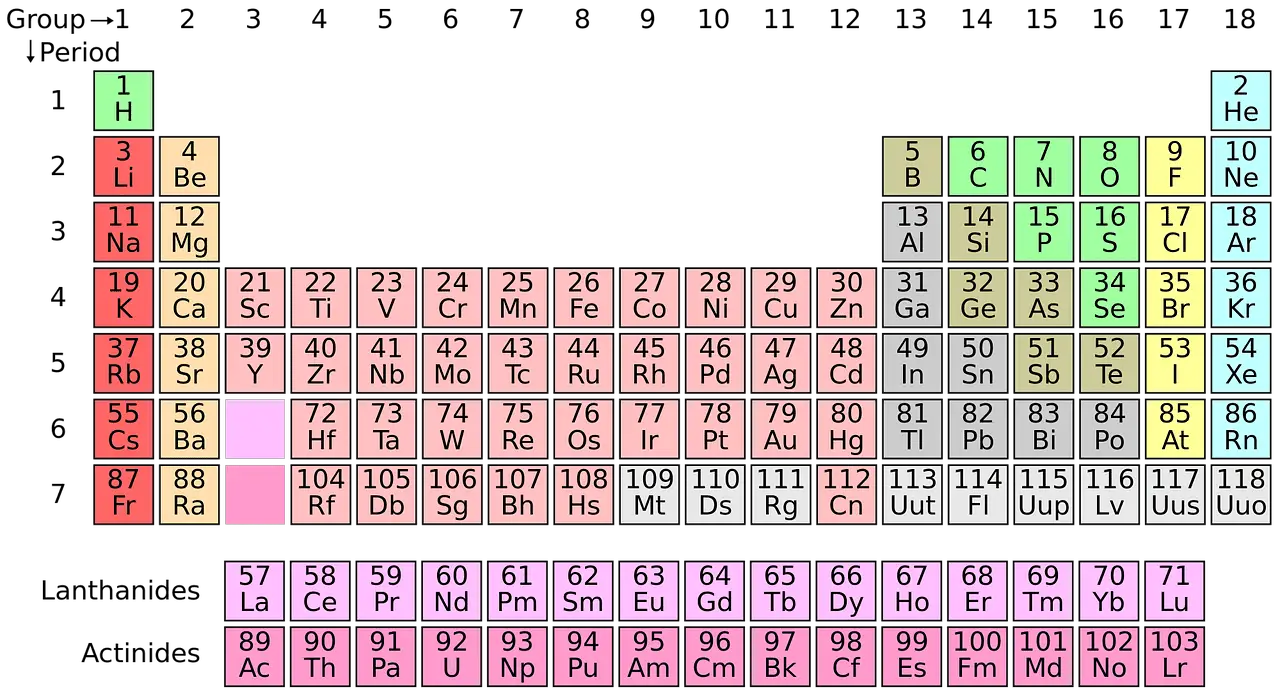
Periodiskajā tabulā ir 118 elementi. Periodiskajā tabulā elementi tiek klasificēti, pamatojoties uz to īpašībām un atomu skaitu.
Katram elementam ir savs unikālais atomu simbols, atomu masa, simbols un elektroniskais izvietojums.
Rodas nepieciešamība klasificēt elementus periodiskajā tabulā. Kļūst apgrūtinoši izpētīt katra no 118 elementiem īpašības. Tātad zinātnieki ir izstrādājuši veidu, kā grupēt līdzīgu īpašību elementus.
Šīs grupēšanas tiek veiktas, pamatojoties uz četriem blokiem.
- s bloks: s-bloka elementus iedala 2 grupās. 1. grupas elementi tiek saukti par sārmu metāliem, bet 2. grupas elementi ir nosaukti kā sārmains zemes metāli.
- p bloks: p-bloka elementus iedala metālos, nemetālos un metaloīdos.
- d bloks: d-bloka elementi sastāv no trim rindām, proti, pirmās, otrās un trešās pāreju sērijas.
- f bloks: f-blokā kopā ir divdesmit astoņi elementi, kas ir sadalīti divās vienādās sērijās. Pirmo četrpadsmit elementu sēriju sauc par lantanīda sēriju. Otro četrpadsmit elementu kopu sauc par aktinīdu sēriju.
Galvenās atšķirības starp molekulu un elementu
- Molekula var būt homonukleāra vai heteronukleāra, savukārt elementam ir unikāls atomu numurs.
- Molekulās ir līdzīgu vai atšķirīgu elementu atomi, savukārt elementi satur tikai līdzīgus atomus.
- Molekulas un elementi atšķiras pēc to ķīmiskās konfigurācijas. Molekulas var veidot noteikta veida saites, ti, kovalentās vai jonu saites. No otras puses, elementi var veidot daudzu veidu saites, pamatojoties uz elektronu izvietojumu.
- Molekula ir viela, ko var tālāk sadalīt mazākās vielās, bet elementus nevar tālāk sadalīt ar ķīmiskiem līdzekļiem.
- Molekulu piemēri ir cukurs, glikoze, hlors, acetonsuc Elementu piemēri ir ogleklis, ūdeņradis, hēlijs utt.
- https://www.sciencedirect.com/science/article/pii/S0166354201002224
- https://aip.scitation.org/doi/abs/10.1063/1.329173
Pēdējo reizi atjaunināts: 23. gada 2023. jūlijā

Pijušs Jadavs pēdējos 25 gadus ir pavadījis, strādājot par fiziķi vietējā sabiedrībā. Viņš ir fiziķis, kurš aizrautīgi cenšas padarīt zinātni pieejamāku mūsu lasītājiem. Viņam ir bakalaura grāds dabaszinātnēs un pēcdiploma diploms vides zinātnē. Vairāk par viņu varat lasīt viņa vietnē bio lapa.


Ziņojums sniedz visaptverošu pārskatu par molekulu un elementu īpašībām un veidojumiem, piedāvājot detalizētu izpratni par jēdzieniem.
Periodiskās tabulas dažādo bloku apraksts ir ļoti saprotams, sniedzot pilnīgu izpratni par elementu klasifikāciju.
Ziņojums efektīvi atspoguļo atšķirību starp atomiem, molekulām un elementiem, pievienojot skaidrību to sastāvam.
Detalizēts skaidrojums par atšķirībām starp molekulām un elementiem ir ļoti informatīvs un sniedz skaidru izpratni par to īpašībām.
Es augstu vērtēju sniegtos detalizētos piemērus, kas vēl vairāk precizē molekulu un elementu jēdzienus.
Elementu klasificēšana periodiskajā tabulā ir labi izskaidrota, palīdzot izprast to grupēšanu, pamatojoties uz pazīmēm.
Elementu klasifikācija periodiskajā tabulā ir precīzi aprakstīta ziņojumā, piedāvājot vērtīgu ieskatu to klasifikācijā.
Detalizēts katra periodiskās tabulas bloka skaidrojums atvieglo elementu grupēšanas izpratni.
Es piekrītu jūsu vērtējumam, ziņa efektīvi ieskicē elementu klasifikāciju, pamatojoties uz to īpašībām.
Ziņojums efektīvi izskaidro atšķirības starp molekulām un elementiem, piedāvājot visaptverošu izpratni par to struktūrām un atomiem.
Detalizēts skaidrojums par to, kas veido elementu, kā arī molekulu, ir ļoti informatīvs un papildina ierakstu.
Ziņojumā ir apskatītas galvenās atšķirības starp molekulām un elementiem. Tas izskaidro abu struktūru un veidošanos, kā arī to īpašību izpētes nozīmi.
Jā, salīdzināšanas tabula sniedz skaidru izpratni par atšķirībām starp molekulām un elementiem.
Piekrītu, šī ziņa ir ļoti informatīva un detalizēta.
Ziņojumā ir izskaidrotas kritiskās atšķirības starp molekulām un elementiem. Detalizētais skaidrojums sniedz visaptverošu izpratni par to sastāvu un struktūru.
Piekrītu, ieraksts sniedz skaidru pārskatu par atomiem, molekulām un elementiem.
Molekulu un elementu piemēri vēl vairāk uzlabo izpratni par ziņojumā apspriestajiem jēdzieniem.
Ziņojums efektīvi formulē atšķirības starp molekulām un elementiem, kā arī detalizētu informāciju par to veidošanos un īpašībām.
Spot on, salīdzināšanas tabula un detalizēti apraksti ir ļoti noderīgi, lai izprastu jēdzienus.
Detalizētā salīdzināšanas tabula efektīvi iezīmē atšķirības starp molekulām un elementiem, sniedzot rūpīgu izpratni par to īpašībām un variācijām.
Piekrītu, molekulu un elementu īpašību un īpašību skaidrojums ir ļoti detalizēts un informatīvs.
Elementu klasifikācija un to īpašības tiek pasniegtas organizēti, uzlabojot amata saprotamību.
Detalizēts molekulu un elementu salīdzinājums ir ļoti saprotams, sniedzot visaptverošu izpratni par to struktūrām un veidojumiem.
Molekulu iedalījums kategorijās, pamatojoties uz dažādām kategorijām, ir vērtīgs ziņas papildinājums, uzlabojot izpratni par tēmu.
Atšķirība starp kovalentajām un jonu saitēm molekulās ir labi izskaidrota ziņojumā.
Detalizēts molekulu un elementu skaidrojums sniedz padziļinātu izpratni par to būtību un sastāvu.