De ziekte van Alzheimer is een progressieve neurodegeneratieve ziekte. Het is een van de belangrijkste oorzaken van seniele dementie. Het onderliggende mechanisme van de ziekte is nog steeds onduidelijk en onderwerp van verder wetenschappelijk onderzoek, maar twee van de meest populaire hypothesen voor het begrijpen van de ziekte van Alzheimer zijn de Amyloid- en de Tau-hypothese.
Key Takeaways
- Amyloïde verwijst naar eiwitafzettingen die plaques in de hersenen vormen, terwijl tau-eiwitten neurofibrillaire knopen in hersencellen vormen.
- Zowel amyloïde als tau worden in verband gebracht met de ziekte van Alzheimer, maar ze spelen een verschillende rol bij de progressie ervan.
- Huidige behandelingen voor de ziekte van Alzheimer richten zich op amyloïde, maar recent onderzoek suggereert dat het richten op tau effectiever kan zijn in het vertragen van cognitieve achteruitgang.
Amyloïde versus Tau
Zowel amyloïde als tau zijn abnormale eiwitafzettingen die in de hersenen worden aangetroffen bij de ziekte van Alzheimer. Dit zijn onoplosbare eiwitten en zijn opgebouwd uit compacte vezels. Amyloïde wordt afgezet buiten de hersencellen, terwijl tau wordt aangetroffen in de neuronale cellen. Amyloïde vormt plaques, terwijl tau klitten vormt.
Vergelijkingstabel
| Parameters van vergelijking: | amyloid | tau |
|---|---|---|
| Eiwittype: | Bèta-amyloïde eiwit | Tau-eiwit |
| Gebied van de getroffen hersenen | Hersencel verbindingen | Elektrische en chemische signalen van hersencellen |
| Symptomen | Geheugenverlies | Geheugenverlies, gedragsveranderingen |
| Veroorzakende factor | Vervanging van alfa-secretase-activiteit door bèta-secretase. | Hyperfosforylering van Tau-eiwit |
| Kenmerkende kenmerken | Amyloïde plaques | Neurofibrillaire knopen |
Wat is amyloïde?
De amyloïde-hypothese is een van de meer onderzochte hypothesen bij het zoeken naar behandelingen om de ziekte van Alzheimer te genezen. Normaal gesproken wordt het amyloïde-voorlopereiwit gesplitst door de activiteit van alfa-secretase en gamma-secretase, waardoor onschadelijke oplosbare peptiden worden geproduceerd.
Mutaties in genen die coderen voor amyloïde precursoreiwit en preseniline, dat een component is van gamma-secretase, zijn echter in verband gebracht met een verhoogde neiging tot de vorming van langere amyloïde fragmenten die samenklonteren om fibrillen en oligomeren te vormen.
Deze fibrillen en oligomeren zijn neurotoxisch en daarom verantwoordelijk voor neuronale dood. Deze oligomeren veroorzaken ook een cascade van gebeurtenissen die de neuronale cellen verder vernietigen. Eén route is kinase-activering die de uiteindelijke hyperfosforylering van Tau-eiwit veroorzaakt en resulteert in verdere neuronale vernietiging.
De amyloïde-hypothese wordt verder versterkt door de associatie met het vroege begin van de ziekte van Alzheimer bij mensen met het syndroom van Down. Omdat het amyloid-precursorproteïne-gen zich op chromosoom 21 bevindt, de extra kopie van chromosoom 21st chromosoom bij mensen met het syndroom van Down bewees dat problemen met het aantal chromosomen of de mutatie ervan een sterke oorzakelijke factor waren voor de ziekte van Alzheimer.
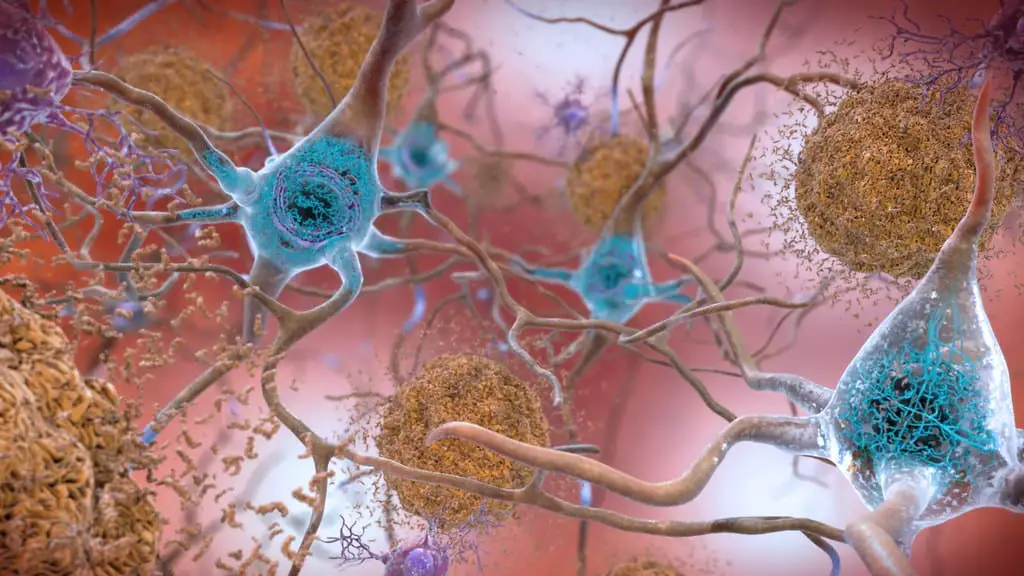
Wat is Tau?
De Tau-hypothese daarentegen is vrij recentelijk onderzocht als de primaire oorzaak van de ziekte van Alzheimer, nadat de proeven om de vorming van bèta-amyloïde-eiwitten tegen te gaan geen veelbelovende resultaten opleverden.
Bovendien kunnen neurofibrillaire knopen als gevolg van aggregatie van tau-eiwitten worden gezien bij patiënten met milde dementie maar zonder beta-amyloïde pathologie. Bovendien kunnen amyloïde plaques worden gezien bij mensen zonder neurodegeneratieve defecten, maar hetzelfde kan niet worden gezegd over mensen met neurofibrillaire knopen, aangezien de Tau-eiwitpathologie nauw verband houdt met de ernst en progressie van de ziekte van Alzheimer.
De Tau-hypothese stelt verder dat de Tau-pathologie voorafgaat aan elke bèta-amyloïde pathologie en de primaire oorzaak is van de ziekte van Alzheimer. Het Tau-eiwit is verantwoordelijk voor de stabiliteit van microtubuli, die het transport van voedingsstoffen in neuronale cellen en de integriteit van de algemene celstructuur in stand houden.
Wijziging van het Tau-eiwit door hyperfosforylering te ondergaan resulteert in Tau-eiwitaggregaties tot knopen, waardoor de microtubuli worden verstoord en de toevoer van voedingsstoffen en celstructuur wordt verstoord, wat resulteert in neuronale dood. Deze knopen kunnen zich verder verplaatsen via de axonen en andere neuronale cellen verstoren, wat resulteert in een functioneel verlies van delen van het zenuwstelsel, waardoor de ziekte van Alzheimer ontstaat.
De klinische proeven targeting Tau-eiwitten hebben nog geen gewenste resultaten opgeleverd, maar de hypothese is vrij recent bestudeerd, dus er zijn nog niet genoeg klinische gegevens beschikbaar.
Belangrijkste verschillen tussen amyloïde en tau
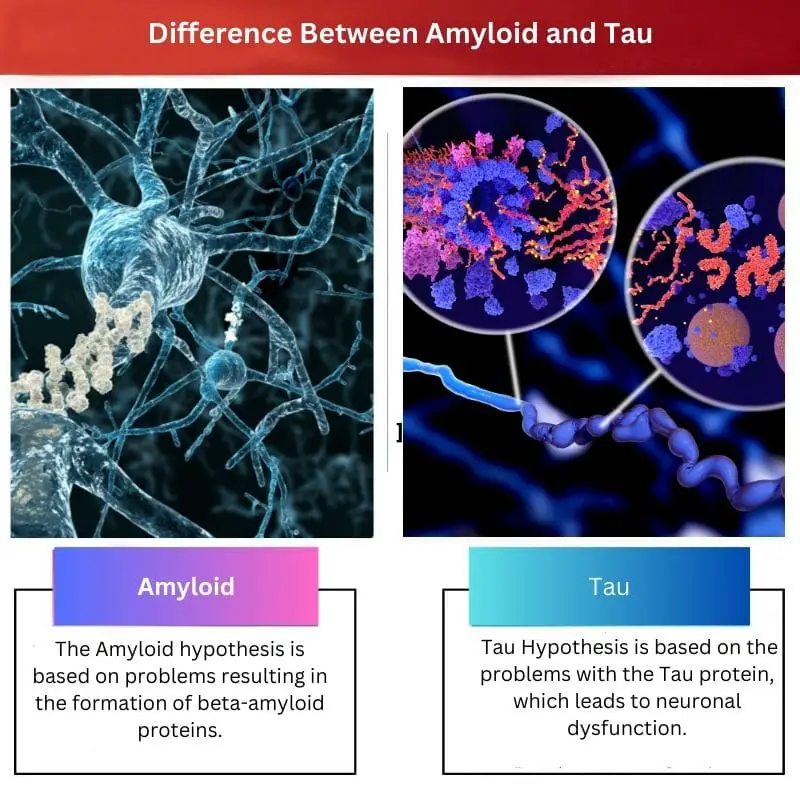
- De amyloïde-hypothese is gebaseerd op problemen die resulteren in de vorming van bèta-amyloïde-eiwitten, die worden gezien als een triggerpoint in de cascade van gebeurtenissen die leiden tot de ziekte van Alzheimer, terwijl de Tau-hypothese is gebaseerd op de problemen met het Tau-eiwit, dat leidt tot neuronale disfunctie.
- De amyloïdhypothese was gebaseerd op de sterke associatie ervan met problemen met chromosoom 21, aangezien elke mutatie of een extra kopie van het chromosoom zou leiden tot de vroege ontwikkeling van de ziekte van Alzheimer, terwijl de Tau-hypothese een sterk verband suggereert tussen neurofibrillaire knopen en de ernst en progressie van de ziekte.
- Gedurende lange tijd werd de Amyloid-hypothese gezien als de primaire oorzaak die de gebeurtenissen die de ziekte van Alzheimer veroorzaken zou veroorzaken en is daarom langer onderzocht in vergelijking met de Tau-hypothese, die pas onlangs werd gezien als een primaire oorzaak en niet als een volgend resultaat van de amyloïdhypothese.
- De bèta-amyloïde pathologie wordt toegeschreven aan het veroorzaken van dementie bij patiënten; de Tau-pathologie heeft echter, naast dementie, ook effecten op gedragsveranderingen aangetoond bij patiënten die lijden aan de ziekte van Alzheimer.
- De bèta-amyloïde fibrillen worden extracellulair gezien in de vorm van plaques die zich in verschillende delen van de hersenen afzetten, terwijl de tau-klitten intracellulair aanwezig zijn in de vorm van neurofibrillaire kluwens.
- https://movementdisorders.onlinelibrary.wiley.com/doi/epdf/10.1002/mds.22594
- https://reader.elsevier.com/reader/sd/pii/S0002944017300809?token=8632CB1A71421C8D29E8BCF80F18C7897E9B686E1DAB508B6203782D87488A0C6ACAC8608FEA76A420108571CA668350&originRegion=eu-west-1&originCreation=20221101051336
Laatst bijgewerkt: 27 juli 2023

Piyush Yadav heeft de afgelopen 25 jaar als natuurkundige in de lokale gemeenschap gewerkt. Hij is een natuurkundige die gepassioneerd is om wetenschap toegankelijker te maken voor onze lezers. Hij heeft een BSc in natuurwetenschappen en een postdoctoraal diploma in milieuwetenschappen. Je kunt meer over hem lezen op zijn bio pagina.

