A doença de Alzheimer é uma doença neurodegenerativa progressiva. É uma das principais causas de demência senil. O mecanismo subjacente da doença ainda não está claro e está sujeito a mais pesquisas científicas, mas duas das hipóteses mais populares na compreensão da doença de Alzheimer são a hipótese amilóide e a hipótese Tau.
Principais lições
- Amilóide refere-se a depósitos de proteínas que formam placas no cérebro, enquanto as proteínas tau formam emaranhados neurofibrilares dentro das células cerebrais.
- Tanto a amiloide quanto a tau estão associadas à doença de Alzheimer, mas têm papéis diferentes em sua progressão.
- Os tratamentos atuais para a doença de Alzheimer visam o amilóide, mas pesquisas recentes sugerem que o direcionamento da tau pode ser mais eficaz em retardar o declínio cognitivo.
Amilóide vs Tau
Tanto a amiloide quanto a tau são depósitos anormais de proteínas encontrados no cérebro na doença de Alzheimer. Estas são proteínas insolúveis e são constituídas por fibras compactas. O amilóide é depositado fora das células cerebrais, enquanto a tau é encontrada dentro das células neuronais. A amilóide forma placas, enquanto a tau forma emaranhados.
Tabela de comparação
| Parâmetros de comparação | amilóide | Tau |
|---|---|---|
| Tipo de proteína | proteína beta-amilóide | Proteína Tau |
| Região do cérebro afetada | conexões de células cerebrais | Sinais elétricos e químicos das células cerebrais |
| Sintomas | Perda de memória | Perda de memória, alterações comportamentais |
| fator causador | Substituição da atividade da alfa-secretase pela beta-secretase. | Hiperfosforilação da proteína Tau |
| Características marcantes | Placas amilóides | Emaranhados neurofibrilares |
o que é amiloide?
A hipótese amilóide é uma das hipóteses mais pesquisadas na tentativa de encontrar tratamentos para curar a doença de Alzheimer. Normalmente, a proteína precursora da amilóide é clivada pela atividade da alfa-secretase e da gama-secretase, produzindo peptídeos solúveis inofensivos.
No entanto, mutações nos genes que codificam a proteína precursora de amiloide e a presenilina, que é um componente da gama-secretase, foram associadas a uma propensão aumentada para a formação de fragmentos de amilóide mais longos que se agregam para formar fibrilas e oligômeros.
Essas fibrilas e oligômeros são neurotóxicos e, portanto, responsáveis pela morte neuronal. Esses oligômeros também desencadeiam uma cascata de eventos que destrói ainda mais as células neuronais. Uma via é a ativação da quinase que causa a eventual hiperfosforilação da proteína Tau e resulta em mais destruição neuronal.
A hipótese amilóide é ainda reforçada pela sua associação com o início precoce da doença de Alzheimer em pessoas com Síndrome de Down. Como o gene da proteína precursora amilóide está localizado no cromossomo 21, a cópia extra do cromossomo 21st cromossomo em pessoas com Síndrome de Down provou que quaisquer problemas com o número de cromossomos ou sua mutação eram um forte fator causal para a doença de Alzheimer.
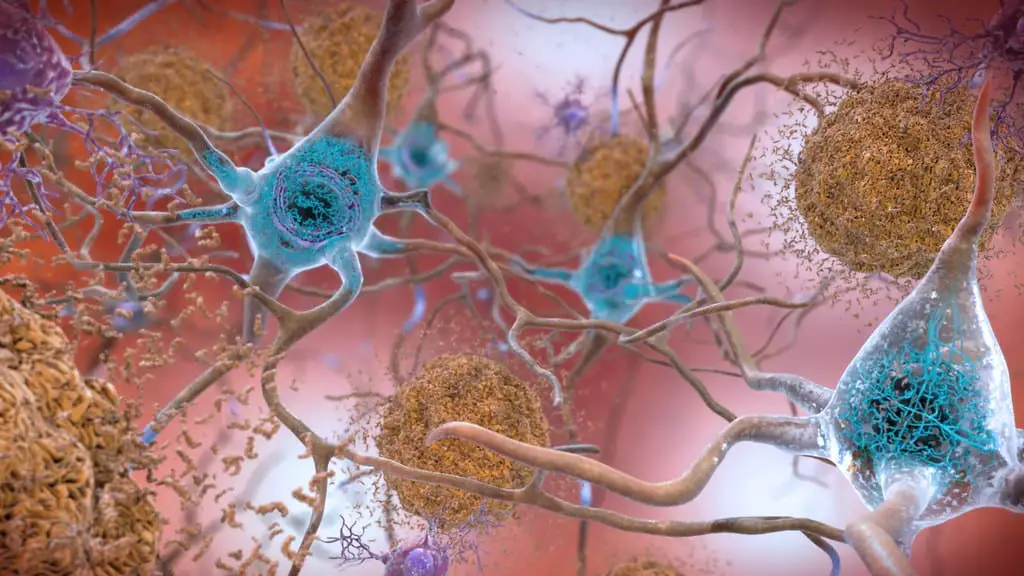
O que é Tau?
A hipótese Tau, por outro lado, é pesquisada recentemente como a principal causa da doença de Alzheimer, depois que os testes para combater a formação de proteínas beta-amilóides não produziram resultados promissores.
Além disso, emaranhados neurofibrilares devido à agregação de proteínas tau podem ser vistos em pacientes com leve demência mas sem patologia beta-amilóide. Além disso, as placas amilóides podem ser vistas em pessoas sem defeitos neurodegenerativos, no entanto, o mesmo não pode ser dito sobre aqueles com emaranhados neurofibrilares, pois a patologia da proteína Tau está intimamente correlacionada com a gravidade e progressão da doença de Alzheimer.
A hipótese Tau argumenta ainda que a patologia Tau precede qualquer patologia beta-amilóide e é a principal causa da doença de Alzheimer. A proteína Tau é responsável pela estabilidade dos microtúbulos, que mantém o transporte de nutrientes dentro das células neuronais e a integridade da estrutura celular geral.
A alteração da proteína Tau por hiperfosforilação resulta em agregações da proteína Tau em emaranhados, interrompendo os microtúbulos e interrompendo o suprimento de nutrientes e a estrutura celular, resultando em morte neuronal. Esses emaranhados podem viajar ainda mais através dos axônios e interromper outras células neuronais, resultando em uma perda funcional de partes do sistema nervoso, causando a doença de Alzheimer.
Os ensaios clínicos alvejando As proteínas tau ainda não mostraram resultados desejáveis, no entanto, a hipótese foi estudada recentemente, portanto, ainda não há dados clínicos suficientes.
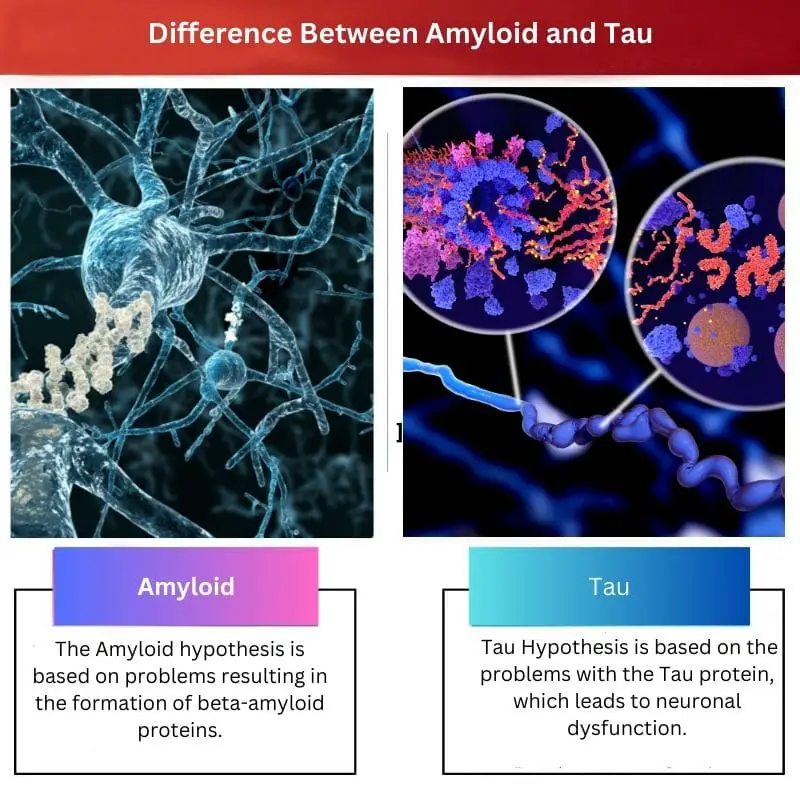
Principais diferenças entre amilóide e tau
- A hipótese amilóide é baseada em problemas que resultam na formação de proteínas beta-amilóides, que é vista como um ponto de gatilho na cascata de eventos que levam à doença de Alzheimer, enquanto a hipótese Tau é baseada nos problemas com a proteína Tau, que leva à disfunção neuronal.
- A hipótese amilóide foi baseada em sua forte associação com problemas com o cromossomo 21, já que qualquer mutação ou uma cópia extra do cromossomo levaria ao desenvolvimento precoce da doença de Alzheimer, enquanto a hipótese Tau sugere uma forte conexão de emaranhados neurofibrilares com a gravidade e progressão da doença.
- Por longos momentos, a hipótese amilóide foi vista como a causa primária que desencadearia os eventos que causavam a doença de Alzheimer e, portanto, foi pesquisada por mais tempo em comparação com a hipótese Tau, que apenas recentemente foi vista como uma causa primária e não um resultado subsequente de a hipótese amilóide.
- A patologia beta-amilóide foi atribuída a causar demência em pacientes; no entanto, a patologia Tau, além da demência, também mostrou seus efeitos nas mudanças comportamentais em pacientes que sofrem da doença de Alzheimer.
- As fibrilas beta-amilóides são vistas extracelularmente na forma de placas que se depositam em diferentes áreas do cérebro, enquanto os emaranhados tau estão presentes intracelularmente na forma de emaranhados neurofibrilares.
- https://movementdisorders.onlinelibrary.wiley.com/doi/epdf/10.1002/mds.22594
- https://reader.elsevier.com/reader/sd/pii/S0002944017300809?token=8632CB1A71421C8D29E8BCF80F18C7897E9B686E1DAB508B6203782D87488A0C6ACAC8608FEA76A420108571CA668350&originRegion=eu-west-1&originCreation=20221101051336
Última atualização: 27 de julho de 2023

Piyush Yadav passou os últimos 25 anos trabalhando como físico na comunidade local. Ele é um físico apaixonado por tornar a ciência mais acessível aos nossos leitores. Ele é bacharel em Ciências Naturais e pós-graduado em Ciências Ambientais. Você pode ler mais sobre ele em seu página bio.

