Dois tipos de reações são descritos pelas palavras endergônica e exergônica. Muitas interações químicas e biológicas ocorrem continuamente dentro e fora do corpo humano.
Este artigo usa uma tabela descritiva para distinguir as distinções fundamentais e avançadas entre as duas reações para facilitar o aprendizado e a compreensão de um iniciante e também de um entusiasta químico.
Principais lições
- As reações exergônicas liberam energia, enquanto as reações endergônicas absorvem energia de seus arredores.
- As reações exergônicas têm uma mudança de energia livre de Gibbs negativa, enquanto as reações endergônicas têm uma mudança positiva.
- As reações endergônicas são não espontâneas, enquanto as reações exergônicas são espontâneas sob determinadas condições.
Reações Exergônicas x Reações Endergônicas
Exergônico reações são reações químicas nas quais a mudança na energia livre é negativa ou há uma liberação líquida de energia livre e indica uma reação espontânea. As reações endergônicas são reações nas quais a mudança padrão na energia livre é positiva e é necessária uma força motriz para realizar isso.

Uma reação que gera energia livre é conhecida como reação 'exergônica'. Como essa reação produz energia em vez de consumi-la, ela pode acontecer sozinha, sem a intervenção de outras forças.
As reações exergônicas na bioquímica, assim como na termoquímica, são aquelas em que a variação da energia livre é negativa (menos em valor numérico).
Estas não são reações involuntárias que não são espontâneas. Para começar, eles precisam de esforço ou entrada de força – principalmente na forma de energia.
O papel comum de uma reação endergônica é liberar energia de moléculas de carboidratos ou qualquer suposta molécula de alimento, permitindo que as criaturas prosperem sem depender apenas da luz solar para obter energia.
Tabela de comparação
| Parâmetros de comparação | Reações Exergônicas | Reações endergônicas |
|---|---|---|
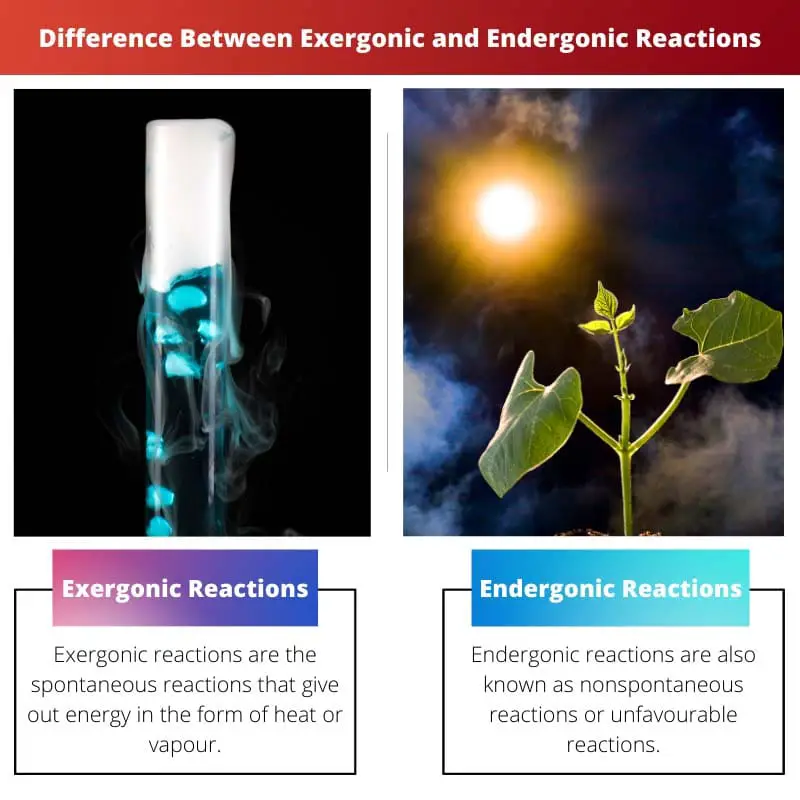
| Definição | As reações exergônicas são reações espontâneas que liberam energia na forma de calor ou vapor. | As reações endergônicas também são conhecidas como reações não espontâneas ou reações desfavoráveis. A reação requer mais energia do que você recebe |
| Energia livre de Gibbs | O valor da energia livre de Gibbs é negativo. | O valor da energia livre de Gibbs é positivo. |
| nível de entropia | O nível de entropia é aumentado em uma reação exergônica típica. | A entropia diminui em uma reação endergônica. |
| Necessidade de energia | Distribui energia na forma de calor. | Absorve energia através do ambiente para iniciar a reação ou a continuação dela. |
| Exemplos | A reação de sódio e cloro para produzir sal de cozinha, combustão e quimioluminescência. Nesta reação, a energia é liberada na forma de luz. | A reação química da fotossíntese é um bom exemplo de reações endergônicas. |
O que são reações exergônicas?
Exergônicas são reações irreversíveis que ocorrem naturalmente no ambiente. O termo “espontâneo” refere-se a algo pronto ou ansioso para ocorrer com pouca ou nenhuma estimulação externa.
Quando submetido ao oxigênio da atmosfera, o sódio, por exemplo, queima. Outro exemplo de reações exergônicas é a defumação da madeira.
Sob temperatura e pressão padrão, a energia livre de Gibbs é zero, indicando que mais calor é retirado do que absorvido. Estas são respostas que não podem ser revertidas.
Organismos vivos empregam processos exergônicos para transportar energia de “armazenamento” em um componente, como gordura ou açúcar, para um estado ativado, como ATP.
O que são reações endergônicas?
Um processo no qual calor ou qualquer forma de energia é absorvida é conhecido como reação endergônica. Isso significa que a mudança geral na energia livre é positiva em termos químicos.
Muitos processos na natureza só podem ocorrer se a energia adequada do ambiente estiver disponível.
A energia externa auxilia na dissolução dessas conexões. A energia liberada como resultado da quebra da ligação alimenta a reação.
No caso de reações endergônicas, essa energia livre de Gibbs é positiva (+), indicando que a reação não é espontânea.
Principais diferenças entre reações exergônicas e endergônicas
- Nas reações exergônicas, a entropia aumenta, enquanto nas reações endergônicas, a entropia diminui.
- A energia dos produtos de uma reação exergônica é maior que a dos reagentes, enquanto a energia dos produtos é menor que a dos reagentes no caso de reações endergônicas.
- https://www.khanacademy.org/science/biology/energy-and-enzymes/free-energy-tutorial/a/gibbs-free-energy
- https://bio.libretexts.org/Bookshelves/Introductory_and_General_Biology/Book%3A_General_Biology_(Boundless)/6%3A_Metabolism/6.2%3A_Potential_Kinetic_Free_and_Activation_Energy/6.2A%3A__Free_Energy
Última atualização: 07 de setembro de 2023

Piyush Yadav passou os últimos 25 anos trabalhando como físico na comunidade local. Ele é um físico apaixonado por tornar a ciência mais acessível aos nossos leitores. Ele é bacharel em Ciências Naturais e pós-graduado em Ciências Ambientais. Você pode ler mais sobre ele em seu página bio.


Este artigo apresenta uma análise minuciosa das reações exergônicas e endergônicas, esclarecendo sua importância nas interações químicas e biológicas.
Este artigo fornece uma explicação perspicaz e abrangente das reações exergônicas e endergônicas. A tabela de comparação e os exemplos são particularmente úteis para compreender as principais diferenças.
O artigo é muito informativo e bem estruturado. A distinção clara entre reações exergônicas e endergônicas facilita a compreensão dos conceitos pelos leitores.
A elucidação do artigo sobre reações exergônicas e endergônicas é louvável, oferecendo uma compreensão proficiente aos leitores sobre os processos químicos e biológicos que governam.
O artigo explica habilmente a dicotomia entre reações exergônicas e endergônicas, exemplificando suas implicações em vários fenômenos naturais.
A explicação do artigo sobre reações exergônicas e endergônicas é muito articulada e educativa. Os exemplos reais fornecidos servem como ilustrações práticas, contribuindo para uma melhor compreensão do conceito.
A comparação abrangente entre reações exergônicas e endergônicas é louvável, elucidando as principais disparidades com precisão e clareza.
A tabela de comparação detalhada destaca efetivamente as disparidades fundamentais entre as reações exergônicas e endergônicas, atendendo a leitores com diversos níveis de conhecimento. O uso de exemplos descritivos melhora ainda mais a compreensão.