Такие термины, как элементы и атомы, часто используются при изучении химии, а иногда и физики. Однако по мере того, как тема продвигается вперед и становится все более и более сложной, значения терминов могут легко запутаться.
Основные выводы
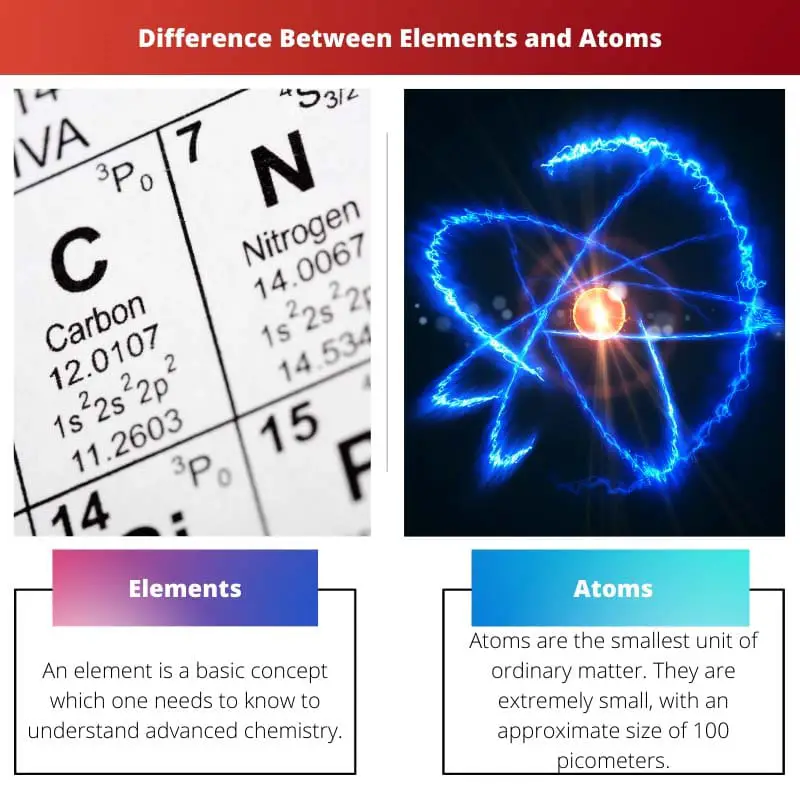
- Элементы не могут быть расщеплены на более простые вещества химическим путем. В то же время атомы являются мельчайшими частицами элемента, сохраняющими химические свойства этого элемента.
- Элементы имеют уникальные атомные номера, которые определяют их свойства и положение в периодической таблице, в то время как у атомов есть протоны, электроны и нейтроны, которые определяют их поведение и взаимодействие.
- Элементы могут объединяться, образуя соединения, но атомы одного и того же элемента не могут быть далее расщеплены без изменения химических свойств вещества.
Elements против атомов
Элементы и атомы различаются, потому что компонент — это наиболее упрощенная форма вещества, состоящего из атомов. Аспект классифицируется в зависимости от его атомного номера. Субатомные частицы объединяются, образуя атомы, которые сливаются, чтобы создать элемент. Позже элементы объединяются, образуя молекулы.

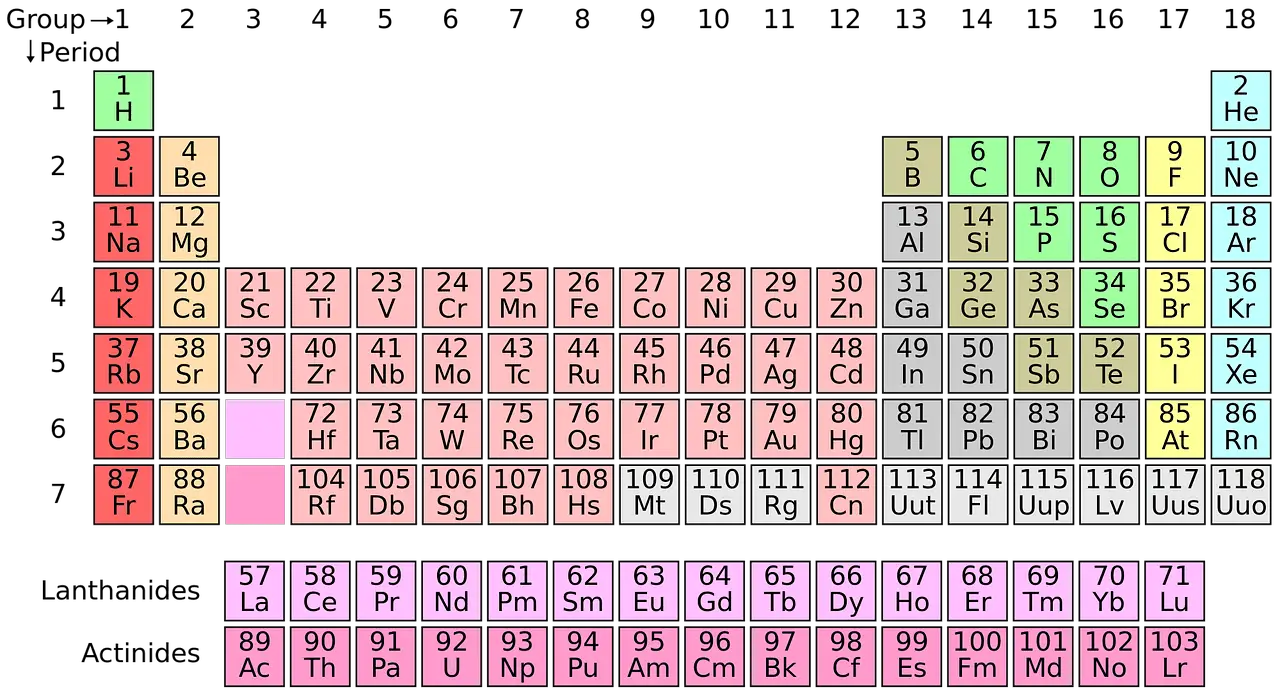
В отличие от химических соединений, химические элементы не могут быть разделены на более простые вещества никаким химическим методом. В периодической таблице элементы систематизированы по их порядковому номеру.
Атом — это мельчайшая частица обычной материи, которая создает химический элемент. Атом состоит из субатомных частиц. Проще говоря, атомы являются строительными блоками для составления элементов.
Сравнительная таблица
| Параметры сравнения | Elements | атомы |
|---|---|---|
| Размер | Больше, чем атомы | Очень маленькие (невидимы даже под микроскопом) |
| Количество типов | Всего 118 элементов. | В природе существует примерно 92 вида атомов. |
| Состав | Конкретный элемент состоит только из одного определенного типа атома. | Атомы состоят из субатомных частиц. Это протоны, электроны и нейтроны. |
| Когда они объединяются | Элементы объединяются, образуя новые химические реакции. | Когда атомы объединяются, они образуют молекулу. |
| Вес | Тяжелее отдельного атома. | Чрезвычайно легкий (относительный вес 1 AMU) |
Что такое Элементы?
Элемент — это фундаментальное понятие, которое необходимо знать, чтобы понять продвинутую химию. В своих атомных ядрах элемент состоит только из атомов, содержащих одинаковое количество протонов.
Химические элементы нельзя разделить на более простые элементы или вещества никаким химическим методом. Последнему приписывается атомный номер, представленный символ "З.'
Современная химия во многом зависит от таблицы Менделеева. Все обнаруженные элементы классифицированы и систематизированы в периодической таблице. Эта концепция была разработана Русский химик Дмитрий Менделеев в 1869 году.
Характеристики элемента отвечают за его физическое состояние при комнатной или средней температуре. Он может быть как в газообразном, так и в твердом или жидком состоянии.
Всего насчитывается около 118 типов элементов.
Вот несколько примеров элементов:
- водород
- Carbon
- Neon
- Магний
- алюминий
- Бор
Что такое атомы?
Атомы являются наименьшими единицами обычной материи. Они крошечные, приблизительный размер 100 пикометров. Кроме того, атом имеет чрезвычайно малый вес. Относительно веса последнего составляет относительно 1AMU.
Ядро состоит из одного или нескольких протонов и нескольких нейтронов. Есть только одно исключение из этого правила: водород, в котором нет нейтронов. На ядро приходится 99.94% массы атома.
Протоны обладают положительным электрическим зарядом, электроны содержат отрицательное количество электричества, а нейтроны не имеют электрического контроля. Атом электрически нейтрален, когда число протонов и электронов равно.
В природе существует 92 различных типа атомов.
Основная концепция и понятие что материя состоит из мельчайших неделимых частиц, являются древними. История атомов восходит к древним временам Индии и Греции.

Основные различия между элементами и атомами
- Когда более чем один элемент объединяется, они образуют новую химическую реакцию, в результате которой образуется новый элемент. Когда более одного атома объединяются (сохраняя различные вещества постоянными), они образуют молекулу.
- Вес элемента тяжелее по сравнению с весом атома, тогда как в случае атомов последний чрезвычайно легкий. Относительный вес последнего составляет примерно 1 АМЕ.
- https://books.google.com/books?hl=en&lr=&id=EvTI-ouH3SsC&oi=fnd&pg=PP1&dq=elements&ots=pQ5TOAfsJ3&sig=LBL5oWU1-cH9p_y8JPtdmdjok7g
- https://pubs.acs.org/doi/pdf/10.1021/ar00109a003
Последнее обновление: 11 июня 2023 г.

Пиюш Ядав последние 25 лет работал физиком в местном сообществе. Он физик, увлеченный тем, чтобы сделать науку более доступной для наших читателей. Он имеет степень бакалавра естественных наук и диплом о высшем образовании в области наук об окружающей среде. Подробнее о нем можно прочитать на его био страница.

Углубленные объяснения облегчили понимание различий между элементами и атомами, что добавило огромную образовательную ценность.
Детальное сравнение элементов и атомов оказалось полезным для обучения.
Четкое и подробное сравнение элементов и атомов облегчило понимание их различий и послужило отличным инструментом обучения.
Изучение различий между элементами и атомами из этой статьи было весьма познавательным и познавательным.
Информативность элементов и атомов сделала сравнение этих двух понятий достаточно ясным и понятным.
В этой статье представлено всестороннее и информативное детальное сравнение элементов и атомов, а также дана неоценимая информация об их характеристиках и поведении.
Я впечатлен четким сравнением различий между элементами и атомами, представленным в этой статье.
Статья имеет большое образовательное значение, особенно для тех, кто интересуется естественными науками и химией.
Это определенно ценный ресурс для всех, кто интересуется изучением элементов и атомов.
Он оказался ценным для понимания фундаментальной научной концепции элементов и атомов.
Всестороннее сравнение элементов и атомов оказалось поучительным и позволило лучше понять эти научные концепции.
Глубокое погружение в сравнение элементов и атомов предоставило ценный образовательный опыт, облегчив понимание этих научных концепций.
В этой статье удалось провести глубокое и всестороннее сравнение элементов и атомов, что очень полезно для образовательных целей и понимания научных концепций.
Образовательная ценность сравнения элементов и атомов в этой статье поистине похвальна.
Подробная информация о ключевых выводах об элементах и атомах очень полезна для лучшего понимания этих концепций.