Химия - очень интересный предмет среди всех остальных. Сюда входят связи, резонанс, яркие соединения, химические реакции и т. д.
В химии соединения порождают ионы, катионы, анионы, электроны и т. д. Главной достопримечательностью предмета является периодическая таблица, в которую входят все элементы, встречающиеся на земле, созданные естественным или искусственным путем.
Основные выводы
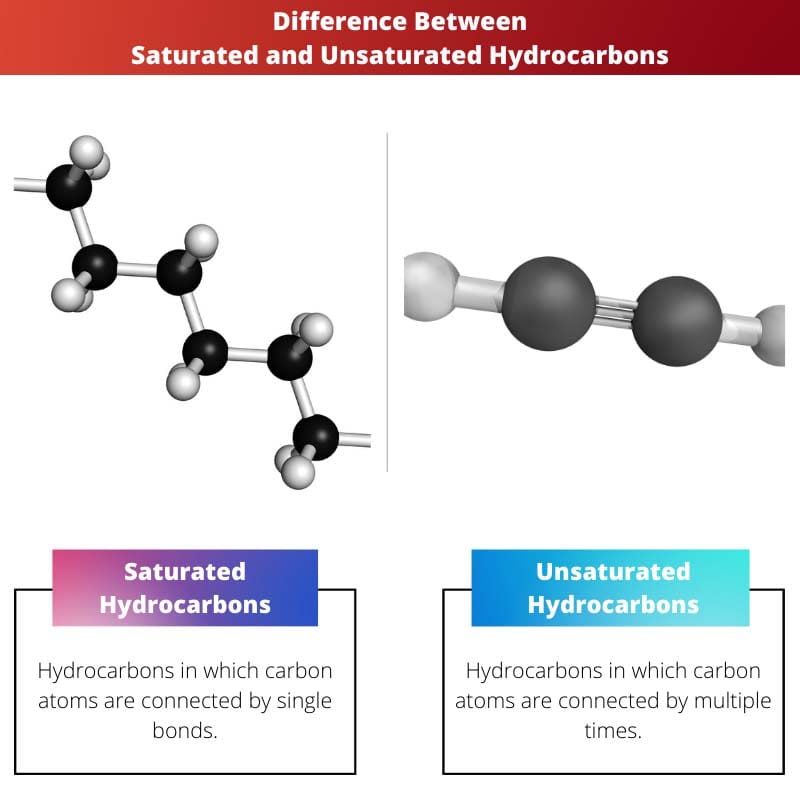
- Насыщенные углеводороды содержат одинарные связи, а ненасыщенные углеводороды содержат двойные или тройные связи.
- Насыщенные углеводороды представляют собой твердые вещества или жидкости при комнатной температуре, а ненасыщенные углеводороды — газы или жидкости.
- Насыщенные углеводороды имеют более высокую температуру плавления и кипения, чем ненасыщенные углеводороды.
Насыщенный углеводород против ненасыщенного углеводорода
Разница между насыщенным углеводородом и ненасыщенным углеводородом заключается в том, что соединение насыщенных углеводородов содержит или имеет одинарную связь между двумя атомами углерода, т. е. два разных атома углерода соединены одинарной связью между ними.

Насыщенный углеводород определяется как углеводород, состоящий только из углерода и водорода, где два атома углерода связаны одинарной связью.
Остальные связи атомов углерода заполняются атомами водорода, так что он не образует кратных связей. Алканы являются примером насыщенных углеводородов.
К соединениям алканов относятся – метан, этан, бутан, пентан, гексан и др.
Ненасыщенный углеводород определяется как углеводород, состоящий только из углерода и водорода, а две водородные связи соединены множественными связями.
Ненасыщенные углеводороды имеют два типа углеводородных соединений, и они называются алкенами и алкинами.
Примерами алкеновых соединений являются бутен, гексен, пентен, этен и т. д., а примерами алкиновых соединений являются ацетилен, окт-1-ин, 1-гексин и т. д.
Сравнительная таблица
| Параметры сравнения | Насыщенный углеводород | Ненасыщенный углеводород |
|---|---|---|
| Определение | Углеводороды, в которых атомы углерода соединены одинарными связями | Углеводороды, в которых атомы углерода соединены многократно |
| Типы углеводородов | Два типа - алканы и циклоалканы | Три типа – алкены, алкины, ароматические |
| Гибридизация | sp3 | sp2 или сп1 |
| Атомы водорода | Большее количество атомов | Меньшее количество атомов |
| Химическая реактивность | Низкий | High |
| Испытание пламенем | Дает синее пламя | Дает закопченное пламя (или цвет земли) |
| Пример | Алканы, циклоалкан, бутан, пентан | Алкины, Алкены, Ароматические, Ацетилен |
Что такое насыщенный углеводород?
Насыщенные углеводороды определяются как углеводороды, образованные двумя атомами углерода с одинарной связью между ними. Остальные связи связаны или образованы атомами водорода для выполнения валентности углерода.
Общая формула, используемая для получения насыщенного углеводорода, – CnH2n+2.
Насыщенные углеводороды бывают двух основных типов – алканы и циклоалканы. Некоторые соединения алканов – метан, этан, пропан, бутан, пентан и т.д.
Циклоалканы представляют собой соединения с кольцевой структурой наряду с гибридизированными атомами. Свойства циклоалканов почти такие же, как у алканов, за исключением температуры кипения и плавления, которые сравнительно выше.
Ниже приведены свойства или использование насыщенных углеводородов:
- Насыщенные углеводороды содержат в своих соединениях большее число атомов водорода.
- Метан — первое алкановое соединение очень полезно и может использоваться в качестве ракетного топлива или в автомобилях, обогревателях и т. д.
- Алканы и циклоалканы представляют собой два существенно разных типа насыщенных углеводородов.
- Циклоалканы могут быть использованы для производства нейлона, нефтяного газа, каучуков и др.
- Этан, второе соединение алкана, является хладагентом холодильника. Кроме того, он играет важную роль в производстве этилена.
Что такое ненасыщенный углеводород?
Ненасыщенные углеводороды определяются как углеводороды, образованные двумя атомами углерода с множественными связями между ними. Множественные связи могут быть двойными связями или тройными связями.
Позднюю валентность углерода выполняют атомы водорода. Общая формула ненасыщенного углеводорода для алкенов – CnH2n, а для алкинов – CnH2n-2.
Ненасыщенные углеводороды представлены тремя основными типами: алкены, алкины и ароматические соединения. Свойства ароматических соединений не такие, как у алкенов и алкинов.
Кроме того, эти соединения сравнительно более стабильны, чем алкены или алкины.
Ниже приведены свойства или использование ненасыщенных углеводородов:
- Чтобы образовать ненасыщенный углеводород, атомов водорода меньше, а также кратных связей (двойных или тройных связей).
- Два атома углерода, присоединенные к ненасыщенному углеводороду, образуют валентный угол около 120 градусов.
- Наиболее распространенный ароматический углеводород, бензол, образует валентный угол 120 градусов с другими атомами.
- В любой реакции, когда образуется вода или углекислый газ, происходит горение.
- Реакции окисления вызываются присоединением или вычитанием атомов водорода в реакции.
Основные различия между насыщенным и ненасыщенным углеводородомs
- Насыщенные углеводороды — это углеводороды, которые образованы атомами углерода и водорода, и два атома углерода связаны одинарной связью, тогда как, с другой стороны, ненасыщенные углеводороды — это углеводороды, которые также образованы атомами углерода и водорода и атомы углерода соединены множественными связями, и это может быть двойная связь или тройная связь.
- Насыщенные углеводороды в основном бывают двух типов: алканы и циклоалканы, тогда как, с другой стороны, ненасыщенные углеводороды в основном бывают трех типов: алкены, алкины и ароматические соединения.
- Гибридизация, проявляемая насыщенными углеводородами, представляет собой sp3, тогда как, с другой стороны, гибридизация, проявляемая ненасыщенными углеводородами, представляет собой sp2 для алкенов и sp1 или sp для алкинов.
- Наличие числа атомов водорода в насыщенных соединениях больше, в то время как сравнительно, с другой стороны, присутствие числа атомов водорода в ненасыщенных соединениях меньше.
- Химическая активность, проявляемая насыщенными соединениями, низка по сравнению с ней, с другой стороны, химическая активность, проявляемая ненасыщенными соединениями, высока.
- Тест пламени, показанный насыщенными соединениями, представляет собой голубое пламя, в то время как, с другой стороны, тест пламени, показанный ненасыщенными соединениями, представляет собой пламя копоти (или пламя цвета почвы).
- Примерами насыщенных углеводородов являются алканы, циклоалканы, бутан, гексан, октан и т. д., тогда как, с другой стороны, примерами ненасыщенных углеводородов являются ароматические соединения, алкины и алкены.
- https://www.sciencedirect.com/science/article/abs/pii/S0376738800006232
- https://pubs.acs.org/doi/abs/10.1021/ct300215p
- https://www.frontiersin.org/articles/10.3389/fchem.2014.00075/full
- https://cdnsciencepub.com/doi/abs/10.1139/v71-612
Последнее обновление: 25 июля 2023 г.

Пиюш Ядав последние 25 лет работал физиком в местном сообществе. Он физик, увлеченный тем, чтобы сделать науку более доступной для наших читателей. Он имеет степень бакалавра естественных наук и диплом о высшем образовании в области наук об окружающей среде. Подробнее о нем можно прочитать на его био страница.


Раздел об основных различиях между насыщенными и ненасыщенными углеводородами дает четкий обзор различных химических характеристик. Это полезно как для студентов, так и для специалистов.
Подробные объяснения насыщенных и ненасыщенных углеводородов и их химических свойств очень полезны. Информация здесь представлена четко и организованно.
Я нашел раздел об использовании насыщенных и ненасыщенных углеводородов особенно интересным. Интересно наблюдать, как эти соединения применяются в различных отраслях промышленности.
Абсолютно! Понимание их практического применения помогает оценить значение этих соединений в повседневной жизни.
Сравнительная таблица, представленная в статье, особенно полезна для быстрого понимания различий между насыщенными и ненасыщенными углеводородами. Отличная работа!
Хорошая статья! Он предоставляет всесторонний обзор различий между насыщенными и ненасыщенными углеводородами, что важно для понимания основ химии.
Я абсолютно согласен! В статье очень четко и лаконично объясняются понятия.
В статье дано подробное объяснение химической активности и свойств насыщенных и ненасыщенных углеводородов. Такое детальное понимание имеет решающее значение в области химии.
Я ценю подробную информацию об использовании насыщенных и ненасыщенных углеводородов. Это помогает понять практическое значение этих соединений в нашей повседневной жизни.
В этой статье подробно описаны химические свойства и различия между насыщенными и ненасыщенными углеводородами. Это отличный ресурс для студентов и всех, кто интересуется химией.
Подробные объяснения насыщенных и ненасыщенных углеводородов и их свойств очень информативны. Приятно иметь такую понятную информацию в одном месте.