Živiny obsažené v potravě nemohou být tělem okamžitě absorbovány. Je třeba je rozložit na menší části pomocí různých enzymů.
V případě bílkovin pomáhají specifické enzymy při jejich štěpení na aminokyseliny, které tělo využívá. Tyto enzymy jsou dvou typů, jmenovitě chymotrypsin a trypsin.
Key Takeaways
- Chymotrypsin je proteolytický enzym, který štěpí peptidové vazby na aromatických aminokyselinách.
- Trypsin je další proteolytický enzym, který se zaměřuje na peptidové vazby na bazických aminokyselinách.
- Oba enzymy hrají zásadní roli při trávení bílkovin v trávicím systému.
Chymotrypsin vs trypsin
Chymotrypsin je trávicí enzym, který štěpí bílkoviny na menší peptidy a aminokyseliny. Trypsin se štěpí peptid vazby na karboxylové straně esenciálních aminokyselin. Trypsin se vyrábí ve slinivce břišní a je důležitý pro trávení bílkovin v tenkém střevě.

Chymotrypsin je enzym, který v podstatě napomáhá procesu trávení štěpením bílkovin. Vylučuje se ze slinivky břišní jako složka pankreatické šťávy.
Enzym je aktivován jeho prekurzorem, který se nazývá chymotrypsinogen. Jedná se o neaktivní enzym, který funguje pouze v přítomnosti trypsinu.
Mezitím je trypsin dalším druhem trávicího enzymu, který pracuje s různými aminokyselinami. Je produkován také slinivkou břišní.
Většina jeho práce však probíhá v tenkém střevě. Jeho prekurzorem je neaktivní enzym zvaný trypsinogen. Neaktivní enzym funguje pouze v přítomnosti enterokinázy.
Srovnávací tabulka
| Parametry srovnání | Chymotrypsin | trypsin |
|---|---|---|
| objev | Byl objeven ve 1900. letech XNUMX. století. | Byl objeven v roce 1876. |
| Význam | Je to trávicí enzym, který pracuje na štěpení aromatických aminokyselin. | Je to trávicí enzym, který funguje na štěpení základních aminokyselin. |
| předchůdce | Jeho prekurzorem je neaktivní enzym zvaný chymotrypsinogen. | Jeho prekurzorem je neaktivní enzym zvaný trypsinogen. |
| Aktivace | Jeho prekurzor se aktivuje pomocí trypsinu. | Jeho prekurzor se aktivuje pomocí enterokinázy. |
| Aminokyseliny | Vybírá aminokyseliny včetně tyrosinu, tryptofanu a fenylalaninu. | Vybírá aminokyseliny včetně argininu a lysinu. |
| použití | Může být použit pro mapování peptidů, syntézu peptidů, analýzu a dokonce i otisky prstů. | Může být použit pro tkáňovou disociaci, mitochondriální izolaci a sběr buněk. |
| Inhibitory | Mezi jeho inhibitory patří benzamidin, aprotinin, DFP, EDTA, Ag+ atd. | Jeho inhibitory zahrnují boronové kyseliny, peptidylaldehydy, deriváty kumarinu atd. |
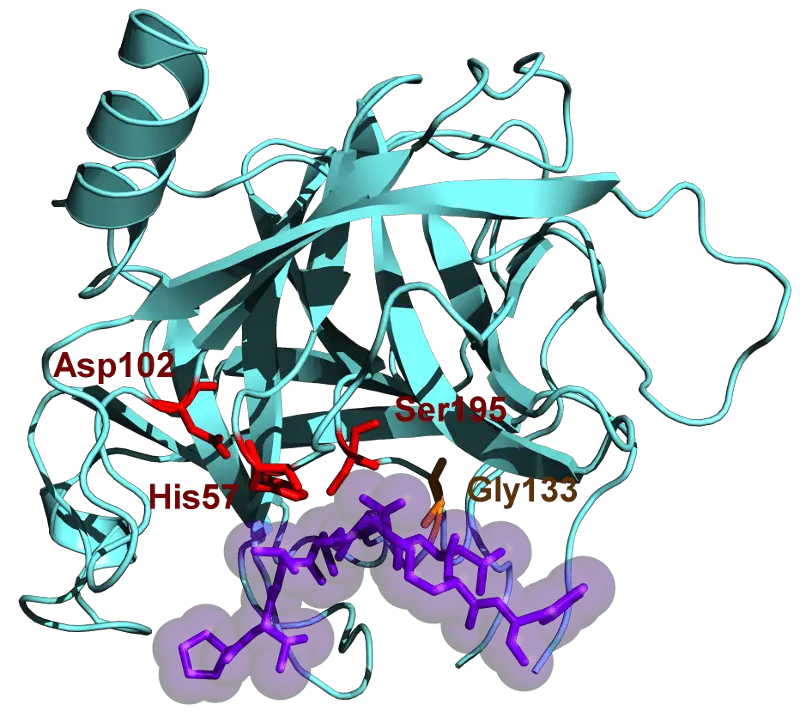
Co je Chymotrypsin?
Chymotrypsin je trávicí enzym, který byl poprvé objeven v roce 1900. Je součástí rodiny serinových proteáz a spadá do kategorie endopeptidáz.
Enzym má a molekulová hmotnost 25.6 kDa. Jeho prekurzor se nazývá chymotrypsinogen. Jedná se o neaktivní enzym, který se aktivuje pomocí trypsinu.
Když k tomu dojde, tvoří se chymotrypsin a uvolňuje se ze slinivky břišní jako složka pankreatické šťávy.
Každý enzym má v sobě aktivní místo, které je vytvořeno pro konkrétní struktury a velikosti, aby se do něj vešly. To znamená, že enzym potřebuje vybrat konkrétní aminokyseliny, které se do nich vejdou.
V případě chymotrypsinu jsou vybrány pouze aromatické aminokyseliny.
Patří mezi ně tyrosin, tryptofan a fenylalanin. Jakmile vstoupí do aktivního místa enzymu, jejich peptidové vazby se přeruší, aby mohly být stráveny.
Tyto enzymy slouží k různým účelům v lékařských studiích a studiích Vito. Používají se pro mapování peptidů, syntézu peptidů, analýzu a dokonce i otisky prstů.
Existují také určité inhibitory, které se vážou s chymotrypsinem, aby se snížila jeho aktivita. Patří mezi ně benzamidin, aprotinin, DFP, EDTA, Ag+ atd.
Nacházejí se v doplňcích, které jsou předepisovány lidem s dysfunkčními enzymy chymotrypsinu.
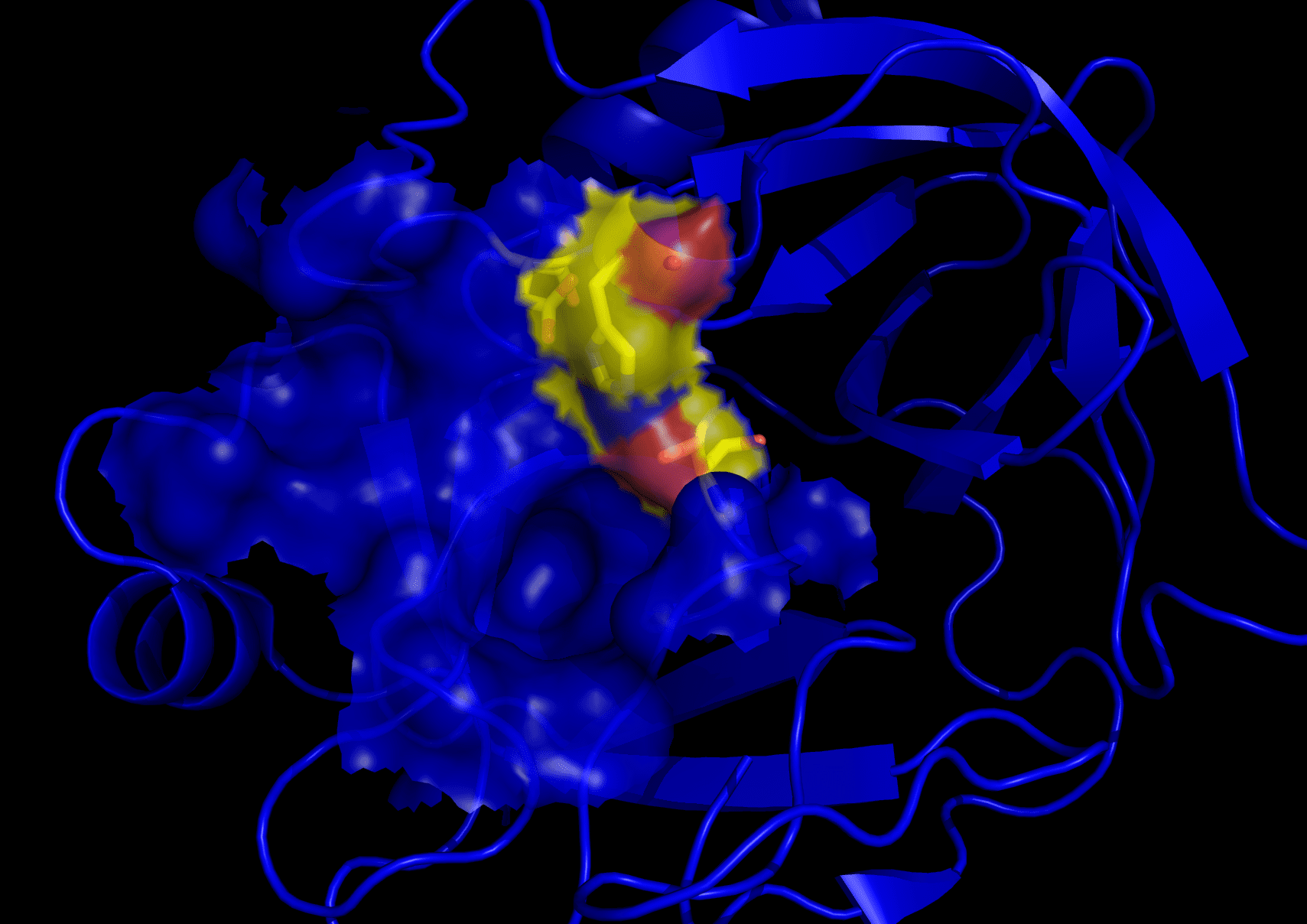
Co je Trypsin?
Trypsin je další trávicí enzym, ale byl objeven mnohem dříve, v roce 1876. Patří také do rodiny serinových proteáz, ale spadá do kategorie globulárních proteinů.
Molekulová hmotnost trypsinu je 23.3 kDa. Jeho funkcí je rušit peptidové vazby v aminokyselinách.
Enzym se uvolňuje ze slinivky břišní ze svého prekurzoru zvaného trypsinogen.
Tento neaktivní enzym přichází do kontaktu s enterokinázou za účelem aktivace. Jakmile k tomu dojde, je přenesen do tenkého střeva, kde probíhá většina jeho fungování.
Enzym pouze vybírá určité bazické aminokyseliny do svého aktivního místa. Patří mezi ně arginin a lysin.
Trypsin má různá použití při tkáňové disociaci, izolaci mitochondrií a sběru buněk. Má také několik inhibitorů, včetně boronových kyselin, peptidylaldehydů, derivátů kumarinu atd.
Ty se nacházejí v různých doplňcích, které mají četné lékařské použití.
Trypsin je dvou hlavních typů. Patří mezi ně alfa-trypsin a beta-trypsin. Každý z nich má jinou strukturu a funguje při jiném prahu tepelné stability.
Obě jejich aktivní místa však obsahují kyselinu asparagovou, histidin a serin, které pomáhají v celém procesu štěpení aminokyselin. Dělají to tak, že odštěpí C-konec, na kterém je uhlík.
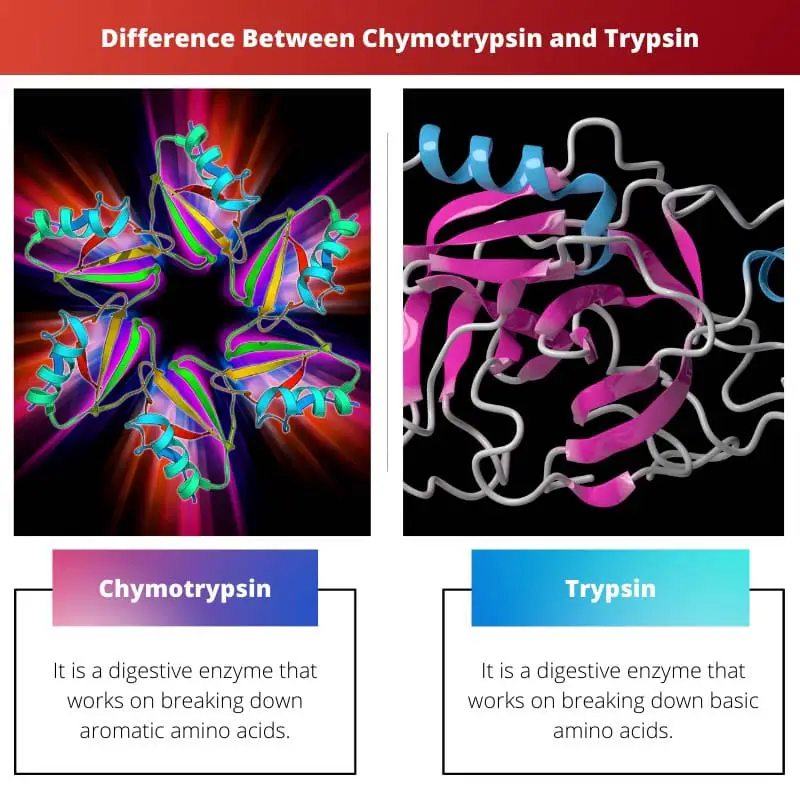
Hlavní rozdíly mezi chymotrypsinem a trypsinem
- Chymotrypsin byl objeven v roce 1900, zatímco trypsin byl objeven v roce 1876.
- Chymotrypsin je trávicí enzym, který štěpí aromatické aminokyseliny, zatímco trypsin je trávicí enzym, který štěpí základní aminokyseliny.
- Chymotrypsin vybírá aminokyseliny, včetně tyrosinu, tryptofanu a fenylalaninu, zatímco trypsin vybírá aminokyseliny, včetně argininu a lysinu.
- Projekt předchůdce chymotrypsin je neaktivní enzym zvaný chymotrypsinogen, zatímco trypsin je neaktivní enzym zvaný trypsinogen.
- Prekurzor chymotrypsinu je aktivován pomocí trypsinu, zatímco prekurzor trypsinu je aktivován pomocí enterokinázy.
- Chymotrypsin lze použít pro mapování peptidů, syntézu peptidů, analýzu a dokonce otisky prstů, zatímco trypsin lze použít pro disociaci tkání, izolaci mitochondrií a sklizeň buněk.
- Mezi inhibitory chymotrypsinu patří benzamidin, aprotinin, DFP, EDTA, Ag+ atd., zatímco inhibitory trypsinu zahrnují boronové kyseliny, peptidylaldehydy, deriváty kumarinu atd.
- https://www.sciencedirect.com/science/article/pii/0022283672900289
- https://www.sciencedirect.com/science/article/pii/0014579395014845
Poslední aktualizace: 11. června 2023

Piyush Yadav strávil posledních 25 let prací jako fyzik v místní komunitě. Je to fyzik, který je zapálený pro zpřístupnění vědy našim čtenářům. Je držitelem titulu BSc v přírodních vědách a postgraduálního diplomu v oboru environmentální vědy. Více si o něm můžete přečíst na jeho bio stránka.


Vynikající podrobné srovnání obou enzymů. Velmi informativní a dobře napsané.
Ano, je to velmi informativní článek. Dobře vysvětlené rozdíly mezi těmito dvěma enzymy.
Hodně jsem se z toho naučil. Přesné informace usnadňují pochopení.
Tento článek poskytuje skvělý pohled na chymotrypsin a trypsin. Skutečně vzdělávací.
Velmi dobře prozkoumané a informativní. Povinná četba pro každého, koho toto téma zajímá.
Tento článek mi přišel velmi poučný a jasný. Netušil jsem, že mezi těmito dvěma enzymy je takový rozdíl.
Souhlasím, velmi důkladné srovnání chymotrypsinu a trypsinu.
Ano, preciznost článku z něj dělá velmi informativní čtení.
Detailní srovnání těchto dvou trávicích enzymů je fascinující. Velmi poučné čtení.
Detailní rozpis obou enzymů je velmi jasný a užitečný!
Souhlasím, článek je dobře strukturovaný a snadno sledovatelný.
Ano, skvělý zdroj informací na toto téma.
Dobře prozkoumaný text. Děkuji za sdílení!
Děkuji za tento komplexní pohled na rozdíly mezi chymotrypsinem a trypsinem.