Υπάρχουν τόσα πολλά πράγματα στη φύση που συνδέονται μεταξύ τους για να σχηματίσουν μια νέα δομή ή μια νέα κατηγορία στοιχείων. Για παράδειγμα: Σκεφτείτε το νερό, πώς σχηματίζεται;
Σχηματίζεται με τη διαδικασία του χημικού δεσμού κατά την οποία 2 άτομα υδρογόνου και 1 άτομο οξυγόνου δεσμεύονται για να σχηματίσουν την υγρή κατάσταση του νερού. Ο χημικός δεσμός είναι σημαντικός για τους ζωντανούς οργανισμούς και την καλή λειτουργία των μερών του σώματός τους.
Βασικές τακτικές
- Οι ιονικοί δεσμοί σχηματίζονται μεταξύ μετάλλων και μη μεταλλικών στοιχείων μέσω της μεταφοράς ηλεκτρονίων, ενώ οι ομοιοπολικοί δεσμοί σχηματίζονται μεταξύ των μη μετάλλων μέσω της κοινής χρήσης ηλεκτρονίων.
- Μεταλλικοί δεσμοί συμβαίνουν μεταξύ ατόμων μετάλλου, που περιλαμβάνουν μια θάλασσα από μη εντοπισμένα ηλεκτρόνια.
- Οι ιοντικές ενώσεις έχουν υψηλά σημεία τήξης και βρασμού. Οι ομοιοπολικές ενώσεις έχουν χαμηλότερα σημεία τήξης και βρασμού και οι μεταλλικές ενώσεις έχουν ποικίλα σημεία τήξης και βρασμού.
Ionic vs Covalent vs Metallic Bonds
Μεταξύ ιόντων με αντίθετα φορτία σχηματίζονται ιονικοί δεσμοί. Αυτά τα ιόντα μπορούν να σχηματιστούν με τη μεταφορά ενός ή περισσότερων ηλεκτρονίων από το ένα άτομο στο άλλο. Οι ομοιοπολικοί δεσμοί σχηματίζονται όταν τα άτομα μοιράζονται ένα ή περισσότερα ζεύγη ηλεκτρονίων. Αυτός ο τύπος δεσμού εμφανίζεται μεταξύ δύο ατόμων μη μετάλλου. Μεταλλικοί δεσμοί σχηματίζονται μεταξύ ατόμων μετάλλων. Σε έναν μεταλλικό δεσμό, τα ηλεκτρόνια σθένους δεν εντοπίζονται σε ένα συγκεκριμένο άτομο, αλλά μάλλον είναι ελεύθερα να κινούνται σε ολόκληρο το μεταλλικό πλέγμα.

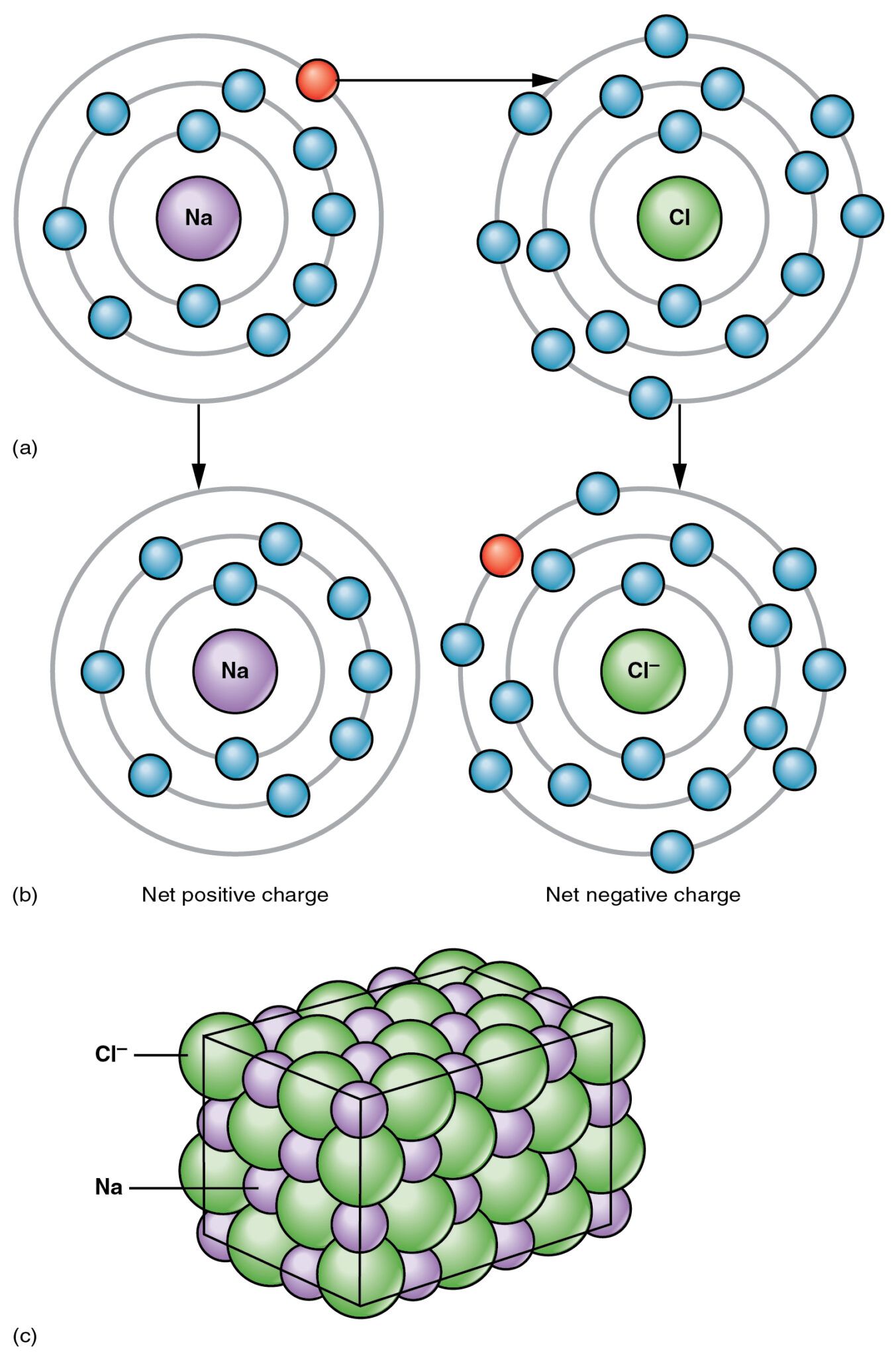
Ο ιωνικός δεσμός είναι η μεταφορά ηλεκτρονίων από ένα μεταλλικό άτομο σε ένα μη μεταλλικό άτομο, για παράδειγμα, λάβετε υπόψη το χλωριούχο νάτριο. Ο ατομικός αριθμός του νατρίου είναι 11 και η ηλεκτρονική διαμόρφωση είναι 2,8,1 Το νάτριο έχει ένα επιπλέον ηλεκτρόνιο στο εξωτερικό περίβλημά του.
Από την άλλη πλευρά, ΧλώριοΟ ατομικός αριθμός του είναι 17 και η ηλεκτρονική διαμόρφωση είναι 2,8,7 Το χλώριο έχει 7 ηλεκτρόνια στο εξωτερικό του περίβλημα, επομένως το χλώριο χρειάζεται ένα ακόμη ηλεκτρόνιο για να ολοκληρώσει την ακραία στιβάδα του, ώστε όλα τα άτομα να είναι σταθερά.
Καθώς το νάτριο έχει ένα επιπλέον ηλεκτρόνιο όταν το νάτριο αντιδρά με τη χορίνη, το νάτριο δίνει αυτό το επιπλέον ηλεκτρόνιο στη Χορίνη. Σε αυτή τη διαδικασία, το νάτριο γίνεται θετικά φορτισμένα ιόντα (Na+) και μετά την αποδοχή του ηλεκτρονίου η χορίνη γίνεται αρνητικά φορτισμένα ιόντα (Cl-).
Αυτά τα δύο αντίθετα φορτισμένα ιόντα συγκρατούνται από μια ισχυρή ηλεκτροστατική δύναμη έλξης γνωστή ως Ιωνικός Δεσμός.
A Ομοιοπολικό δεσμό σχηματίζεται όταν δύο ή περισσότερα άτομα ενώνονται μεταξύ τους με αμοιβαία κοινή χρήση ηλεκτρονίων. Για παράδειγμα, λαμβάνοντας υπόψη το σχηματισμό αερίου οξυγόνου (O2) θα πάρουμε 2 άτομα οξυγόνου καθώς γνωρίζουμε ότι ο αριθμός του ηλεκτρονίου στο Οξυγόνο είναι 8 και υπάρχουν 6 ηλεκτρόνια σθένους στο εξωτερικό περίβλημα.
Όταν αυτά τα δύο εξωτερικά κελύφη σθένους που περιέχουν 6 ηλεκτρόνια οξυγόνου λάβουν άλλα 2 ηλεκτρόνια, θα είναι σταθερά, καθώς θα εκπληρωθεί ο κανόνας της Οκτάδας.
Για να σταθεροποιηθούν αυτά τα δύο άτομα οξυγόνου συνδυάζονται και μοιράζονται δύο άτομα οξυγόνου αμοιβαία για να σχηματίσουν αέριο οξυγόνο, αυτό ονομάζεται ομοιοπολικός δεσμός.
Μεταλλικός δεσμός είναι η ηλεκτροστατική έλξη μεταξύ μεταλλικών ιόντων που είναι διατεταγμένα σε μια δομή πλέγματος (κανονικό επαναλαμβανόμενο σχέδιο) και της ελεύθερης αιώρησης ηλεκτρονίων γύρω τους.
Σε μια μεταλλική δομή, υπάρχουν μόνο ιόντα μετάλλων, αυτά τα μεταλλικά ιόντα είναι διατεταγμένα το ένα δίπλα στο άλλο σε ένα κανονικό επαναλαμβανόμενο σχέδιο και τα ελεύθερα αιωρούμενα ηλεκτρόνια λειτουργούν ως κόλλα και συγκρατούν τη δομή στη θέση του.
Αυτό είναι μια πολύ ισχυρή έλξη, επομένως το σημείο τήξης και το σημείο βρασμού των μετάλλων είναι πολύ υψηλά. Τα ελεύθερα ηλεκτρόνια είναι οι λόγοι που το μέταλλο είναι καλός αγωγός του ηλεκτρισμού.
Συγκριτικός πίνακας
| Παράμετροι σύγκρισης | Ιοντικός δεσμός | Ομοιοπολικό δεσμό | Μεταλλικός δεσμός |
|---|---|---|---|
| Σχηματισμός | Μεταλλικά και μη | Δύο μη μεταλλικά | Φορτίζει θετικά άτομα και ελεύθερα ηλεκτρόνια |
| Πολικότητα | Ψηλά | Χαμηλός | Μη πολικό |
| Σχήμα Μορίου | Χωρίς συγκεκριμένο σχήμα, δομή πλέγματος | Ορισμένο σχήμα | Χωρίς συγκεκριμένο σχήμα |
| Παραδείγματα | Χλωριούχο Νάτριο, Θειικό Οξύ | Μεθάνιο, Υδροχορικό Οξύ | Νάτριο, Μαγνήσιο |
| Σημείο τήξης | Υψηλό σημείο τήξης | Χαμηλό σημείο τήξης | Υψηλό σημείο τήξης |
Τι είναι ο Ιωνικός Δεσμός;
Ο ιοντικός δεσμός λαμβάνει χώρα όταν υπάρχει απόκτηση και απώλεια ηλεκτρονίων μεταξύ ενός μετάλλου και ενός μη μετάλλου, για να πραγματοποιηθεί ένας ιωνικός δεσμός θα πρέπει να υπάρχει τουλάχιστον ένα μέταλλο.
Για παράδειγμα, ένα άτομο μαγνησίου έχασε δύο ηλεκτρόνια και σχημάτισε ιόντα μαγνησίου που είναι θετικά φορτισμένα και είναι ιόντα μετάλλου. Από την άλλη πλευρά, το άτομο οξυγόνου αποκτά δύο ηλεκτρόνια και γίνεται αρνητικά φορτισμένα ιόντα οξειδίου και είναι αμέταλλο.
Αυτά τα δύο άτομα έλκονται μεταξύ τους καθώς το ένα είναι θετικό και το άλλο αρνητικό και αυτή η έλξη ονομάζεται Ιωνικός Δεσμός.
Τι είναι ο ομοιοπολικός δεσμός;
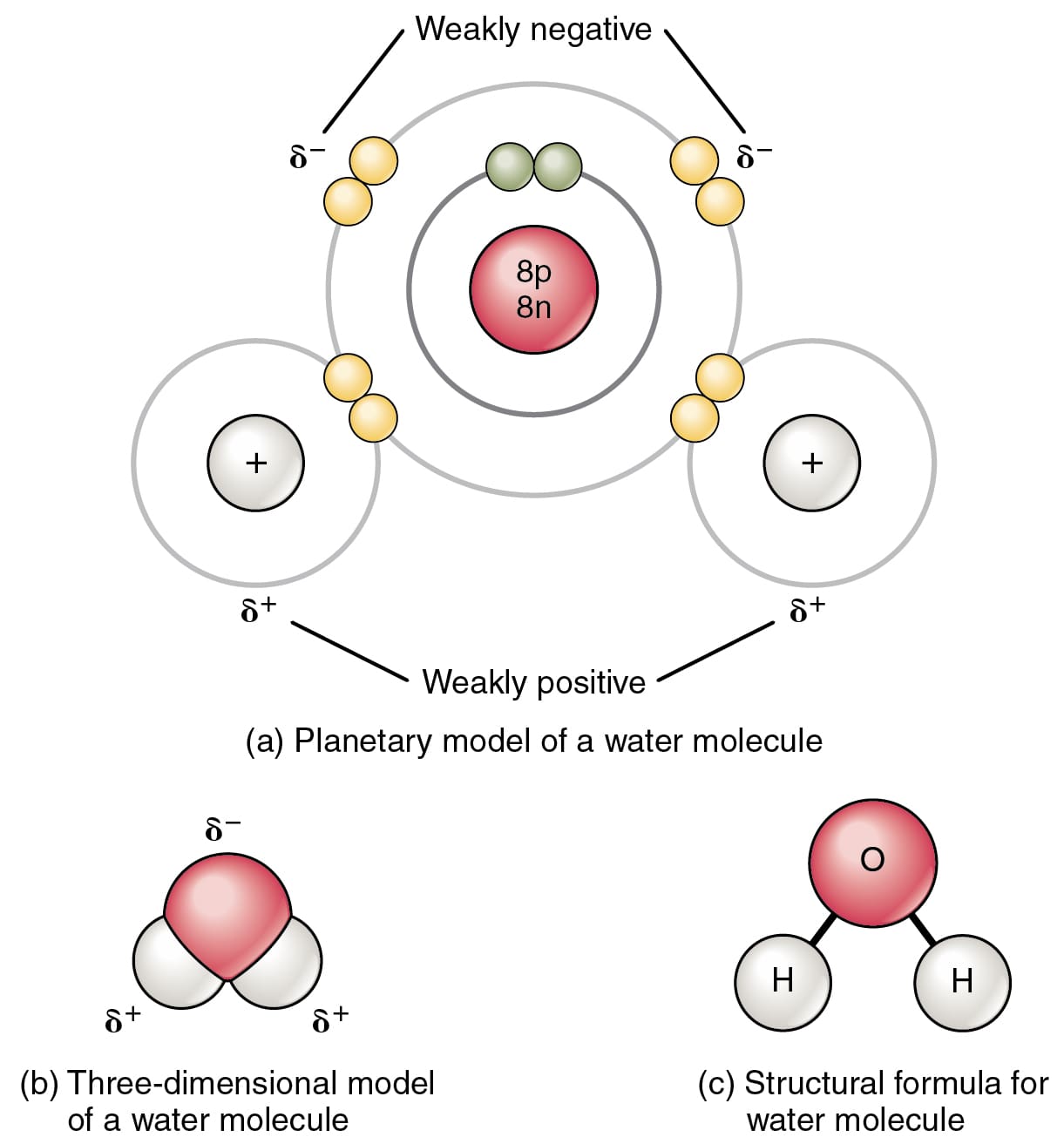
Ο ομοιοπολικός δεσμός λαμβάνει χώρα μόνο στα μη μέταλλα, δεν μπορεί ποτέ να πραγματοποιηθεί με τα μέταλλα, συμβαίνει όταν δύο ή περισσότερα από δύο αμέταλλα μοιράζονται ένα ζεύγος ηλεκτρονίων αμοιβαία.
Για παράδειγμα, έχουμε δύο άτομα χλωρίου και τα εξωτερικά κελύφη αυτών των ατόμων χλωρίου επικαλύπτονται και μοιράζονται ένα ζεύγος ηλεκτρονίων για να σχηματίσουν ένα στοιχείο.
Τα δύο άτομα ενώνονται μεταξύ τους που σχηματίζει έναν πολύ ισχυρό δεσμό που τα συγκρατεί. Αυτός ο τύπος δεσμού ονομάζεται ομοιοπολικός δεσμός.
Τι είναι ένας μεταλλικός δεσμός;
Εμφανίζεται μεταλλικός δεσμός μεταξύ των μετάλλων, τα μέταλλα χάνουν ηλεκτρόνια για να σχηματίσουν θετικά ιόντα και τα χαλαρά ηλεκτρόνια γίνονται αποτοπισμένα ηλεκτρόνια, πράγμα που σημαίνει ότι δεν είναι πλέον προσκολλημένα σε κανένα ιόν και επιπλέουν σε μια θάλασσα από μη εντοπισμένα ηλεκτρόνια.
Καθώς τα ιόντα είναι θετικά και τα αποτοποθετημένα ηλεκτρόνια είναι αρνητικά, θα υπάρχει μια έλξη μεταξύ τους. Η ηλεκτροστατική έλξη μεταξύ θετικών ιόντων και αρνητικών μη εντοπισμένων ηλεκτρονίων ονομάζεται Μεταλλικός Δεσμός.
Κύριες διαφορές μεταξύ ιοντικών, ομοιοπολικών και μεταλλικών δεσμών
- Στον ιοντικό δεσμό ένα άτομο παρέχει ηλεκτρόνια σε ένα άλλο, στον ομοιοπολικό δεσμό δύο άτομα ανταλλάσσουν ηλεκτρόνια σθένους, ενώ σε έναν μεταλλικό δεσμό το μεταλλικό πλέγμα περιλαμβάνει άτομα που μοιράζονται πολλά ηλεκτρόνια.
- Στο Ιωνικό Ενέργεια δεσμών ενός δεσμού είναι υψηλότερο από αυτό ενός μεταλλικού δεσμού, το ίδιο συμβαίνει και με τον ομοιοπολικό δεσμό, ενώ στον μεταλλικό δεσμό υπάρχει λιγότερη ενέργεια δεσμού από ό,τι σε άλλους πρωτεύοντες δεσμούς.
- Ο ιωνικός δεσμός είναι ένας αδύναμος αγωγός από την άλλη πλευρά, ο ομοιοπολικός δεσμός είναι ένας πολύ αδύναμος αγωγός, ενώ ο μεταλλικός δεσμός είναι ένας ισχυρός αγωγός.
- Ο ιωνικός δεσμός μπορεί να είναι σε στερεή κατάσταση, ο ομοιοπολικός δεσμός μπορεί να είναι σε στερεή, υγρή και αέρια κατάσταση, ενώ οι μεταλλικοί δεσμοί μπορούν να είναι μόνο σε στερεή κατάσταση.
- Ο ιωνικός δεσμός δεν έχει εύπλαστο χαρακτηριστικό το ίδιο συμβαίνει και με τον ομοιοπολικό δεσμό, ενώ ο μεταλλικός δεσμός έχει ένα εύπλαστο χαρακτηριστικό
- https://journals.aps.org/pr/abstract/10.1103/PhysRev.171.701
- https://www.tandfonline.com/doi/abs/10.1080/00150199208019535
Τελευταία ενημέρωση: 02 Ιουλίου, 2023

Ο Piyush Yadav έχει περάσει τα τελευταία 25 χρόνια δουλεύοντας ως φυσικός στην τοπική κοινότητα. Είναι ένας φυσικός που θέλει να κάνει την επιστήμη πιο προσιτή στους αναγνώστες μας. Είναι κάτοχος πτυχίου Φυσικών Επιστημών και Μεταπτυχιακού Διπλώματος στην Επιστήμη του Περιβάλλοντος. Μπορείτε να διαβάσετε περισσότερα για αυτόν στο δικό του βιο σελίδα.


Η πολυπλοκότητα των αλληλεπιδράσεων μεταξύ των διαφορετικών τύπων δεσμών είναι απολύτως συναρπαστική.
Αυτό το άρθρο έχει σίγουρα αυξήσει τις γνώσεις μου σχετικά με τους ιοντικούς, τους ομοιοπολικούς και τους μεταλλικούς δεσμούς. Ο συγγραφέας έχει κάνει φανταστική δουλειά στην παρουσίαση των πληροφοριών.
Η εξήγηση του τρόπου με τον οποίο τα άτομα συνδέονται μεταξύ τους για να σχηματίσουν διαφορετικούς τύπους δεσμών είναι καλά επεξηγημένη. Πολύ καλή δουλειά σε αυτό το άρθρο!
Το άρθρο είναι ξεκάθαρα γραμμένο και υπάρχουν τόσες πολύτιμες πληροφορίες εδώ. Εκτιμώ τον πίνακα σύγκρισης, θέτει πραγματικά τα πράγματα σε μια προοπτική.
Ο συγκριτικός πίνακας είναι πράγματι πολύ χρήσιμος και συνοπτικός.
Είναι προφανές ότι ο συγγραφέας κατανοεί καλά το θέμα και έχει επικοινωνήσει αποτελεσματικά αυτές τις αρχές.
Αυτό είναι ένα πολύ κατατοπιστικό άρθρο. Εξηγεί ξεκάθαρα τις διαφορές μεταξύ ιοντικών, ομοιοπολικών και μεταλλικών δεσμών και αποτελεί εξαιρετική αναφορά για όποιον σπουδάζει χημεία.
Σύμφωνος! Παρέχει μια ολοκληρωμένη επισκόπηση του θέματος.
Πιστεύω ότι αυτό το άρθρο θα είναι πολύ ωφέλιμο για τους μαθητές στον τομέα της χημείας.
Αυτή η εξήγηση είναι απίστευτα εμπεριστατωμένη και διορατική. Νιώθω σαν να έχω μάθει πραγματικά κάτι.