原子は鉱物の結晶を含むすべての物質を構成しています。 電子、陽子、中性子がすべての原子を構成しています。
ダルトンの原子理論は、物質、化学反応、化学について多くのことを明らかにしました。 それにもかかわらず、ダルトンの信念に反して、原子はより小さな亜原子粒子やサブユニットに分解できるため、これは真実ではありませんでした。
主要な取り組み
- 電子は、原子核の周りの電子雲に見られる負に帯電した亜原子粒子であり、陽子は原子核に見られる正に帯電した粒子です。
- 中性子は、陽子とともに原子核にも見られる非荷電粒子です。
- 陽子と中性子は同じような質量を持ちますが、電子は陽子や中性子よりもはるかに小さい質量を持ちます。
電子対陽子対中性子
電子、陽子、中性子の違いは、それらが運ぶ電荷です。 電子はマイナスに帯電し、陽子はマイナスに帯電しますが、中性子は電荷を持ちません。 むしろ彼らは中立です。 陽子、電子、中性子は、原子を構成する素粒子です。

電子は負の電荷を持っています。 電子の記号は (e–) です。 電子の原子質量単位は (5.45×10–4) です。 電子の軌道は、 核 原子の。
比較すると、電子の重さは関係ありません。 電子は、化学反応だけでなく、核プロセスでも役割を果たします。
陽子は正電荷を持っています。 (p+) は陽子の記号です。 陽子の原子質量単位は 1 です。陽子は原子核内にあります。 陽子の質量は (1.672×10–27 kg) です。 陽子は、核内で起こるプロセスにのみ関与しています。
中性子は、中性に帯電しているか帯電していないかのいずれかです。 中性子の記号は (n⁰) です。 中性子の原子質量単位は XNUMX です。 中性子は、水素を除いて原子核の内部にも存在します。 中性子は陽子よりもいくらか大きな質量を持っています。 中性子は核反応にのみ関与します。
比較表
| 比較のパラメータ | 電子 | Proton | 中性子 |
|---|---|---|---|
| 料金 | 負 | ポジティブ | 普通 |
| として記号化 | e- | p+ | n⁰ |
| 原子質量 | 5.45×10^-4 | 1 | 1 |
会場 | 核の境界の外側。 | 原子核の内部。 | 核内では、水素は例外です。 |
| 重量 | 重要ではありません。 | 1.672×10^–27kg | 陽子以上。 |
| 関係する反応 | 核反応と化学反応の両方。 | 核反応 | 核反応 |
電子とは何ですか?
電子は、より単純でより小さい粒子で構成されています。 それらはレプトンと呼ばれ、素粒子の一種です。 電子の電荷は 1 で、陽子の電荷と同じですが、負の性質を持っています。
電子は非常に小さい粒子です。 電子は非常に軽く、その重さは中性子と陽子の約 0.5×10^-3 の重さです。
全体の質量を計算する場合、それらは無視できると見なされます。 原子は、正電荷と中性に帯電した粒子の同数を構成し、全体の重量に寄与します。
負に帯電した電子は宇宙に見られます。 (e–) は電子を表します。 電子の質量は (5.45×10–4) 原子質量単位。 軌道では、電子は原子核の外側にあります。
比較するとき、電子の重さは関係ありません。 核反応と化学反応の両方で、電子が役割を果たします。

プロトンとは?
陽子は中性子とともに原子核の内部にあるため、核子と呼ばれます。 それらは両方とも一緒になって、原子の質量に寄与します。
原子核には陽子が含まれています。 (1.672×10–27 kg) は陽子の質量です。 核内で起こるプロセスだけが陽子を伴います。
原子を構成する XNUMX つの一次粒子のうちの XNUMX つです。 陽子は原子核の中に存在します。 これは、原子の中心にある小さくて密度の高い領域です。 陽子は正の電荷を XNUMX つ持ち、XNUMX 原子質量単位 (AMU) の質量も持ちます。
中性子と組み合わせると、原子の質量のほぼすべてを占めます。 正電荷は陽子を意味します。 (p+) はプロトンを表します。 1 は陽子の原子質量単位です。

Neutronとは何ですか?
ほとんどの水素原子を除くすべての原子は、原子核に中性子を持っています。 中性子は電荷を持たず、電荷を帯びている陽子や電子とは異なり、電気的に中性です。
このため、上の図の中性子は n0 と呼ばれます。 「ゼロ料金」はゼロで表されます。 文字 (n⁰) は中性子を表します。
XNUMXつは中性子の原子質量単位です。 原子核には、水素以外の中性子も含まれています。 中性子は質量の点で陽子よりも少し有利です。 核プロセスのみが中性子を伴います。 中性子の電荷は中性またはゼロです。
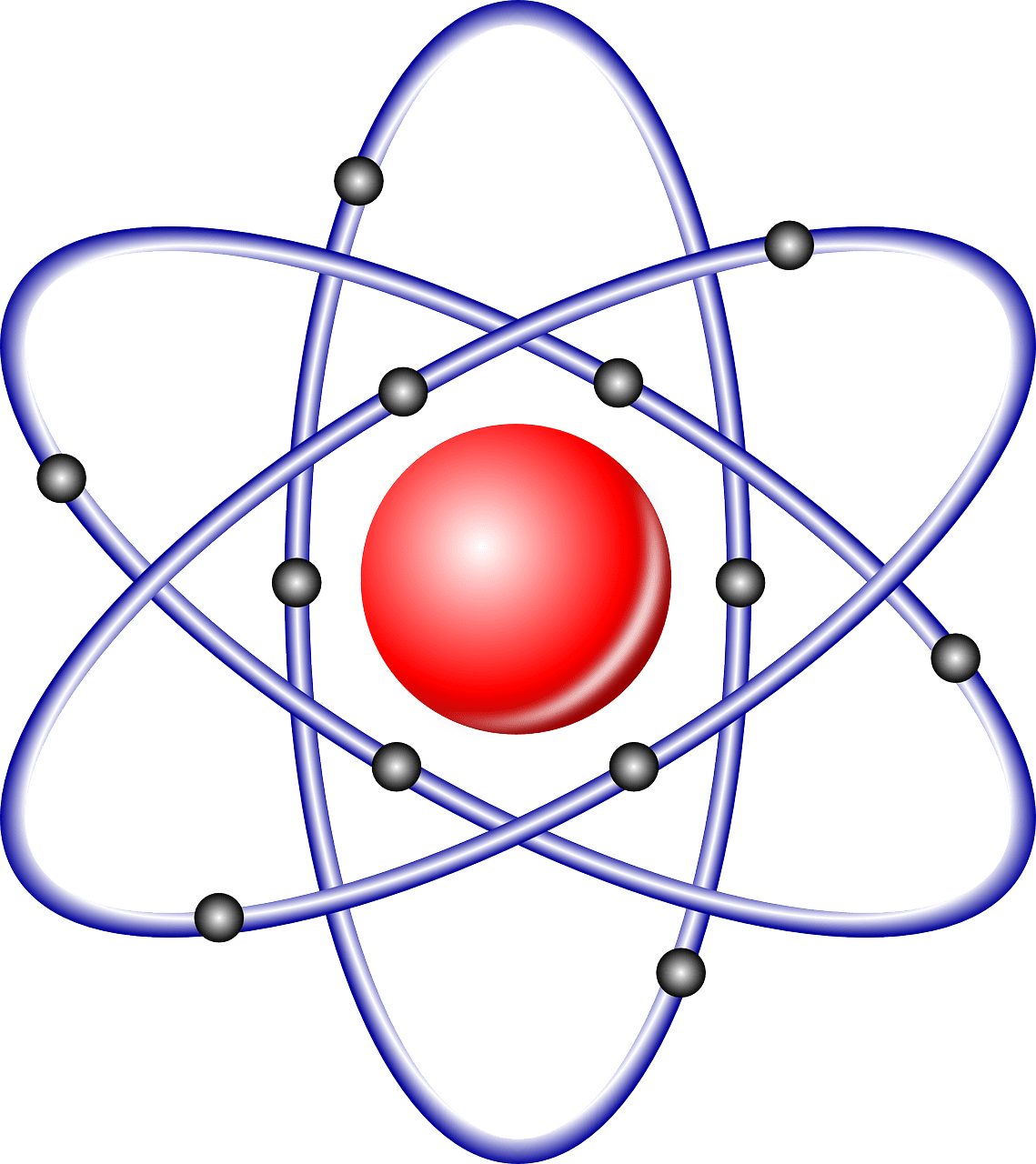
電子、陽子、中性子の主な違い
- 電子は負に帯電しています。 ただし、プロトンはプラスに帯電しています。 一方、中性子は中性に帯電しているか、電荷を持っていません。
- 電子は (e–) で表されます。 ただし、陽子は (p+) として記号化されます。 一方、中性子は (n⁰) で表されます。
- 電子の原子質量単位は (5.45×10^–4) です。 ただし、陽子の原子質量単位は1です。一方、中性子の原子質量単位はXNUMXです。
- 電子は、軌道上の原子核の境界の外側に位置しています。 しかし、陽子は原子核の中にあります。 一方、中性子は原子核の内部にもありますが、水素は例外です。
- 比較が行われる場合、電子の重量は重要ではありません。 しかし、陽子の重さは (1.672×10^–27 kg) です。 一方、中性子の重さは陽子より少し重いです。
- 電子は、核反応と化学反応の両方に関与しています。 ただし、陽子は核内でのみ発生する反応に関与します。 一方、中性子は核反応のみに参加します。
- https://www.nature.com/articles/184892a0
- https://ieeexplore.ieee.org/abstract/document/9050475/
- https://journals.aps.org/pr/abstract/10.1103/PhysRev.129.2566
最終更新日 : 31 年 2023 月 XNUMX 日

Piyush Yadav は、過去 25 年間、地元のコミュニティで物理学者として働いてきました。 彼は、読者が科学をより身近なものにすることに情熱を傾ける物理学者です。 自然科学の学士号と環境科学の大学院卒業証書を取得しています。 彼の詳細については、彼のウェブサイトで読むことができます バイオページ.

この記事の電子、陽子、中性子の区別に関する包括的な説明は、本当に啓発的です。この知識は科学分野に興味がある人にとって基礎的なものです。
これらの亜原子粒子の明確な図は、原子や物質内でのそれらの役割を理解するのに大いに役立ちます。
私はこれ以上同意できませんでした。この記事は、原子構造の領域を詳しく調べる人にとって貴重なリソースです。
この記事では、電子、陽子、中性子の包括的で有益な分析を提供します。それが提供する深い理解は、科学の分野に興味がある人にとって本当に貴重です。
この記事に示されている詳細な比較表により、電子、陽子、中性子の違いについての理解が大幅に深まりました。提供されるコンテンツは啓発的で教育的です。
私も同じ気持ちです。この記事では、これらの重要な素粒子に関する豊富な知識と明確な説明を提供します。
電子、陽子、中性子の区別の明確な説明は非常に高く評価されます。これらの粒子を理解することは、原子や物質の組成を理解する上で不可欠です。
この記事は、電子、陽子、中性子の複雑な詳細を効果的に伝えます。
私も全く同感です。素粒子に関する包括的な知識を持つことは、さまざまな科学分野において基礎となります。
電子、陽子、中性子の区別は、原子の構造と物質の挙動を理解する上で中心となります。
原子粒子とその相互作用の驚くべき複雑さは、科学者や研究者を魅了し続けています。
原子は現実の構成要素であり、その構成要素の研究は自然界を理解するために不可欠です。
この記事の電子、陽子、中性子の詳細な分解は本当に注目に値します。この包括的な理解は、さまざまな科学分野において不可欠です。
この記事は、原子構造の複雑な性質を理解しようとする人にとって貴重なリソースとして役立ちます。
絶対に。この記事で共有された洞察は、原子粒子についての深い理解を促進するために重要です。
電子、陽子、中性子の特性は、物質の最も基本的なレベルでの特性と挙動を示します。
原子内で作用する力のシンフォニーは、電子、陽子、中性子の相互作用によって美しく調整されます。
原子構造と素粒子の探求により、物理宇宙に対する私たちの理解が再形成されました。
電子、陽子、中性子の属性と挙動は化学と物理学の核心であり、物質とエネルギーの原理を動かします。
亜原子領域は宇宙の深遠な謎への鍵を握っており、それに関する私たちの研究は驚くべき洞察をもたらし続けています。
電子、陽子、中性子は原子の構造内で異なる役割と特性を持ち、それらの化学的および物理的特性に影響を与えます。
原子内の素粒子の相互作用により、私たちの世界の基礎を形成する多様な元素や化合物が生まれます。
電子、陽子、中性子の電荷と質量は、宇宙の物質の複雑さと豊かさを生み出します。
電子、陽子、中性子の違いは電荷にあります。電子はマイナスに帯電しますが、陽子はプラスに帯電し、中性子は中性です。
電子、陽子、中性子の電荷は、原子の挙動と原子間の相互作用に重要な影響を及ぼします。
電子、陽子、中性子の基本的な違いについて教えていただきありがとうございます。この情報は、物質の基本的な構成要素を理解する上で非常に重要です。
私はこれ以上同意できませんでした。この記事では、これらの素粒子について簡潔に説明しました。
この情報は、学生や化学の分野に興味がある人にとって非常に貴重です。
原子を形成する素粒子に関する発見は、私たちの科学的知識と技術的能力に革命をもたらしました。
電子、陽子、中性子が織りなす亜原子のタペストリーは、自然界の複雑な構造とその創造力を明らかにします。
この記事では、電子、陽子、中性子について徹底的かつわかりやすく概要を説明しました。それらの違いを詳しく説明することで、原子の構造についての理解が深まりました。
この記事で共有される洞察は、原子理論をより深く理解したい人にとって不可欠です。
この比較表は、これらの素粒子間の相違を強調するのに特に役立つことがわかりました。
この記事で電子、陽子、中性子を徹底的に解説することは、原子粒子についての理解を深める上で非常に貴重です。情報の明瞭さと深さは格別です。
これらの素粒子間の違いを明確に説明することは、本当に啓発的であり、非常に有益です。
絶対に。この論文は、素粒子の複雑な性質を解明することに成功しました。
ダルトンの原子理論は物質と化学反応の理解において大きな進歩でしたが、現代科学は原子の成分についてさらに詳しい情報を明らかにしました。
原子の成分とその挙動に関する発見は、化学と物理科学に新たな境地を切り開きました。
原子は本当に魅力的な構造であり、その謎を解明することは、何世紀にもわたって科学者にとって素晴らしい旅でした。
この記事での電子、陽子、中性子の明快な説明は、原子の構造を包括的に理解しようとする人にとって非常に貴重です。このリソースは豊富な知識を提供します。
これらの素粒子の詳細な比較は実に啓発的であり、物質の複雑な組成を理解するのに役立ちます。
私はこれ以上同意できませんでした。この記事の豊富な情報は、原子理論の領域を深く掘り下げる人にとって不可欠です。
電子、陽子、中性子の電荷と質量は、原子の特性と挙動を理解する上で重要な要素です。
原子内の正および負に帯電した粒子の対称的な配置は、その安定性と反応性に不可欠です。
原子の基本粒子である電子、陽子、中性子は、物理世界とその無数の現象に対する私たちの理解を支えています。
原子の構造とダイナミクスは、私たちが認識する宇宙を形作る基礎的なメカニズムへの窓を提供します。
この記事が電子、陽子、中性子の区別を明確に示していることは賞賛に値します。この詳細な情報により、物質と原子の基礎についての理解が深まります。
これ以上うまく言えませんでした。この記事で共有された洞察は本当に啓発的です。
この記事は、素粒子に関する正確な知識を求める人にとって貴重なリソースとして役立ちます。
原子を構成する素粒子は電子、陽子、中性子です。これらの粒子は異なる電荷を持ち、原子内の異なる場所に存在します。
電子、陽子、中性子は、原子の最も基本的な構成要素の一部です。それらの特性と特徴は、物理世界を理解するための基礎となります。
ダルトンの原子理論は当時画期的なものでしたが、さらなる研究により、原子は実際により小さな亜原子粒子に分解できることが示されました。