熱力学は、行われた仕事と熱を扱う化学の分野です。 特に二人の関係。
この関係は、進行中の化学反応中または変化したときに確立されます。 それは、反応物と生成物の物理的状態に見られます。
反応の実際的な計算に限定されるだけでなく、それに関連する数学的関係と計算も含まれます。
主要な取り組み
- 等張液は細胞内と同じ濃度の溶質を持ち、平衡はバランスの状態を指します。
- アイソトニック ソリューションはセルの形状とサイズを維持するのに役立ちますが、Equilibrium は化学反応における反応物と生成物のバランスを維持するのに役立ちます。
- 等張液の例は生理食塩水であり、平衡の例は CO2 と H2O が反応して炭酸を形成する場合です。
等張液対平衡
等張液は、濃度勾配が半透膜を通過する溶質と溶媒に等しい溶液です。 溶質と溶媒の動きは同じです。 平衡とは、化学反応が安定したときに発生し、順反応と逆反応が釣り合っていることです。

アイソトニック ソリューションは、これが別として知られている XNUMX つのタイプのソリューションの XNUMX つです。 高張液と 低張 解決策はわかっています。
溶液は、構成要素、つまり溶質と溶媒の両方が同じ濃度で持続する場合、等張状態を獲得できます。 そのような状態の良い例は、人体の血球です。
それらは、栄養素、水、およびその他の物質が膜を通過して、主に酸素を運ぶことを可能にします. 平衡は、反応物と生成物の両方の場合の化学溶液の状態です。
それらは安定しているか、同じレートです。 換言すれば、順反応および逆反応が起こり、得られた生成物が得られ、それが再び反応物中で分解する。
それぞれの反応では、順方向の反応速度と逆方向の反応速度は同じかもしれませんが、平衡状態でゼロになることはありません。
比較表
| 比較のパラメータ | 等張液 | 平衡 |
|---|---|---|
| 発見者 | シドニー・リンガー | ギブスとル・シャトリエ |
| 年 | 1882 | 1873 |
| 定義 | 半透膜を通過する成分(溶質と溶媒)の濃度は同じです。 | 正反応と逆反応が均衡または安定しているとき |
| 準備 | 手動で準備できます | それ自体で達成されるため、手動で準備することはできません |
| 物理的パラメータ | そのような効果はありません | 反応速度、温度、圧力などの影響を受ける |
| ムーブメント | 同じ濃度勾配のため動きは見られません | 正味の力がゼロのため動かない |
等張液とは?
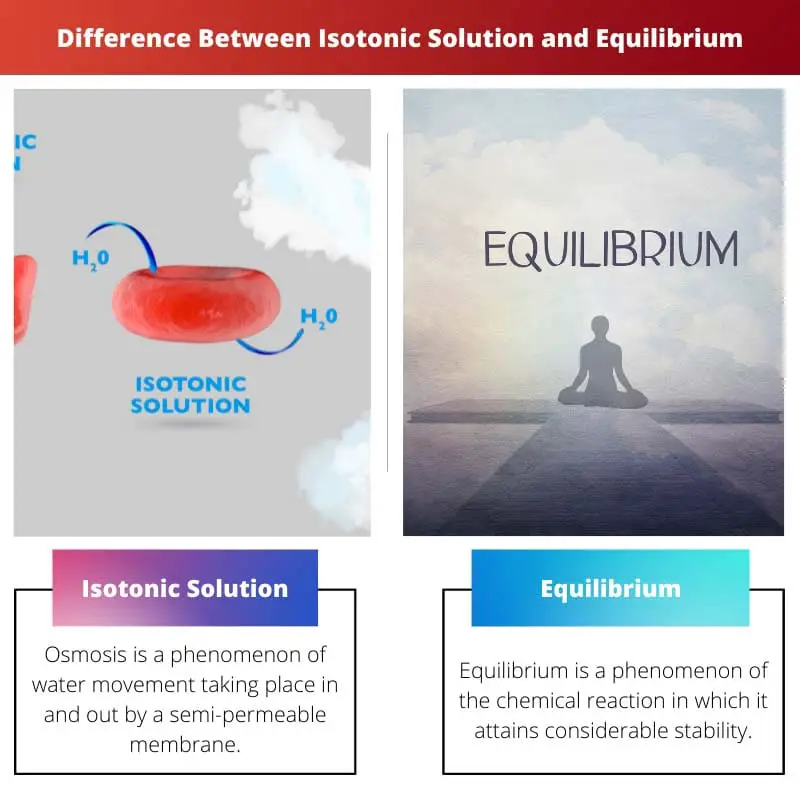
浸透とは、半透膜によって水の出入りが起こる現象です。 これは、低張性ソリューションであるXNUMXつのタイプのソリューションにさらに細分されます。
高張液と等張液。 等張液とは、溶液の濃度勾配が同じ (溶質と溶媒の) 半透膜を通過する場所です。
言葉自体は等しいという意味で、溶質と溶媒の両方の動きは等しいです。 シドニー・リンガーは1882年にアイソトニック・ソリューションの現象を発見しました。
等張液の現象は、実験室で手動で準備することで確立できます。 等張液は、外的要因の影響を受けないと言われています。
たとえば、反応速度、圧力、温度などです。また、粒子の動きは溶液中で非常に遅く、目立たないほどです。

平衡とは何ですか?
平衡は、かなりの安定性を達成する化学反応の現象です。 言い換えれば、XNUMXつの反応が前方にある場合、反応物が変化します。
生成物と生成物が再び分解する逆反応。 反応物を形成するには、反応物をさらに壊すことができるかなりの点で安定性を達成します。
また、生成物が分解して反応物を形成することはありません。 平衡という言葉自体は、平等と安定を意味します。
これに加えて、平衡現象はギブスとル・シャトリエによって発見されました。 彼らは両方とも、ギブスが 1873 年から 1878 年まで働いた別のタイムラインでそれに取り組みました。
ル シャトリエが 1875 年に研究を行った一方で、他の多くの科学者もこの発見に取り組みました。
おそらく、この現象は、反応速度、温度、圧力などの外的要因の影響を受けます。また、ゼロに等しくない力が作用しているため、動きは気付かれません。
等張液と平衡の主な違い
- 等張性溶液の現象は科学者のシドニー・リンガーによって発見されましたが、一方、平衡の現象はXNUMX人の科学者ギブスとル・シャトリエによって発見されました。
- 等張溶液現象の発見は 1882 年になされたのに対し、一方、平衡現象の発見は 1873 年に最初になされ、その後、別の科学者が別のタイムラインで取り組んだことになります。
- 等張溶液の現象は、半透膜を通過する溶液 (溶質と溶媒の両方) の濃度勾配が同じ場合について述べることができます。ソリューションの順方向および逆方向の反応が安定していると述べられています。
- 等張液を定義するソリューションは手動で準備できますが、一方、平衡反応は特定の点でそれ自体に到達するため、手動で準備することはできません。
- 等張液は最終的に外部の物理的要因の影響を受けませんが、一方、平衡現象は温度、圧力、濃度、反応速度などの外部現象の影響を受けやすい傾向があります。
- 等張溶液では、半透膜による成分の移動は非常に遅く、浸透のプロセスによって発生しますが、一方、平衡では、その移動は、等しい正味の力はゼロです。
参考文献
- https://link.springer.com/article/10.1007/BF02989804
- https://pubs.acs.org/doi/pdf/10.1021/je60058a011
- https://onlinelibrary.wiley.com/doi/abs/10.1111/j.1365-2818.1985.tb02641.x
- https://wires.onlinelibrary.wiley.com/doi/abs/10.1002/wcs.108
最終更新日 : 11 年 2023 月 XNUMX 日

Piyush Yadav は、過去 25 年間、地元のコミュニティで物理学者として働いてきました。 彼は、読者が科学をより身近なものにすることに情熱を傾ける物理学者です。 自然科学の学士号と環境科学の大学院卒業証書を取得しています。 彼の詳細については、彼のウェブサイトで読むことができます バイオページ.


等張溶液と平衡の詳細な比較とそれらの主な違いの説明は非常に勉強になります。平衡反応は自然に起こる一方で、等張溶液は手動で調製できることを知るのは興味深いです。
浸透と、等張溶液を含む 3 種類の溶液について提供される情報は、非常にわかりやすくなっています。等張溶液が外部の物理的要因にどのように影響されないかを知るのは興味深いことです。
この記事では、等張液と平衡の概念をわかりやすく説明します。等張溶液中の溶質と溶媒の動きと、平衡状態における順反応と逆反応のバランスとの違いは、十分に説明されています。
私も同意します。この記事は等張溶液と平衡の違いを詳細な情報で効果的に強調しています。
等張溶液と平衡の発見と定義についての詳細な説明は啓発的です。等張溶液は外部の物理的要因の影響を受けないという主張は興味深いものです。
等張溶液と化学平衡についての包括的な説明をありがとうございます。等張溶液では溶質と溶媒の動きが等しいことは明らかですが、平衡とは順反応と逆反応のバランスを指します。
等張液と平衡の詳細な説明と比較表により、これらの概念を包括的に理解できます。等張溶液と平衡反応の動きの違いを分かりやすく説明していただき感謝しています。
比較表は、等張溶液と平衡の主な違いを理解するのに非常に役立ちます。平衡反応は自然に起こる一方で、等張溶液は手動で調製できることに注目するのは興味深いことです。
等張液と平衡の説明は、その定義と主な違いとともに、徹底的で有益です。等張溶液と平衡を説明するために使用される例も非常に役立ちます。