Ķīmija ir ļoti interesants priekšmets starp visiem citiem. Tas ietver saites, rezonansi, spilgtus savienojumus, ķīmiskas reakcijas utt.
Ķīmijā savienojumi rada jonus, katjonus, anjonus, elektronus utt. Priekšmeta galvenā pievilcība ir periodiskā tabula, kas aizņem visus dabiski vai mākslīgi radītos elementus uz zemes.
Atslēgas
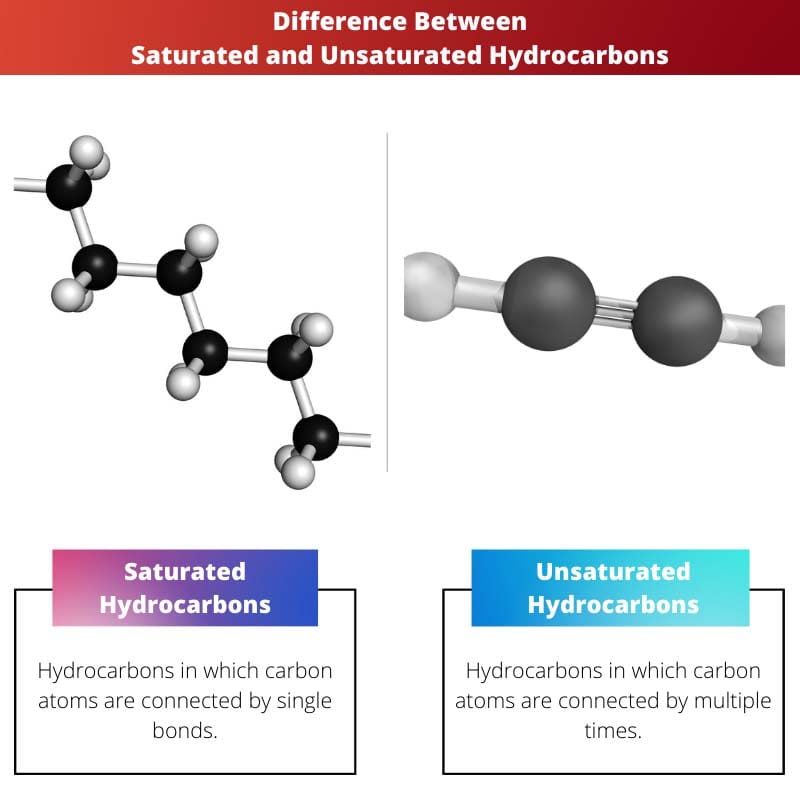
- Piesātinātie ogļūdeņraži satur vienas saites, bet nepiesātinātie ogļūdeņraži satur dubultās vai trīskāršās saites.
- Piesātinātie ogļūdeņraži ir cietas vielas vai šķidrumi istabas temperatūrā, savukārt nepiesātinātie ogļūdeņraži ir gāzes vai šķidrumi.
- Piesātinātajiem ogļūdeņražiem ir augstāka kušanas un viršanas temperatūra nekā nepiesātinātajiem ogļūdeņražiem.
Piesātinātais ogļūdeņradis pret nepiesātināto ogļūdeņradi
Atšķirība starp piesātināto ogļūdeņražu un nepiesātināto ogļūdeņražu ir tāda, ka piesātināto ogļūdeņražu savienojums satur vai tam ir viena saite starp diviem oglekli, ti, divi dažādie oglekļa atomi ir savienoti ar vienotu saiti starp tiem.

Piesātinātais ogļūdeņradis ir norādīts kā ogļūdeņraži, kas sastāv tikai no oglekļa un ūdeņraža, kur divi oglekļa atomi ir saistīti ar vienotu saiti.
Atlikušās oglekļa atomu saites tiek izpildītas ar ūdeņraža atomiem, lai tās neveidotu vairākas saites. Alkāni ir piesātināta ogļūdeņraža piemērs.
Alkānu savienojumi ir – metāns, etāns, butāns, pentāns, heksāns u.c.
Nepiesātinātais ogļūdeņradis ir norādīts kā ogļūdeņraži, kas sastāv tikai no oglekļa un ūdeņraža, un abas ūdeņraža saites ir savienotas ar vairākām saitēm.
Nepiesātinātajiem ogļūdeņražiem ir divu veidu ogļūdeņražu savienojumi, un tiek uzskatīts, ka tie ir alkēni un alkīni.
Alkēnu savienojumu piemēri ir – butēns, heksēns, pentēns, etēns utt., bet alkīnu savienojumu piemēri – acetilēns, okt-1-īns, 1-heksīns utt.
Salīdzināšanas tabula
| Salīdzināšanas parametri | Piesātināts ogļūdeņradis | Nepiesātināts ogļūdeņradis |
|---|---|---|
| Definīcija | Ogļūdeņraži, kuros oglekļa atomi ir savienoti ar vienotām saitēm | Ogļūdeņraži, kuros oglekļa atomi ir savienoti vairākas reizes |
| Ogļūdeņražu veidi | Divi veidi – alkāni un cikloalkāni | Trīs veidi – alkēni, alkīni, aromātiskie |
| hibridizācija | sp3 | sp2 vai sp1 |
| Ūdeņraža atomi | Vairāk atomu | Mazāks atomu skaits |
| Ķīmiskā reaģētspēja | Zems | augsts |
| Liesmas tests | Dod zilu liesmu | Piešķir sodrēju liesmu (vai augsnes krāsas) |
| Piemērs | Alkāni, cikloalkāns, butāns, pentāns | Alkīni, alkēni, aromātiskie, acetilēns |
Kas ir piesātinātais ogļūdeņradis?
Piesātinātos ogļūdeņražus definē kā ogļūdeņražus, ko veido divi oglekļa atomi, starp kuriem ir viena saite. Pārējās saites ir savienotas vai veidotas ar ūdeņraža atomiem, lai izpildītu oglekļa valenci.
Vispārējā formula, ko izmanto piesātinātā ogļūdeņraža iegūšanai, ir – CnH2n+2.
Piesātinātie ogļūdeņraži ir divu veidu - alkāni un cikloalkāni. Daži no alkānu savienojumiem ir - metāns, etāns, propāns, butāns, pentāns utt.
Cikloalkāni ir savienojumi ar gredzenveida struktūrām kopā ar hibridizētiem atomiem. Cikloalkānu īpašības ir gandrīz līdzīgas alkānu īpašībām, izņemot viršanas un kušanas temperatūru, kas ir salīdzinoši augstākas.
Tālāk ir norādītas piesātināto ogļūdeņražu īpašības vai lietojumi:
- Piesātinātie ogļūdeņraži savos savienojumos satur lielāku skaitu ūdeņraža atomu.
- Metāns – pirmais alkāna savienojums ir ļoti noderīgs, un to var izmantot kā raķešu degvielu vai automašīnās, sildītājos utt.
- Alkāni un cikloalkāni ir divi ievērojami atšķirīgi piesātināto ogļūdeņražu veidi.
- Cikloalkānus var izmantot neilona, naftas gāzes, gumijas u.c. ražošanai.
- Etāns, otrais alkāna savienojums, ir ledusskapja dzesēšanas šķidrums. Turklāt tam ir liela nozīme etilēna ražošanā.
Kas ir nepiesātināts ogļūdeņradis?
Nepiesātinātos ogļūdeņražus definē kā ogļūdeņražus, ko veido divi oglekli, starp kuriem ir vairākas saites. Daudzkārtējās saites var būt dubultsaites vai trīskāršās saites.
Vēlāko oglekļa valenci aizpilda ūdeņraža atomi. Vispārīgā nepiesātinātā ogļūdeņraža formula ir alkēniem – CnH2n, bet alkīniem – CnH2n-2.
Nepiesātinātajiem ogļūdeņražiem ir trīs veidu - alkēni, alkīni un aromātiskie savienojumi. Aromātisko savienojumu īpašības nav tādas pašas kā alkēniem un alkīniem.
Turklāt šie savienojumi ir salīdzinoši stabilāki nekā alkēni vai alkīni.
Tālāk ir norādītas nepiesātināto ogļūdeņražu īpašības vai lietojumi:
- Lai izveidotu nepiesātinātu ogļūdeņražu, ūdeņraža atomu skaits ir mazāks, kā arī daudzkārtējās saites (dubultā vai trīskāršā saite).
- Divi oglekļa atomi, kas saistīti ar nepiesātināto ogļūdeņradi, veido aptuveni 120 grādu lielu saites leņķi.
- Visizplatītākais aromātiskais ogļūdeņradis, benzols, veido 120 grādu saites leņķi ar citiem atomiem.
- Jebkurā reakcijā, kad veidojas ūdens vai oglekļa dioksīds, notiek sadegšana.
- Oksidācijas reakcijas izraisa ūdeņraža atomu pievienošana vai atņemšana reakcijā.
Galvenās atšķirības starp piesātinātajiem un nepiesātinātajiem ogļūdeņražiems
- Piesātinātais ogļūdeņradis ir ogļūdeņraži, kas veidojas ar oglekļa un ūdeņraža atomiem, un divi oglekļa atomi ir saistīti ar vienu saiti, savukārt, no otras puses, nepiesātinātais ogļūdeņradis ir ogļūdeņraži, kas veidojas arī ar oglekļa un ūdeņraža atomiem un oglekļa atomi ir savienoti ar vairākām saitēm, un tā var būt dubultā vai trīskāršā saite.
- Piesātinātie ogļūdeņraži ir galvenokārt divu veidu, un tie ir – alkāni un cikloalkāni, savukārt, salīdzinoši, nepiesātinātie ogļūdeņraži ir galvenokārt trīs veidu un tie ir – alkēni, alkīni un aromātiskie savienojumi.
- Hibridizācija, ko parāda piesātinātie ogļūdeņraži, ir sp3, savukārt, no otras puses, nepiesātināto ogļūdeņražu hibridizācija ir sp2 alkēniem un sp1 vai sp alkīniem.
- Ūdeņraža atomu skaits piesātinātajos savienojumos ir lielāks, savukārt, salīdzinoši, nepiesātinātajos savienojumos ūdeņraža atomu skaits ir mazāks.
- Piesātināto savienojumu ķīmiskā reaktivitāte ir zema, ja to salīdzina, no otras puses, nepiesātināto savienojumu ķīmiskā reaktivitāte ir augsta.
- Liesmas tests, ko parāda piesātinātie savienojumi, ir zilā liesma, savukārt, no otras puses, nepiesātināto savienojumu liesmas tests ir kvēpu liesma (vai augsnes krāsas liesma).
- Piesātināto ogļūdeņražu piemēri ir – alkāni, cikloalkāni, butāns, heksāns, oktāns u.c., savukārt, salīdzinoši, nepiesātinātie ogļūdeņraži ir – aromātiskie savienojumi, alkīni un alkēni.
- https://www.sciencedirect.com/science/article/abs/pii/S0376738800006232
- https://pubs.acs.org/doi/abs/10.1021/ct300215p
- https://www.frontiersin.org/articles/10.3389/fchem.2014.00075/full
- https://cdnsciencepub.com/doi/abs/10.1139/v71-612
Pēdējo reizi atjaunināts: 25. gada 2023. jūlijā

Pijušs Jadavs pēdējos 25 gadus ir pavadījis, strādājot par fiziķi vietējā sabiedrībā. Viņš ir fiziķis, kurš aizrautīgi cenšas padarīt zinātni pieejamāku mūsu lasītājiem. Viņam ir bakalaura grāds dabaszinātnēs un pēcdiploma diploms vides zinātnē. Vairāk par viņu varat lasīt viņa vietnē bio lapa.


Sadaļā par galvenajām atšķirībām starp piesātinātajiem un nepiesātinātajiem ogļūdeņražiem sniegts skaidrs pārskats par dažādām ķīmiskajām īpašībām. Tas ir noderīgi gan studentiem, gan profesionāļiem.
Sīki izstrādāti piesātināto un nepiesātināto ogļūdeņražu un to ķīmisko īpašību skaidrojumi ir ļoti noderīgi. Šeit sniegtā informācija ir sniegta skaidrā un sakārtotā veidā.
Īpaši interesanta man likās sadaļa par piesātināto ogļūdeņražu un nepiesātināto ogļūdeņražu izmantošanu. Ir aizraujoši redzēt, kā šie savienojumi tiek izmantoti dažādās nozarēs.
Pilnīgi noteikti! Izpratne par to pielietojumiem reālajā pasaulē palīdz novērtēt šo savienojumu nozīmi ikdienas dzīvē.
Rakstā sniegtā salīdzināšanas tabula ir īpaši noderīga, lai ātri izprastu atšķirības starp piesātinātajiem un nepiesātinātajiem ogļūdeņražiem. Labi padarīts!
Jauks raksts! Tas sniedz visaptverošu pārskatu par atšķirībām starp piesātinātajiem un nepiesātinātajiem ogļūdeņražiem, kas ir būtiski, lai izprastu ķīmijas pamatus.
Es pilnīgi piekrītu! Rakstā ļoti skaidri un kodolīgi izskaidroti jēdzieni.
Rakstā ir sniegts pamatīgs skaidrojums par piesātināto un nepiesātināto ogļūdeņražu ķīmisko reaktivitāti un īpašībām. Šāda veida detalizēta izpratne ir ļoti svarīga ķīmijas jomā.
Es novērtēju detalizēto informāciju par piesātināto un nepiesātināto ogļūdeņražu izmantošanu. Tas palīdz izprast šo savienojumu praktisko nozīmi mūsu ikdienas dzīvē.
Šajā rakstā ir labi izklāstītas piesātināto un nepiesātināto ogļūdeņražu ķīmiskās īpašības un atšķirības. Tas ir lielisks resurss studentiem un ikvienam, kam interesē ķīmija.
Detalizēti piesātināto ogļūdeņražu, nepiesātināto ogļūdeņražu un to īpašību skaidrojumi ir ļoti informatīvi. Ir lieliski, ka vienviet ir tik skaidra informācija.