Молекулы и элементы состоят из атомов. Атомы — это мельчайшие единицы, которые нельзя упростить до более мелких материалов. Элементы являются производными от свойств атома. Атомы составляют основу молекул и элементов.
Важно проводить тонкое различие между молекулами и элементами, чтобы изучать их свойства и природу.
Основные выводы
- Элемент – это чистое вещество из атомов с одинаковым числом протонов.
- Молекула объединяет два или более атомов, удерживаемых вместе химическими связями.
- Элементы нельзя разложить на более простые вещества, а молекулы можно разложить на составные атомы.
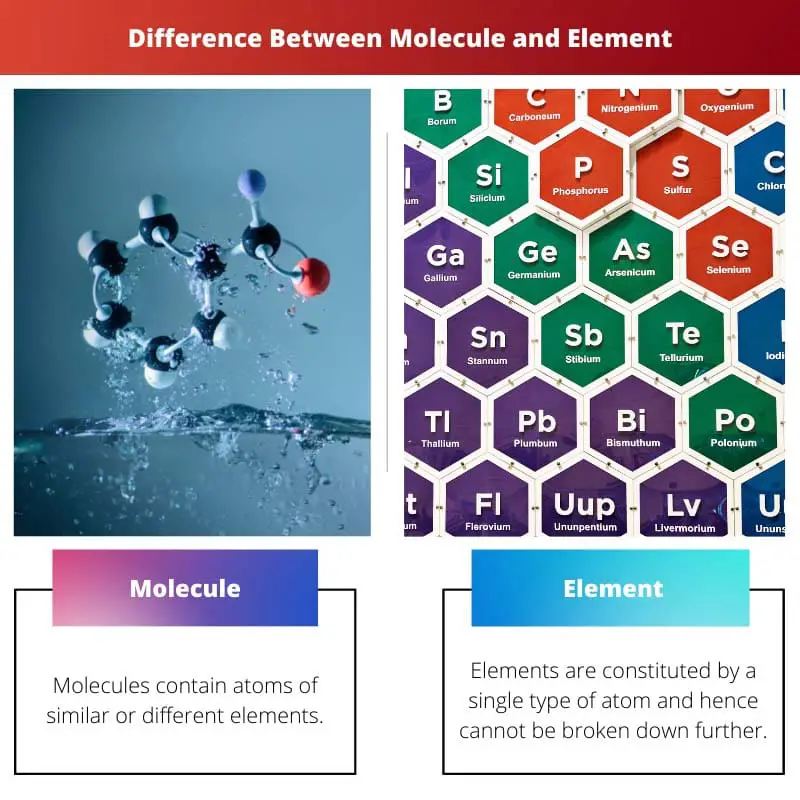
Молекула против элемента
Разница между молекулами и элементами заключается в их свойствах и образовании. Молекулы состоят из двух или более атомов, образующих химические связи сходных или разнородных элементов. С другой стороны, элементы имеют разное образование. Они образованы одним атомом. Их нельзя разложить на более простые вещества, поскольку они существуют в чистом виде.

Молекулы образуются путем химической связи двух или более атомов. Химические связи образуются путем обмена электронами. Когда атомы элементов связываются друг с другом, они образуют молекулы.
Атомы некоторых элементов могут быть легко связаны, например, с хлором, в то время как некоторые могут быть трудно связаны, например, с аргоном.
Элемент состоит из атома одного типа. Частицы элементов могут быть искусственными или искусственными. Различное расположение атома может привести к различным версиям этого элемента.
Например, хотя алмаз и графит являются аллотропами углерода, они совершенно разные по внешнему виду. Они имеют одинаковую химическую структуру, но разные химические свойства.
Сравнительная таблица
| Параметры сравнения | молекула | Элемент |
|---|---|---|
| атомы | Молекулы содержат атомы одинаковых или разных элементов. | Элементы состоят из одного типа атомов и, следовательно, не могут быть разбиты дальше. |
| Разделение | Его можно разделить далее с помощью химических средств. | Ни в коем случае его нельзя разделить дальше. |
| Облигации | Они образуют либо ионные, либо ковалентные связи. | Они могут образовывать различные типы связей в зависимости от стабильности и электронной конфигурации. |
| Участники | Он состоит из двух или более атомов, связанных друг с другом. | В настоящее время насчитывается 115 химических элементов. |
| Примеры | Его примерами являются вода, d-окись углерода, озон и т. д. | Его примерами являются азот, медь, цинк, кислород и т.д. |
Что такое молекула?
Слово «молекула» относится к атомам, которые удерживаются вместе сильными химическими связями. Они различаются по размеру в зависимости от соединенных атомов. Одни молекулы образованы двумя одинаковыми атомами, другие – сложными связями.
- Два атома одного и того же элемента: Кислород (O2), образованный двумя атомами кислорода
- Три атома подобного элемента: Озон (03), образованный тремя атомами кислорода
- Комплексное склеивание: Углекислый газ (CO2), образованный соединением одного атома углерода и двух атомов кислорода
Молекулы могут быть образованы ковалентными или ионными связями. Ковалентная связь также известна как общая связь. В ковалентных связях атомы делят свои электроны, тогда как в ионных связях атом отдает свой электрон другому атому.
Отдельный элемент не считается молекулой. Например, один элемент кислорода (O) или углерода (C) не является молекулой. Молекулы образуются, когда два или более атома образуют химическую связь.
Некоторыми распространенными молекулами являются озон, вода, глюкоза и т. д.
Молекулы делятся на несколько категорий, некоторые из которых представляют собой гомоядерные и гетероядерные молекулы, органические или неорганические молекулы, двухатомные, трехатомные или многоатомные молекулы и т. д.

Что такое Элемент?
Элементы — это чистые вещества, которые нельзя разделить или разложить на более простые вещества. Они могут относиться к атомам, имеющим одинаковое количество протонов в ядре. Они могут различаться массой и нейтронами.
Когда атомы, содержащие сходные элементы, имеют разное число нейтронов, их называют изотопы.
В таблице Менделеева свое место занимают 118 элементов. В периодической таблице элементы классифицируются на основе их характеристик и атомного номера.
Каждый элемент имеет свой уникальный атомный символ, атомную массу, символ и электронное устройство.
Возникает необходимость классифицировать элементы периодической таблицы. Изучение свойств каждого из 118 элементов становится громоздким. Итак, ученые разработали способ группировки элементов со схожими характеристиками.
Эти группировки выполняются на основе четырех блоков.
- с блок: Элементы s-блока делятся на 2 группы. Элементы 1 группы называются щелочными металлами, а элементы 2 группы называются щелочной земные металлы.
- п блок: Элементы p-блока подразделяются на металлы, неметаллы и металлоиды.
- д блок: Элементы d-блока состоят из трех рядов, а именно первого, второго и третьего переходных рядов.
- ф блок: f-блок содержит всего двадцать восемь элементов, которые разбиты на две равные серии. Ряд первых четырнадцати элементов называется рядом лантанидов. Второй набор из четырнадцати элементов называется серией актинидов.
Основные различия между молекулой и элементом
- Молекула может быть гомоядерной или гетероядерной, а элемент называется имеющим уникальный атомный номер.
- Молекулы состоят из атомов одинаковых или разных элементов, тогда как элементы содержат только одинаковые атомы.
- Молекулы и элементы различаются по своей химической конфигурации. Молекулы могут образовывать определенный тип связи, т. е. ковалентную или ионную связь. С другой стороны, элементы могут образовывать многочисленные типы связей в зависимости от расположения электронов.
- Молекула — это вещество, которое может быть далее разделено на более мелкие вещества, в то время как элементы не могут быть далее разделены химическими средствами.
- Примеры молекул включают сахар, глюкозу, хлор, ацетони т. д. Примеры элементов включают углерод, водород, гелий и т. д.
- https://www.sciencedirect.com/science/article/pii/S0166354201002224
- https://aip.scitation.org/doi/abs/10.1063/1.329173
Последнее обновление: 23 июля 2023 г.

Пиюш Ядав последние 25 лет работал физиком в местном сообществе. Он физик, увлеченный тем, чтобы сделать науку более доступной для наших читателей. Он имеет степень бакалавра естественных наук и диплом о высшем образовании в области наук об окружающей среде. Подробнее о нем можно прочитать на его био страница.


В посте представлен всеобъемлющий обзор характеристик и образований молекул и элементов, предлагающий детальное понимание концепций.
Описание различных блоков таблицы Менделеева очень информативно и обеспечивает глубокое понимание классификаций элементов.
Пост эффективно отражает разницу между атомами, молекулами и элементами, добавляя ясности в их состав.
Подробное объяснение различий между молекулами и элементами высокоинформативно и дает четкое представление об их характеристиках.
Я ценю предоставленные подробные примеры, которые дополнительно проясняют понятия о молекулах и элементах.
Классификация элементов в таблице Менделеева хорошо объяснена, помогая понять их группировку на основе характеристик.
Классификация элементов в периодической таблице удачно описана в посте, что дает ценную информацию об их классификации.
Подробное объяснение каждого блока таблицы Менделеева облегчает понимание группировки элементов.
Согласен с вашей оценкой, в посте эффективно изложена классификация элементов по их характеристикам.
Пост эффективно объясняет различия между молекулами и элементами, предлагая полное понимание их структур и атомов.
Подробное объяснение того, что представляет собой элемент и молекула, очень информативно и добавляет посту глубины.
В посте рассматриваются основные различия между молекулами и элементами. Это объясняет структуру и формирование обоих, а также важность изучения их свойств.
Да, сравнительная таблица дает четкое представление о различиях между молекулами и элементами.
Согласен, пост очень информативный и подробный.
В посте объясняются важные различия между молекулами и элементами. Подробное объяснение дает полное представление об их составе и структуре.
Согласен, пост дает четкое представление об атомах, молекулах и элементах.
Примеры молекул и элементов еще больше улучшают понимание концепций, обсуждаемых в посте.
В посте эффективно сформулированы различия между молекулами и элементами, а также детали их образования и свойств.
Кстати, сравнительная таблица и подробные описания очень помогают в понимании концепций.
Подробная сравнительная таблица эффективно описывает различия между молекулами и элементами, обеспечивая полное понимание их свойств и различий.
Согласен, объяснение свойств и характеристик молекул и элементов весьма подробное и информативное.
Классификация элементов и их свойств представлены в организованном виде, что повышает понятность статьи.
Детальное сравнение молекул и элементов очень полезно и дает полное представление об их структурах и образованиях.
Категоризация молекул по разным категориям является ценным дополнением к посту, улучшающим понимание темы.
В статье хорошо объяснена разница между ковалентными и ионными связями в молекулах.
Подробное объяснение молекул и элементов обеспечивает глубокое понимание их природы и состава.