Мир — прекрасное место. Горы, море, небо и все, что физически существует, состоит из атомов.
Они строительные блоки Вселенной. Однако атомы нестабильны. Следовательно, они стабилизируют себя, создавая молекулы и ионы.
Основные выводы
- Молекула — это группа из двух или более атомов, химически связанных друг с другом, а ион — это атом или молекула с электрическим зарядом.
- Молекулы нейтральны, а ионы могут быть заряжены положительно или отрицательно.
- Молекулы образуются за счет ковалентной связи, а ионы образуются за счет переноса электронов между атомами.
Молекула против иона
Молекулы и ионы различаются, потому что у молекулы нет общего заряда, а у иона он есть. Это происходит потому, что все в этой вселенной стремится к равновесию.
Атомы делают это, образуя молекулы и ионы. Кроме того, молекулы образуются за счет обмена электронами, тогда как ионы образуются за счет обмена электронами.
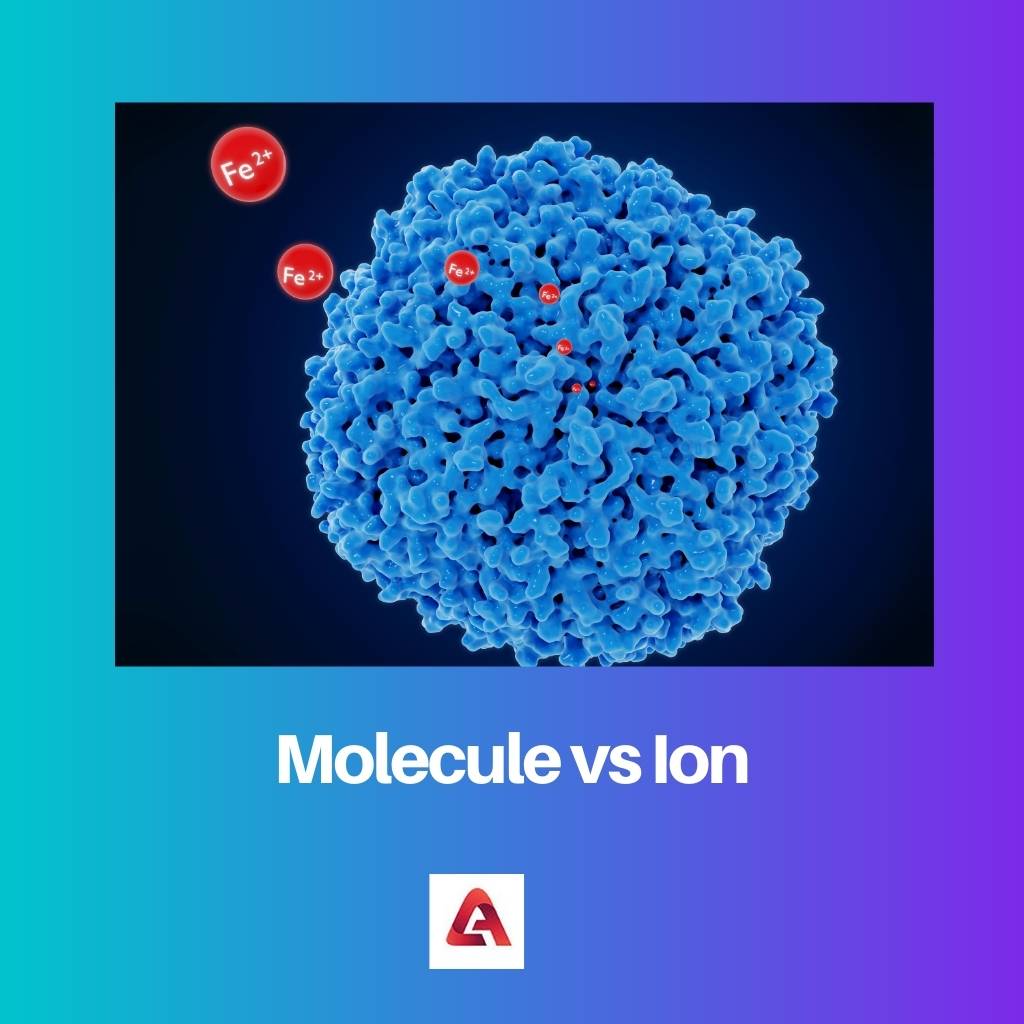
Один или несколько атомов образуют ковалентные связи, чтобы стать молекулой. Наименьшая единица, из которой состоит вещество, — это молекула. Молекула сохраняет все химические свойства эссенции. Атомы изображают молекулы, представленные кружками, образующие связи вместе.
Химический вид с чистым положительным или отрицательным зарядом известен как ион. Ан атом и молекулу можно назвать ионом, если они имеют ненулевые чистые счета. Следовательно, все ионы либо имеют больше электронов, чем протонов, либо больше протонов, чем электронов в их молекулярной или атомной структуре.
Сравнительная таблица
| Параметры сравнения | молекула | ион |
|---|---|---|
| Распределение электронов | Молекулы образуются за счет обмена электронами между двумя или более атомами или двумя противоположно заряженными ионами. | Ионы образуются, когда атомы приобретают или теряют заряд для достижения конфигурации благородного газа. |
| Размер | Размер молекулы зависит от размера атомов или ионов, участвующих в образовании связи. | Анионы более значимы, чем исходные молекулы, а катионы более второстепенны, чем исходные молекулы. |
| Стабильность | Молекулы более стабильны, чем ионы. | Ионы менее стабильны, чем молекулы. |
| обучение | Ковалентные связи или ионные связи образуют молекулы. | Ионы образуются в результате ионной связи между двумя ионами с противоположным зарядом и являются более мощными, чем ковалентные. |
| Электропроводность | Поскольку суммарный заряд молекул равен нулю, они не являются хорошими проводниками электричества. | Ионы являются хорошими проводниками электричества. |
Что такое молекула?
Наименьшая единица соединения, которая показывает химические свойства соединения, известна как молекула. Молекулы состоят из двух или более атомов, ковалентно связанных друг с другом, т. е. они имеют один или несколько общих электронов.
Молекулы составляют большую часть Земли, и почти все органические вещества состоят из молекул.
Молекулы могут быть гомоядерными и гетероядерными, что означает, что они состоят из одинаковых или разных элементов соответственно.
Ковалентная связь образуется, когда два атома с неполными октетами имеют общие биты. Ковалентная связь превращает различные атомы в молекулу.
Молекулы состоят из атомов, сгруппированных вместе ковалентными или ионными связями.
Ковалентно связанные молекулы слабее, чем молекулы с ионной связью. Это происходит потому, что ионные связи обладают мощной электростатической силой, удерживающей ионы вместе.
Благодаря этому ионные молекулы более стабильны, чем молекулы, связанные ковалентно.

Что такое Ион?
Ион — это химический вид с чистым положительным или отрицательным зарядом некоторой величины. Ионы относятся к молекулам и атомам, которые имеют ненулевой чистый контроль.
Следовательно, ионы имеют либо больше протонов, чем электронов, либо больше электронов, чем протонов в своей молекулярной или атомной структуре.
Ионы, которые имеют большее количество электронов, чем протоны, и имеют суммарный отрицательный заряд, известны как анионы.
И наоборот, ионы с более значительным числом протонов, чем электронов, и обладающие суммарным положительным зарядом, известны как катионы.
Ионные связи образуются только при возникновении электростатических сил между отрицательно заряженным анионом и положительно заряженным катионом.
Эти электростатические силы притягивают анионы и катионы друг к другу, чтобы стабилизировать общий заряд. Эти электростатические силы помогают в формировании ионные соединения.
Ионы, состоящие только из одного элемента, называются атомарными или одноатомными ионами. Участвующие атомы несут некоторый суммарный заряд, положительный или отрицательный.
В то время как два или более элементов входят в состав иона, их называют молекулярными или многоатомными ионами.
Основные различия между молекулами и ионами
- Молекулы не имеют суммарного заряда, тогда как ионы имеют суммарный положительный или отрицательный контроль.
- Молекулы образуются, когда два или более атома делят электроны, чтобы завершить свой октет, в то время как ионы обмениваются электронами и образуют ионные соединения из-за электростатических сил.
- Поскольку ионы удерживаются вместе электростатическими силами, они гораздо более стабильны, чем молекулы, образованные ковалентными связями.
- Из-за высоких сил притяжения между двумя ионами они имеют большую энергию решетки, чем ковалентно связанные молекулы.
- Из-за более высокой энергии решетки ионы более стабильны, чем ковалентно связанные.
- Размер молекул зависит от атомов, участвующих в образовании связей. Катионы меньше, чем их исходные молекулы, тогда как анионы более значительны, чем их исходные молекулы.

- https://ui.adsabs.harvard.edu/abs/1988STIA…8915174M/abstract
- https://pubs.acs.org/doi/pdf/10.1021/ja00260a006
Последнее обновление: 11 июня 2023 г.

Пиюш Ядав последние 25 лет работал физиком в местном сообществе. Он физик, увлеченный тем, чтобы сделать науку более доступной для наших читателей. Он имеет степень бакалавра естественных наук и диплом о высшем образовании в области наук об окружающей среде. Подробнее о нем можно прочитать на его био страница.

Сравнительная таблица статьи оказалась особенно полезной для понимания различных характеристик молекул и ионов. Это отличный ориентир для быстрого сравнения.
Я также нашел сравнения очень полезными. Это удобный способ быстро понять основные различия между молекулами и ионами.
В статье предлагалось всестороннее сравнение молекул и ионов, но ей не хватало более увлекательного подхода, который мог бы сделать содержание более увлекательным для читателей.
Я понимаю вашу точку зрения. Хотя информация была ценной, более увлекательное повествование могло бы повысить общую привлекательность статьи.
Сравнительная таблица статьи эффективно суммировала основные различия между молекулами и ионами. Это полезный инструмент для анализа и закрепления концепций.
В статье дано четкое и краткое представление о молекулах и ионах, что ценно для новичков в области химии.
Я согласен. Это хорошая отправная точка для тех, кто плохо знаком с химией, но она могла бы включать в себя более продвинутые концепции для тех, кто более глубоко разбирается в предмете.
Эта статья представляет собой увлекательный взгляд на мир молекул и ионов. Подробные объяснения и сравнения дали большое понимание.
Статья мне показалась очень информативной и хорошо структурированной. Это действительно помогло мне понять разницу между молекулами и ионами.
Я полностью согласен. Предоставленная информация очень познавательна и интересна.
Статья хорошо упростила сложные понятия, но в ней не хватало углубленного обсуждения химических свойств и поведения молекул и ионов.
Я согласен с вами. Хотя статья представляла собой общий обзор, она могла бы включать более подробную информацию о химических свойствах этих фундаментальных единиц.
Предоставленные сравнения были очень полезны для понимания различий между молекулами и ионами. Ценю ясность объяснений.
Статья показалась мне слишком элементарной. Он не предлагал особой глубины для тех, кто ищет более подробную информацию.
Я не мог не согласиться. Ясность и простота статьи делают ее ценным ресурсом для всех, кто интересуется химией.
Я думаю, что статья эффективно подчеркивает ключевые различия между молекулами и ионами, облегчая понимание для специалистов, не являющихся химиками.
Я думаю, что статья слишком упростила понятия о молекулах и ионах. Можно было бы глубже изучить химию, лежащую в основе этих фундаментальных строительных блоков.
Я понимаю вашу точку зрения, но для общего обзора статья является хорошей отправной точкой. Важно сделать сложные темы доступными для широкой аудитории.
Объяснения были ясными и краткими, что облегчало понимание различий между молекулами и ионами. Статья послужила прочной основой для дальнейшего обучения.
Я также нашел ясность объяснений очень полезной. Это отлично подходит для формирования четкого понимания этих концепций.