Las moléculas y los elementos están formados por átomos. Los átomos son la unidad más pequeña que no se puede simplificar en materiales más pequeños. Los elementos se derivan de las propiedades de un átomo. Los átomos forman la base de las moléculas y los elementos.
Es importante hacer una fina distinción entre moléculas y elementos para estudiar sus propiedades y naturaleza.
Puntos clave
- Un elemento es una sustancia pura de átomos con el mismo número de protones.
- Una molécula combina dos o más átomos que se mantienen unidos por enlaces químicos.
- Los elementos no se pueden descomponer en sustancias más simples, mientras que las moléculas se pueden descomponer en átomos constituyentes.
Molécula vs Elemento
La diferencia entre moléculas y elementos radica en sus propiedades y formación. Las moléculas consisten en dos o más átomos que forman enlaces químicos de elementos similares o diferentes. Por otro lado, los elementos tienen diferentes formaciones. Están formados por un solo átomo. No pueden hermanarse en sustancias más simples tal como existen en su forma pura.

Las moléculas se forman por la unión química de dos o más átomos. Los enlaces químicos se forman por el intercambio de electrones. Cuando los átomos de los elementos se unen entre sí, dan como resultado moléculas.
Los átomos de algunos elementos pueden ser fáciles de unir, por ejemplo, con cloro, mientras que algunos pueden ser difíciles de unir, por ejemplo, con argón.
Un elemento consta de un solo tipo de átomo. Las partículas de los elementos pueden ser artificiales o hechas por el hombre. Diferentes arreglos de un átomo podrían conducir a diferentes versiones de ese elemento.
Por ejemplo, aunque el diamante y grafito son alótropos de carbono, son bastante diferentes en apariencia. Tienen la misma estructura química pero propiedades químicas diferentes.
Tabla de comparación
| Parámetros de comparación | molécula | Element |
|---|---|---|
| Los átomos | Las moléculas contienen átomos de elementos similares o diferentes. | Los elementos están constituidos por un solo tipo de átomo y, por lo tanto, no se pueden descomponer más. |
| División | Se puede dividir aún más usando medios químicos. | No se puede dividir más de ninguna manera. |
| Bonos | Forman enlaces iónicos o covalentes. | Pueden formar varios tipos de enlaces según la estabilidad y la configuración electrónica. |
| Miembros | Se compone de dos o más átomos unidos entre sí. | Actualmente hay 115 elementos químicos. |
| Ejemplos | Sus ejemplos son el agua, el óxido de carbono, el ozono, etc. | Sus ejemplos son nitrógeno, cobre, zinc, oxígeno, etc. |
¿Qué es Molécula?
La palabra molécula se refiere a los átomos que se mantienen unidos por fuertes enlaces químicos. Varían en tamaño dependiendo de los átomos conectados. Algunas moléculas están formadas por dos átomos similares y otras por enlaces complejos.
- Dos átomos de un elemento similar: Oxígeno (O2), formado por dos átomos de oxígeno
- Tres átomos de un elemento similar: Ozono(03), formado por tres átomos de oxígeno
- Unión compleja: Dióxido de carbono (CO2), formado por la unión de un átomo de carbono y dos átomos de oxígeno
Las moléculas pueden estar formadas por enlaces covalentes o enlaces iónicos. Un enlace covalente también se conoce como enlace compartido. En los enlaces covalentes, los átomos comparten sus electrones, mientras que en los enlaces iónicos, un átomo dona su electrón a otro átomo.
Un solo elemento no se considera una molécula. Por ejemplo, un solo elemento de oxígeno (O) o carbono (C) no es una molécula. Las moléculas se forman cuando dos o más átomos forman un enlace químico.
Algunas moléculas comunes son el ozono, el agua, la glucosa, etc.
Las moléculas se dividen en varias categorías, algunas de las cuales son moléculas homonucleares y heteronucleares, moléculas orgánicas o inorgánicas, moléculas diatómicas, triatómicas o poliatómicas, etc.

¿Qué es Elemento?
Los elementos son sustancias puras que no se pueden dividir ni descomponer en materia más simple. Pueden referirse a los átomos que tienen un número similar de protones en su núcleo. Pueden diferir en sus masas y neutrones.
Cuando los átomos que contienen elementos similares tienen un número distinto de neutrones, se denominan isótopos.
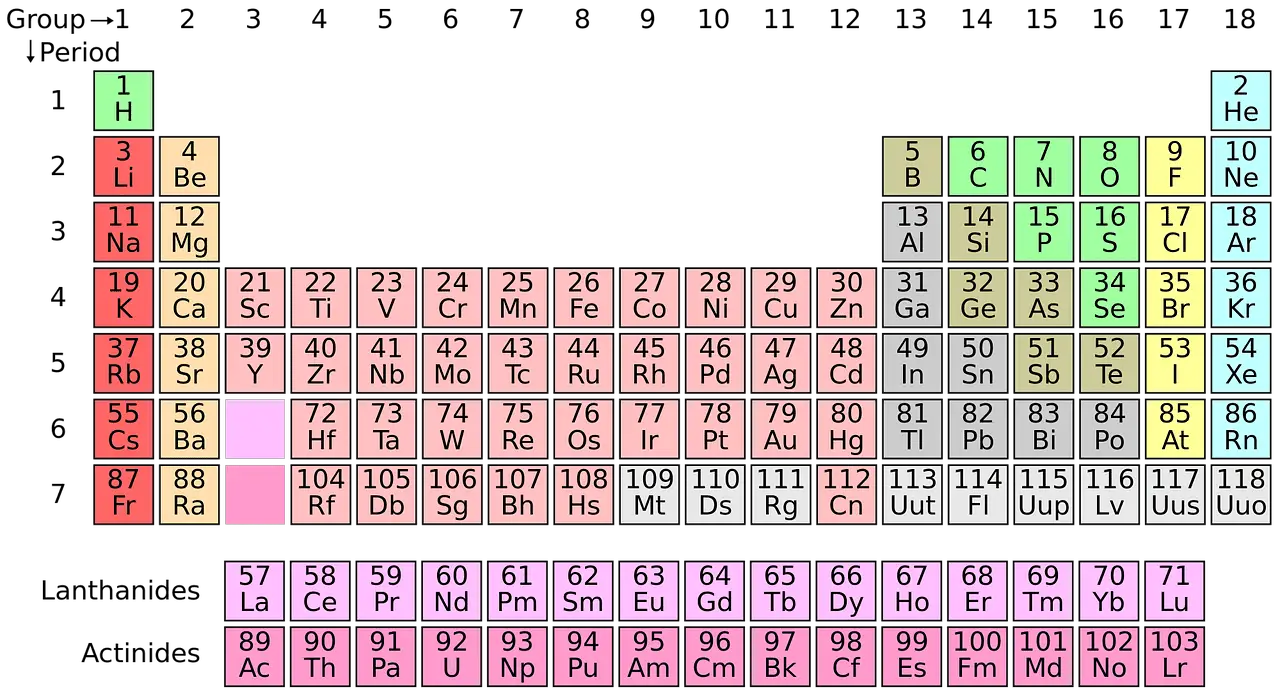
Hay 118 elementos haciendo su lugar en la tabla periódica. En la tabla periódica, los elementos se clasifican según sus características y número atómico.
Cada elemento tiene su símbolo atómico único, masa atómica, símbolo y disposición electrónica.
Surge la necesidad de clasificar los elementos en la tabla periódica. Se vuelve engorroso estudiar las propiedades de cada uno de los 118 elementos. Entonces, los científicos han desarrollado una forma de agrupar elementos de características similares.
Estas agrupaciones se realizan en base a cuatro bloques.
- bloque s: Los elementos del bloque s se clasifican en 2 grupos. Los elementos del grupo 1 se nombran como metales alcalinos, y los elementos del grupo 2 se nombran como alcalino metales de la tierra.
- bloque p: Los elementos del bloque p se clasifican en metales, no metales y metaloides.
- bloque d: Los elementos del bloque d constan de tres filas, a saber, la primera, segunda y tercera serie de transición.
- bloque f: f-block contiene un total de veintiocho elementos que se dividen en dos series iguales. La serie de los primeros catorce elementos se denomina serie de los lantánidos. El segundo conjunto de catorce elementos se denomina serie de actínidos.
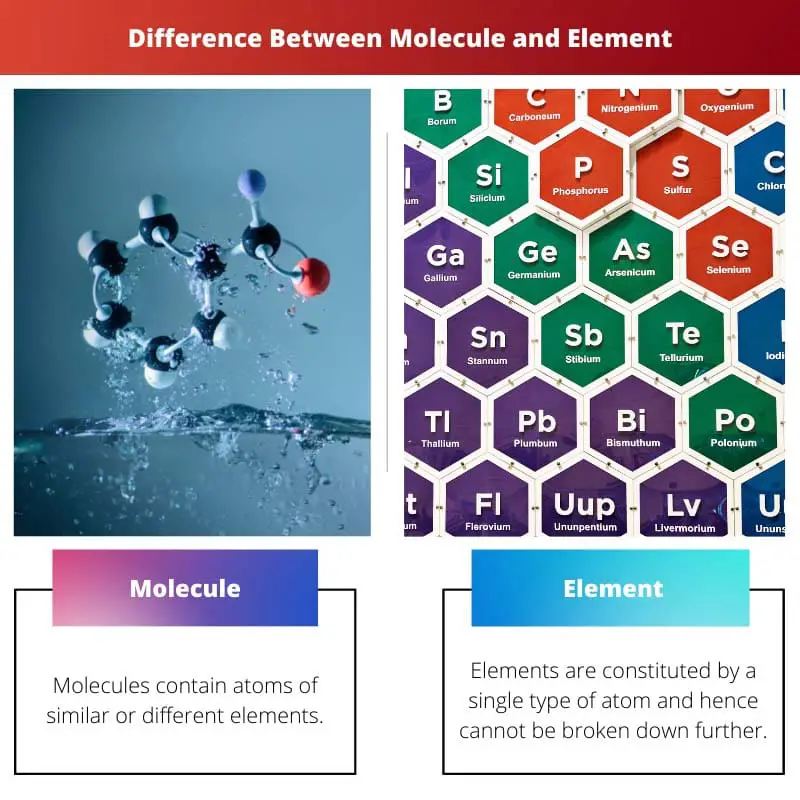
Principales diferencias entre molécula y elemento
- Una molécula puede ser homonuclear o heteronuclear, mientras que se dice que un elemento tiene un número atómico único.
- Las moléculas tienen átomos de elementos similares o diferentes, mientras que los elementos contienen solo átomos similares.
- Las moléculas y los elementos difieren en su configuración química. Las moléculas pueden formar un tipo específico de enlace, es decir, enlaces covalentes o iónicos. Por otro lado, los elementos pueden formar numerosos tipos de enlaces basados en la disposición de los electrones.
- La molécula es una sustancia que se puede dividir en sustancias más pequeñas, mientras que los elementos no se pueden dividir más por medios químicos.
- Los ejemplos de moléculas incluyen azúcar, glucosa, cloro, acetona, etc. Los ejemplos de elementos incluyen carbono, hidrógeno, helio, etc.
- https://www.sciencedirect.com/science/article/pii/S0166354201002224
- https://aip.scitation.org/doi/abs/10.1063/1.329173
Última actualización: 23 julio, 2023

Piyush Yadav ha pasado los últimos 25 años trabajando como físico en la comunidad local. Es un físico apasionado por hacer que la ciencia sea más accesible para nuestros lectores. Tiene una licenciatura en Ciencias Naturales y un Diploma de Postgrado en Ciencias Ambientales. Puedes leer más sobre él en su página de biografía.


La publicación proporciona una descripción general completa de las características y formaciones de moléculas y elementos, ofreciendo una comprensión detallada de los conceptos.
La descripción de los diferentes bloques de la tabla periódica es muy reveladora y proporciona una comprensión profunda de las clasificaciones de elementos.
La publicación captura efectivamente la distinción entre átomos, moléculas y elementos, agregando claridad a sus composiciones.
La explicación detallada de las diferencias entre moléculas y elementos es muy informativa y proporciona una comprensión clara de sus características.
Aprecio los ejemplos detallados proporcionados, que aclaran aún más los conceptos de moléculas y elementos.
La categorización de elementos en la tabla periódica se explica bien, lo que ayuda a comprender su agrupación según sus características.
La categorización de los elementos de la tabla periódica se describe acertadamente en la publicación y ofrece información valiosa sobre sus clasificaciones.
La explicación detallada de cada bloque de la tabla periódica facilita la comprensión de la agrupación de elementos.
Coincido con tu valoración, el post describe efectivamente la clasificación de elementos en función de sus características.
La publicación explica eficazmente las diferencias entre moléculas y elementos, ofreciendo una comprensión integral de sus estructuras y átomos.
La explicación detallada de lo que constituye un elemento y una molécula es muy informativa y añade profundidad a la publicación.
La publicación analiza las principales diferencias entre moléculas y elementos. Se explica la estructura y formación de ambos, y la importancia de estudiar sus propiedades.
Sí, la tabla comparativa proporciona una comprensión clara de las diferencias entre moléculas y elementos.
Estoy de acuerdo, esta publicación es muy informativa y está bien detallada.
La publicación explica las distinciones críticas entre moléculas y elementos. La explicación detallada proporciona una comprensión integral de su composición y estructura.
De acuerdo, la publicación proporciona una descripción clara de los átomos, moléculas y elementos.
Los ejemplos de moléculas y elementos mejoran aún más la comprensión de los conceptos discutidos en la publicación.
La publicación articula efectivamente las diferencias entre moléculas y elementos, junto con los detalles de su formación y propiedades.
En concreto, la tabla comparativa y las descripciones detalladas son muy útiles para comprender los conceptos.
La tabla de comparación detallada describe eficazmente las diferencias entre moléculas y elementos, proporcionando una comprensión profunda de sus propiedades y variaciones.
Estoy de acuerdo, la explicación de las propiedades y características de las moléculas y elementos es muy detallada e informativa.
La clasificación de elementos y sus propiedades se presentan de forma organizada, mejorando la comprensibilidad del post.
La comparación detallada entre moléculas y elementos es muy reveladora y proporciona una comprensión integral de sus estructuras y formaciones.
La categorización de moléculas basada en diferentes categorías es una valiosa adición a la publicación, ya que mejora la comprensión del tema.
La diferencia entre enlaces covalentes e iónicos en las moléculas está bien explicada en la publicación.
La explicación detallada de moléculas y elementos proporciona una comprensión profunda de su naturaleza y composición.