El mundo es un lugar hermoso. Las montañas, el mar, el cielo y todas las cosas que existen físicamente comprenden átomos.
Son los bloques de construcción del universo. Sin embargo, los átomos no son estables. Por lo tanto, se estabilizan haciendo moléculas e iones.
Puntos clave
- Una molécula es un grupo de dos o más átomos unidos químicamente, mientras que un ion es un átomo o molécula con carga eléctrica.
- Las moléculas son neutras, mientras que los iones pueden tener carga positiva o negativa.
- Las moléculas se forman a través de enlaces covalentes, mientras que los iones se forman a través de la transferencia de electrones entre átomos.
Molécula vs Ion
Las moléculas y los iones se diferencian porque una molécula no tiene carga neta, mientras que un ion sí. Esto sucede porque todo en este universo quiere alcanzar el equilibrio.
Los átomos hacen esto formando moléculas e iones. Además, las moléculas se desarrollan compartiendo electrones, mientras que los iones se forman debido al intercambio de electrones.
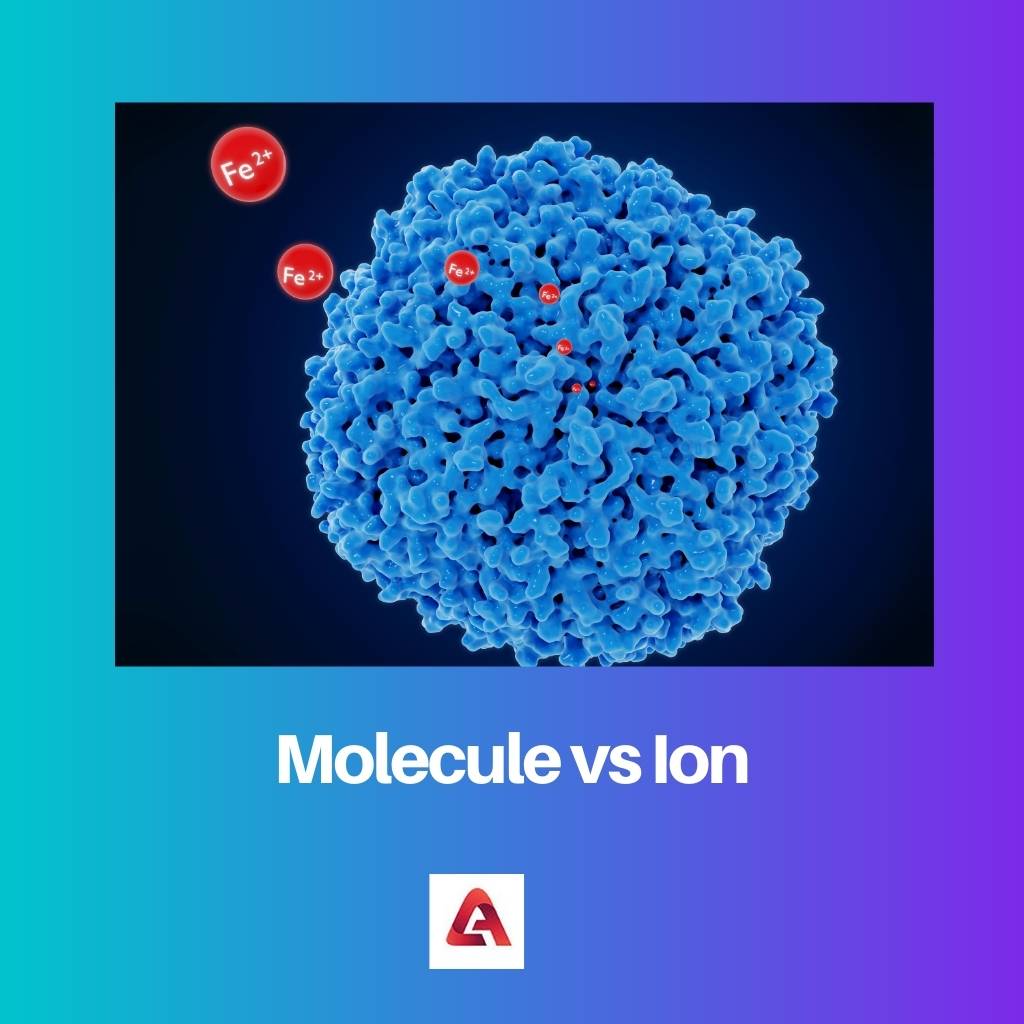
Uno o más átomos forman enlaces covalentes para convertirse en una molécula. La unidad más pequeña de la que está hecha una sustancia es una molécula. Una molécula conserva todas las propiedades químicas de la esencia. Los átomos representan moléculas, representadas mediante círculos, formando enlaces entre sí.
Una especie química con una carga neta positiva o negativa se conoce como ion. Un átomo y una molécula puede denominarse ion si tienen cuentas netas distintas de cero. Por lo tanto, todos los iones tienen más electrones que protones o más protones que electrones en su estructura molecular o atómica.
Tabla de comparación
| Parámetros de comparación | molécula | ion |
|---|---|---|
| distribución de electrones | Las moléculas se forman debido al intercambio de electrones entre dos o más átomos o por dos iones de carga opuesta. | Los iones se forman cuando los átomos ganan o pierden carga para lograr una configuración de gas noble. |
| Tamaño | El tamaño de la molécula depende del tamaño de los átomos o iones involucrados en la formación del enlace. | Los aniones son más significativos que las moléculas originales y los cationes son menos importantes que las moléculas originales. |
| Estabilidad | Las moléculas son más estables que los iones. | Los iones son menos estables que las moléculas. |
| Espiritual | Los enlaces covalentes o enlaces iónicos forman moléculas. | Los iones se forman por enlaces iónicos entre dos iones de carga opuesta y son más potentes que los covalentes. |
| Conducción de electricidad | Como las moléculas tienen carga neta cero, no son buenas conductoras de la electricidad. | Los iones son buenos conductores de electricidad. |
¿Qué es una molécula?
La unidad más pequeña de un compuesto, que muestra las propiedades químicas del compuesto, se conoce como molécula. Las moléculas constan de dos o más átomos unidos entre sí de forma covalente, es decir, comparten uno o más electrones.
Las moléculas comprenden la mayor parte de la tierra, y casi todas las sustancias orgánicas están hechas de moléculas.
Las moléculas pueden ser homonucleares y heteronucleares, lo que significa que comprenden elementos iguales o diferentes, respectivamente.
Un enlace covalente se forma cuando dos átomos con octetos incompletos comparten bits. Un enlace covalente transforma los diferentes átomos en una molécula.
Las moléculas consisten en átomos agrupados ya sea a través de enlaces covalentes o enlaces iónicos.
Las moléculas unidas covalentemente son más débiles que las moléculas unidas iónicamente. Esto sucede porque los enlaces iónicos tienen una poderosa fuerza electrostática que mantiene unidos a los iones.
Debido a esto, las moléculas iónicas son más estables que las moléculas unidas covalentemente.

¿Qué es un ion?
Un ion es una especie química con una carga neta positiva o negativa de cierta magnitud. Los iones se refieren a moléculas y átomos que tienen un control neto distinto de cero.
Por lo tanto, los iones tienen más protones que electrones o más electrones que protones en su estructura molecular o atómica.
Los iones que tienen un número más significativo de electrones que de protones y tienen una carga neta negativa se conocen como aniones.
Por el contrario, los iones con un número más significativo de protones que de electrones y con una carga neta positiva se conocen como cationes.
Los enlaces iónicos se forman solo cuando surgen fuerzas electrostáticas entre un anión con carga negativa y un catión con carga positiva.
Estas fuerzas electrostáticas atraen los aniones y cationes entre sí para estabilizar la carga neta. Estas fuerzas electrostáticas ayudan en la formación de compuestos ionicos.
Los iones formados por un solo elemento se denominan iones atómicos o monoatómicos. Los átomos participantes tienen alguna carga neta, ya sea positiva o negativa.
Mientras que si dos o más elementos están involucrados en un ion, se denominan iones moleculares o poliatómicos.
Principales diferencias entre moléculas e iones
- Las moléculas no tienen una carga neta, mientras que los iones tienen un control neto positivo o negativo.
- Las moléculas se forman cuando dos o más átomos comparten electrones para completar su octeto, mientras que los iones intercambian electrones y forman compuestos ionicos debido a las fuerzas electrostáticas.
- Dado que los iones se mantienen unidos por fuerzas electrostáticas, son mucho más estables que las moléculas formadas por enlaces covalentes.
- Debido a las altas fuerzas de atracción entre dos iones, tienen más energía de red que las moléculas unidas covalentemente.
- Debido a la mayor energía de la red, los iones son más estables que los enlazados covalentemente.
- El tamaño de las moléculas depende de los átomos involucrados en la formación de enlaces. Los cationes son más pequeños que sus moléculas originales, mientras que los aniones son más importantes que sus moléculas originales.

- https://ui.adsabs.harvard.edu/abs/1988STIA…8915174M/abstract
- https://pubs.acs.org/doi/pdf/10.1021/ja00260a006
Última actualización: 11 de junio de 2023

Piyush Yadav ha pasado los últimos 25 años trabajando como físico en la comunidad local. Es un físico apasionado por hacer que la ciencia sea más accesible para nuestros lectores. Tiene una licenciatura en Ciencias Naturales y un Diploma de Postgrado en Ciencias Ambientales. Puedes leer más sobre él en su página de biografía.

La tabla comparativa del artículo fue particularmente útil para comprender las distintas características de moléculas e iones. Es un gran punto de referencia para comparaciones rápidas.
Las comparaciones también me parecieron muy útiles. Es una manera conveniente de comprender rápidamente las principales disparidades entre moléculas e iones.
El artículo ofrecía una comparación exhaustiva de moléculas e iones, pero carecía de un enfoque más atractivo para que el contenido fuera más cautivador para los lectores.
Entiendo tu argumento. Si bien la información era valiosa, una narrativa más atractiva podría haber mejorado el atractivo general del artículo.
La tabla comparativa del artículo resumió efectivamente las principales diferencias entre moléculas e iones. Es una herramienta útil para repasar y reforzar los conceptos.
El artículo proporcionó una comprensión clara y concisa de las moléculas y los iones, lo que resulta valioso para los principiantes en el campo de la química.
Estoy de acuerdo. Es un buen punto de partida para cualquiera que sea nuevo en la química, pero podría haber incluido conceptos más avanzados para aquellos con una comprensión más profunda del tema.
Este artículo es una mirada fascinante al mundo de las moléculas y los iones. Las explicaciones detalladas y las comparaciones proporcionaron grandes ideas.
El artículo me pareció muy informativo y bien estructurado. Realmente me ayudó a comprender las diferencias entre moléculas e iones.
Estoy completamente de acuerdo. La información proporcionada es muy educativa e interesante.
El artículo hizo un buen trabajo al simplificar conceptos complejos, pero carecía de discusiones profundas sobre las propiedades químicas y el comportamiento de moléculas e iones.
Estoy de acuerdo con usted. Si bien el artículo proporcionó una descripción general, podría haber incluido información más detallada sobre las propiedades químicas de estas unidades fundamentales.
Las comparaciones proporcionadas fueron muy útiles para comprender las diferencias entre moléculas e iones. Agradezco la claridad en las explicaciones.
El artículo me pareció demasiado elemental. No ofrecía mucha profundidad para quienes buscaban información más avanzada.
No podría estar mas de acuerdo. La claridad y simplicidad del artículo lo convierten en un recurso valioso para cualquier persona interesada en la química.
Creo que el artículo destaca eficazmente las diferencias clave entre moléculas e iones, lo que facilita su comprensión para los expertos que no son expertos en química.
Creo que el artículo simplificó demasiado los conceptos de moléculas e iones. Podría haber profundizado en la química detrás de estos componentes fundamentales.
Entiendo su punto, pero para una descripción general, el artículo proporciona un buen punto de partida. Es importante hacer que los temas complejos sean accesibles a una amplia audiencia.
Las explicaciones fueron claras y concisas, lo que facilitó la comprensión de las diferencias entre moléculas e iones. El artículo proporcionó una base sólida para seguir aprendiendo.
La claridad de las explicaciones también me resultó muy útil. Es fantástico para desarrollar una comprensión sólida de estos conceptos.