Molekule i elementi sastoje se od atoma. Atomi su najsitnije jedinice koje se ne mogu pojednostaviti u manje materijale. Elementi su izvedeni iz svojstava atoma. Atomi čine temelje molekula i elemenata.
Važno je napraviti finu razliku između molekula i elemenata za proučavanje njihovih svojstava i prirode.
Ključni za poneti
- Element je čista tvar atoma s istim brojem protona.
- Molekula spaja dva ili više atoma koji se drže zajedno kemijskim vezama.
- Elementi se ne mogu rastaviti na jednostavnije tvari, dok se molekule mogu rastaviti na sastavne atome.
Molekula protiv elementa
Razlika između molekula i elemenata leži u njihovim svojstvima i tvorbi. Molekule se sastoje od dva ili više atoma koji tvore kemijske veze sličnih ili različitih elemenata. S druge strane, elementi imaju različite formacije. Sastoji se od jednog atoma. One se ne mogu podijeliti na jednostavnije tvari jer postoje u svom čistom obliku.

Molekule nastaju kemijskim povezivanjem dva ili više atoma. Kemijske veze nastaju izmjenom elektrona. Kada se atomi elemenata međusobno povežu, rezultiraju molekulama.
Atomi nekih elemenata mogu se lako povezati s, primjerice, klorom, dok se neki teško mogu povezati s, primjerice, argonom.
Element se sastoji od jedne vrste atoma. Čestice elemenata mogu biti umjetne ili stvorene od strane čovjeka. Različiti rasporedi atoma mogu dovesti do različitih verzija tog elementa.
Na primjer, iako je dijamant i grafit su alotropi ugljika, prilično su različiti po izgledu. Imaju istu kemijsku strukturu, ali različita kemijska svojstva.
Tabela za usporedbu
| Parametri usporedbe | Molekula | Element |
|---|---|---|
| atomi | Molekule sadrže atome sličnih ili različitih elemenata. | Elementi se sastoje od jedne vrste atoma i stoga se ne mogu dalje rastaviti. |
| Podjela | Može se dalje podijeliti kemijskim sredstvima. | Ne može se dalje dijeliti ni na koji način. |
| Okovi | Oni tvore ili ionske ili kovalentne veze. | Oni mogu tvoriti različite vrste veza ovisno o stabilnosti i elektroničkoj konfiguraciji. |
| članovi | Sastoji se od dva ili više atoma međusobno povezanih. | Trenutno postoji 115 kemijskih elemenata. |
| Primjeri | Njegovi primjeri su voda, ugljikov-d-oksid, ozon itd. | Njegovi primjeri su dušik, bakar, cink, kisik itd. |
Što je Molecule?
Riječ molekula odnosi se na atome koji se zajedno drže jakim kemijskim vezama. Razlikuju se u veličini ovisno o spojenim atomima. Neke molekule tvore dva slična atoma, a druge složene veze.
- Dva atoma sličnog elementa: Kisik (O2), formiran od dva atoma kisika
- Tri atoma sličnog elementa: Ozon(03), formiran od tri atoma kisika
- Složeno lijepljenje: Ugljik-dioksid (CO2), nastao spajanjem jednog atoma ugljika i dva atoma kisika
Molekule mogu biti formirane ili kovalentnim vezama ili ionskim vezama. Kovalentna veza je također poznata kao zajednička veza. U kovalentnim vezama atomi dijele svoje elektrone, dok u ionskim vezama atom daruje svoj elektron drugom atomu.
Pojedinačni element ne smatra se molekulom. Na primjer, jedan element kisika (O) ili ugljika (C) nije molekula. Molekule nastaju kada dva ili više atoma formiraju kemijsku vezu.
Neke uobičajene molekule su ozon, voda, glukoza itd.
Molekule se dijele na temelju nekoliko kategorija, od kojih su neke homonuklearne i heteronuklearne molekule, organske ili anorganske molekule, dvoatomne, troatomske ili poliatomske molekule itd.

Što je Element?
Elementi su čiste tvari koje se ne mogu dalje dijeliti ili rastaviti na jednostavniju materiju. Mogu se odnositi na atome koji imaju sličan broj protona u svojoj jezgri. Mogu se razlikovati po svojim masama i neutronima.
Kada atomi koji sadrže slične elemente imaju različit broj neutrona, oni se nazivaju izotopi.
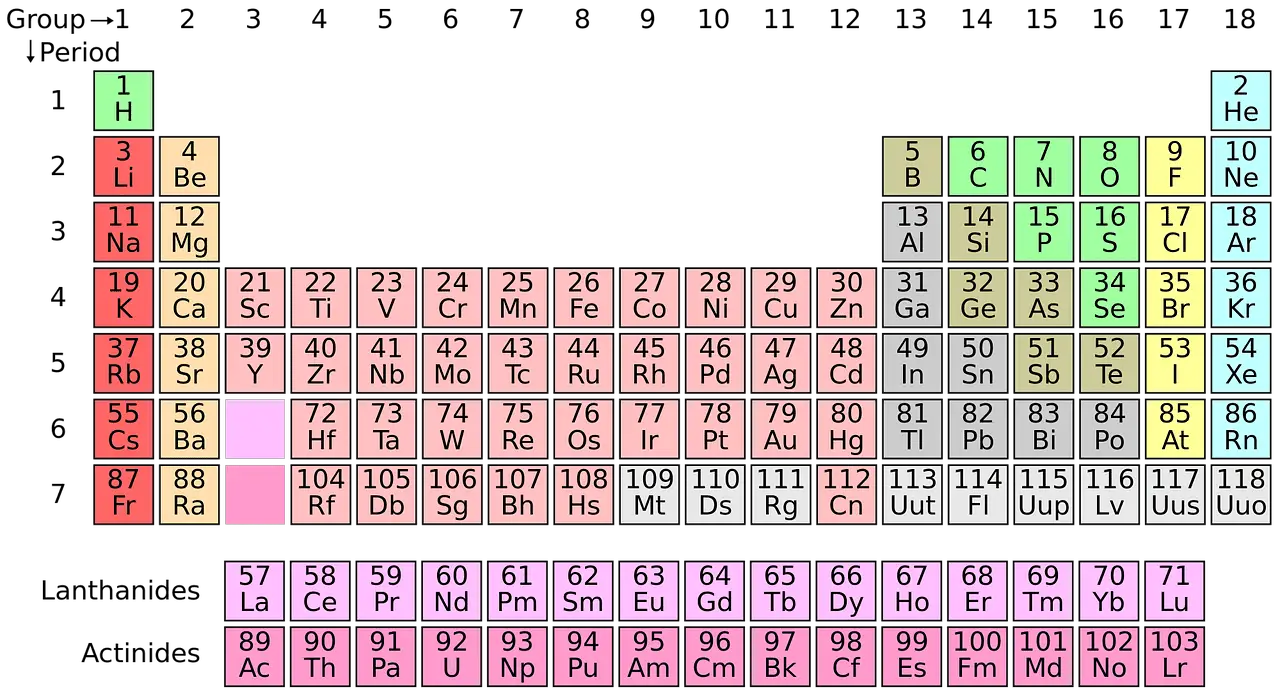
Postoji 118 elemenata koji zauzimaju svoje mjesto u periodnom sustavu. U periodnom sustavu elementi su klasificirani na temelju njihovih karakteristika i atomskog broja.
Svaki element ima svoj jedinstveni atomski simbol, atomsku masu, simbol i elektronički raspored.
Javlja se potreba za klasifikacijom elemenata u periodnom sustavu. Postaje glomazno proučavati svojstva svakog od 118 elemenata. Dakle, znanstvenici su razvili način grupiranja elemenata sličnih karakteristika.
Ova se grupiranja rade na temelju četiri bloka.
- s blok: s-blok elementi se svrstavaju u 2 grupe. Elementi skupine 1 nazivaju se alkalijski metali, a elementi skupine 2 nazivaju se kao lužični zemljani metali.
- p blok: p-blok elementi se kategoriziraju u metale, nemetale i metaloide.
- d blok: d-blok elementi sastoje se od tri reda, odnosno prve, druge i treće prijelazne serije.
- f blok: f-blok sadrži ukupno dvadeset i osam elemenata koji su podijeljeni u dva jednaka niza. Niz od prvih četrnaest elemenata naziva se niz lantanida. Drugi skup od četrnaest elemenata naziva se serija aktinida.
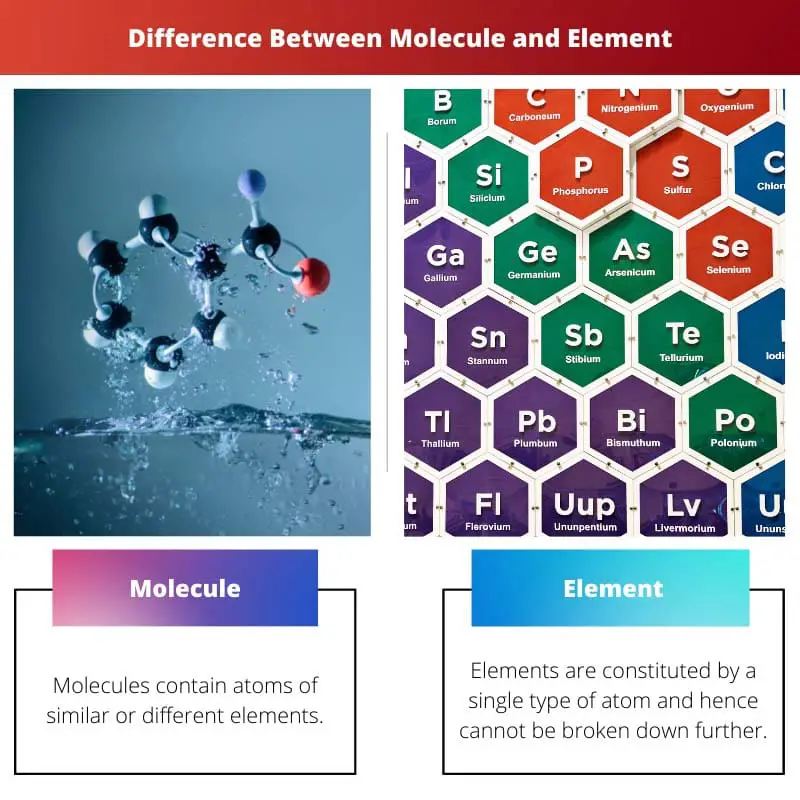
Glavne razlike između molekule i elementa
- Molekula može biti homonuklearna ili heteronuklearna, dok se za element kaže da ima jedinstveni atomski broj.
- Molekule imaju atome sličnih ili različitih elemenata, dok elementi sadrže samo slične atome.
- Molekule i elementi razlikuju se po svojoj kemijskoj konfiguraciji. Molekule mogu tvoriti određenu vrstu veze, tj. kovalentne ili ionske veze. S druge strane, elementi mogu formirati brojne vrste veza na temelju rasporeda elektrona.
- Molekula je tvar koja se može dalje dijeliti na manje tvari, dok se elementi ne mogu dalje dijeliti kemijskim putem.
- Primjeri molekula uključuju šećer, glukozu, klor, aceton, itd. Primjeri elemenata uključuju ugljik, vodik, helij itd.
- https://www.sciencedirect.com/science/article/pii/S0166354201002224
- https://aip.scitation.org/doi/abs/10.1063/1.329173
Zadnje ažuriranje: 23. srpnja 2023

Piyush Yadav proveo je posljednjih 25 godina radeći kao fizičar u lokalnoj zajednici. On je fizičar koji strastveno želi učiniti znanost dostupnijom našim čitateljima. Posjeduje diplomu prirodnih znanosti i poslijediplomski studij znanosti o okolišu. Više o njemu možete pročitati na njegovom bio stranica.


Post pruža opsežan pregled karakteristika i formacija molekula i elemenata, nudeći detaljno razumijevanje koncepata.
Opis različitih blokova u periodnom sustavu vrlo je pronicljiv i pruža temeljito razumijevanje klasifikacija elemenata.
Post učinkovito prikazuje razliku između atoma, molekula i elemenata, dodajući jasnoću njihovom sastavu.
Detaljno objašnjenje razlika između molekula i elemenata vrlo je informativno i omogućuje jasno razumijevanje njihovih karakteristika.
Cijenim pružene detaljne primjere koji dodatno pojašnjavaju koncepte molekula i elemenata.
Kategorizacija elemenata u periodnom sustavu je dobro objašnjena, što pomaže u razumijevanju njihovog grupiranja na temelju karakteristika.
Kategorizacija elemenata u periodnom sustavu prikladno je opisana u postu, nudeći dragocjene uvide u njihovu klasifikaciju.
Detaljno objašnjenje svakog bloka u periodnom sustavu olakšava razumijevanje grupiranja elemenata.
Slažem se s vašom procjenom, post učinkovito ocrtava klasifikaciju elemenata na temelju njihovih karakteristika.
Post učinkovito objašnjava razlike između molekula i elemenata, nudeći sveobuhvatno razumijevanje njihovih struktura i atoma.
Detaljno objašnjenje o tome što čini element kao i molekulu vrlo je informativno i daje dubinu postu.
Post govori o glavnim razlikama između molekula i elemenata. Objašnjava strukturu i formiranje oba, te važnost proučavanja njihovih svojstava.
Da, usporedna tablica pruža jasno razumijevanje razlika između molekula i elemenata.
Slažem se, ovaj je post vrlo informativan i detaljan.
Post objašnjava kritične razlike između molekula i elemenata. Detaljno objašnjenje pruža cjelovito razumijevanje njihovog sastava i strukture.
Slažem se, post pruža jasan pregled atoma, molekula i elemenata.
Primjeri molekula i elemenata dodatno poboljšavaju razumijevanje koncepata o kojima se govori u postu.
Post učinkovito artikulira razlike između molekula i elemenata, zajedno s detaljima njihove formacije i svojstava.
Usporedna tablica i detaljni opisi vrlo su korisni u razumijevanju koncepata.
Detaljna usporedna tablica učinkovito ocrtava razlike između molekula i elemenata, pružajući temeljito razumijevanje njihovih svojstava i varijacija.
Slažem se, objašnjenje svojstava i karakteristika molekula i elemenata vrlo je detaljno i informativno.
Klasifikacija elemenata i njihova svojstva prikazani su na organiziran način, čime se poboljšava razumljivost posta.
Detaljna usporedba između molekula i elemenata vrlo je pronicljiva, pruža sveobuhvatno razumijevanje njihovih struktura i formacija.
Kategorizacija molekula na temelju različitih kategorija vrijedan je dodatak postu, poboljšavajući razumijevanje teme.
Razlika između kovalentnih i ionskih veza u molekulama dobro je objašnjena u postu.
Detaljno objašnjenje molekula i elemenata omogućuje dubinsko razumijevanje njihove prirode i sastava.