Le molecole e gli elementi sono costituiti da atomi. Gli atomi sono l'unità più piccola che non può essere semplificata in materiali più piccoli. Gli elementi derivano dalle proprietà di un atomo. Gli atomi costituiscono il fondamento delle molecole e degli elementi.
È importante fare una sottile distinzione tra molecole ed elementi per studiarne le proprietà e la natura.
Punti chiave
- Un elemento è una sostanza pura di atomi con lo stesso numero di protoni.
- Una molecola unisce due o più atomi tenuti insieme da legami chimici.
- Gli elementi non possono essere scomposti in sostanze più semplici, mentre le molecole possono essere scomposte in atomi costituenti.
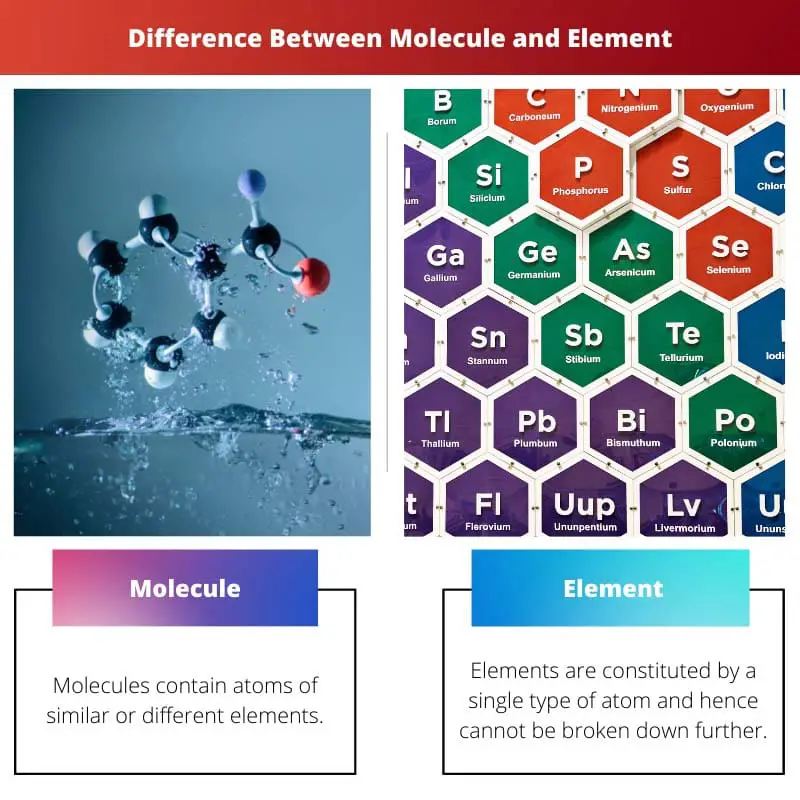
Molecola vs Elemento
La differenza tra molecole ed elementi sta nelle loro proprietà e formazione. Le molecole sono costituite da due o più atomi che formano legami chimici di elementi simili o dissimili. D'altra parte, gli elementi hanno formazioni diverse. Sono formati da un singolo atomo. Non possono essere fratelli in sostanze più semplici in quanto esistono nella loro forma pura.

Le molecole sono formate dal legame chimico di due o più atomi. I legami chimici sono formati dallo scambio di elettroni. Quando gli atomi degli elementi si legano tra loro, si traducono in molecole.
Gli atomi di alcuni elementi possono essere facilmente legati con, ad esempio, il cloro, mentre alcuni possono essere difficili da legare con, ad esempio, l'argon.
Un elemento è costituito da un singolo tipo di atomo. Le particelle degli elementi potrebbero essere artificiali o artificiali. Diverse disposizioni di un atomo potrebbero portare a diverse versioni di quell'elemento.
Ad esempio, sebbene diamante e grafite sono allotropi del carbonio, hanno un aspetto abbastanza diverso. Hanno la stessa struttura chimica ma proprietà chimiche diverse.
Tavola di comparazione
| Parametri di confronto | molecola | elemento |
|---|---|---|
| atomi | Le molecole contengono atomi di elementi simili o diversi. | Gli elementi sono costituiti da un solo tipo di atomo e quindi non possono essere scomposti ulteriormente. |
| Divisione | Può essere ulteriormente suddiviso utilizzando mezzi chimici. | Non può essere ulteriormente diviso in alcun modo. |
| Legami | Formano legami ionici o covalenti. | Possono formare vari tipi di legami a seconda della stabilità e della configurazione elettronica. |
| Utenti | Consiste di due o più atomi legati tra loro. | Ci sono attualmente 115 elementi chimici. |
| Esempi | I suoi esempi sono acqua, ossido di carbonio, ozono, ecc. | I suoi esempi sono azoto, rame, zinco, ossigeno, ecc. |
Cos'è la Molecola?
La parola molecola si riferisce agli atomi tenuti insieme da forti legami chimici. Hanno dimensioni variabili a seconda degli atomi collegati. Alcune molecole sono formate da due atomi simili e altre da legami complessi.
- Due atomi di un elemento simile: Ossigeno (O2), formato da due atomi di ossigeno
- Tre atomi di un elemento simile: Ozono(03), formato da tre atomi di ossigeno
- Legame complesso: Anidride carbonica (CO2), formata dal legame di un atomo di carbonio e due atomi di ossigeno
Le molecole possono essere formate da legami covalenti o legami ionici. Un legame covalente è anche noto come legame condiviso. Nei legami covalenti, gli atomi condividono i loro elettroni, mentre nei legami ionici, un atomo dona il suo elettrone a un altro atomo.
Un singolo elemento non è considerato una molecola. Ad esempio, un singolo elemento di ossigeno (O) o carbonio (C) non è una molecola. Le molecole si formano quando due o più atomi formano un legame chimico.
Alcune molecole comuni sono l'ozono, l'acqua, il glucosio, ecc.
Le molecole sono suddivise in base a diverse categorie, alcune delle quali sono molecole omonucleari ed eteronucleari, molecole organiche o inorganiche, molecole biatomiche, triatomiche o poliatomiche, ecc.

Cos'è l'elemento?
Gli elementi sono sostanze pure che non possono essere ulteriormente suddivise o scomposte in materia più semplice. Possono riferirsi agli atomi che hanno un numero simile di protoni nel loro nucleo. Possono differire nelle loro masse e neutroni.
Quando gli atomi contenenti elementi simili hanno un numero distinto di neutroni, vengono indicati come isotopi.
Ci sono 118 elementi che fanno il loro posto nella tavola periodica. Nella tavola periodica gli elementi sono classificati in base alle loro caratteristiche e al numero atomico.
Ogni elemento ha il suo unico simbolo atomico, massa atomica, simbolo e disposizione elettronica.
Sorge la necessità di classificare gli elementi nella tavola periodica. Diventa ingombrante studiare le proprietà di ciascuno dei 118 elementi. Quindi, gli scienziati hanno sviluppato un modo per raggruppare elementi con caratteristiche simili.
Questi raggruppamenti vengono eseguiti sulla base di quattro blocchi.
- blocco s: Gli elementi s-block sono classificati in 2 gruppi. Gli elementi del gruppo 1 sono denominati come metalli alcalini e gli elementi del gruppo 2 sono denominati come alcalino metalli terrestri.
- blocco p: Gli elementi p-block sono classificati in metalli, non metalli e metalloidi.
- blocco d: Gli elementi del blocco d sono costituiti da tre righe, vale a dire la prima, la seconda e la terza serie di transizione.
- blocco f: Il blocco f contiene un totale di ventotto elementi divisi in due serie uguali. La serie dei primi quattordici elementi è detta serie dei lantanidi. La seconda serie di quattordici elementi è chiamata serie degli attinidi.
Principali differenze tra molecola ed elemento
- Una molecola può essere omonucleare o eteronucleare, mentre un elemento è indicato come avente un numero atomico univoco.
- Le molecole hanno atomi di elementi simili o diversi, mentre gli elementi contengono solo atomi simili.
- Molecole ed elementi differiscono nella loro configurazione chimica. Le molecole possono formare un tipo specifico di legame, cioè legami covalenti o ionici. D'altra parte, gli elementi possono formare numerosi tipi di legami basati sulla disposizione degli elettroni.
- La molecola è una sostanza che può essere ulteriormente suddivisa in sostanze più piccole, mentre gli elementi non possono essere ulteriormente suddivisi con mezzi chimici.
- Esempi di molecole includono zucchero, glucosio, cloro, acetone, ecc. Esempi di elementi includono carbonio, idrogeno, elio, ecc.
- https://www.sciencedirect.com/science/article/pii/S0166354201002224
- https://aip.scitation.org/doi/abs/10.1063/1.329173
Ultimo aggiornamento: 23 luglio 2023

Piyush Yadav ha trascorso gli ultimi 25 anni lavorando come fisico nella comunità locale. È un fisico appassionato di rendere la scienza più accessibile ai nostri lettori. Ha conseguito una laurea in scienze naturali e un diploma post-laurea in scienze ambientali. Puoi leggere di più su di lui sul suo pagina bio.

Il post fornisce una panoramica completa delle caratteristiche e delle formazioni di molecole ed elementi, offrendo una comprensione dettagliata dei concetti.
La descrizione dei diversi blocchi nella tavola periodica è molto approfondita e fornisce una comprensione approfondita delle classificazioni degli elementi.
Il post cattura efficacemente la distinzione tra atomi, molecole ed elementi, aggiungendo chiarezza alle loro composizioni.
La spiegazione dettagliata delle differenze tra molecole ed elementi è altamente istruttiva e fornisce una chiara comprensione delle loro caratteristiche.
Apprezzo gli esempi dettagliati forniti, che chiariscono ulteriormente i concetti di molecole ed elementi.
La categorizzazione degli elementi nella tavola periodica è spiegata bene, aiutando a comprenderne il raggruppamento in base alle caratteristiche.
La categorizzazione degli elementi nella tavola periodica è opportunamente descritta nel post, offrendo preziosi spunti sulla loro classificazione.
La spiegazione dettagliata di ciascun blocco nella tavola periodica facilita la comprensione del raggruppamento degli elementi.
Sono d'accordo con la tua valutazione, il post delinea efficacemente la classificazione degli elementi in base alle loro caratteristiche.
Il post spiega efficacemente le differenze tra molecole ed elementi, offrendo una comprensione completa delle loro strutture e atomi.
La spiegazione dettagliata di ciò che costituisce un elemento e una molecola è altamente istruttiva e aggiunge profondità al post.
Il post discute le principali differenze tra molecole ed elementi. Spiega la struttura e la formazione di entrambi e l'importanza di studiarne le proprietà.
Sì, la tabella comparativa fornisce una chiara comprensione delle differenze tra molecole ed elementi.
Sono d'accordo, questo post è molto informativo e ben dettagliato.
Il post spiega le distinzioni critiche tra molecole ed elementi. La spiegazione dettagliata fornisce una comprensione completa della loro composizione e struttura.
D'accordo, il post fornisce una chiara panoramica di atomi, molecole ed elementi.
Gli esempi di molecole ed elementi migliorano ulteriormente la comprensione dei concetti discussi nel post.
Il post articola in modo efficace le differenze tra molecole ed elementi, insieme ai dettagli della loro formazione e proprietà.
Perfetto, la tabella comparativa e le descrizioni dettagliate sono molto utili per comprendere i concetti.
La tabella comparativa dettagliata delinea in modo efficace le differenze tra molecole ed elementi, fornendo una comprensione approfondita delle loro proprietà e variazioni.
Sono d'accordo, la spiegazione delle proprietà e delle caratteristiche delle molecole e degli elementi è molto dettagliata e istruttiva.
La classificazione degli elementi e le loro proprietà sono presentate in modo organizzato, migliorando la comprensibilità del post.
Il confronto dettagliato tra molecole ed elementi è molto approfondito e fornisce una comprensione completa delle loro strutture e formazioni.
La categorizzazione delle molecole in base a diverse categorie è una preziosa aggiunta al post, migliorando la comprensione dell'argomento.
La differenza tra legami covalenti e ionici nelle molecole è ben spiegata nel post.
La spiegazione dettagliata delle molecole e degli elementi fornisce una comprensione approfondita della loro natura e composizione.