De wereld is een prachtige plek. De bergen, de zee, de lucht en alle dingen die fysiek bestaan, bestaan uit atomen.
Het zijn de bouwstenen van het universum. Atomen zijn echter niet stabiel. Daarom stabiliseren ze zichzelf door moleculen en ionen te maken.
Key Takeaways
- Een molecuul is een groep van twee of meer atomen die chemisch aan elkaar zijn gebonden, terwijl een ion een atoom of molecuul is met een elektrische lading.
- Moleculen zijn neutraal, terwijl ionen positief of negatief geladen kunnen zijn.
- Moleculen worden gevormd door covalente binding, terwijl ionen worden gevormd door de overdracht van elektronen tussen atomen.
Molecuul versus ion
Moleculen en ionen verschillen omdat een molecuul geen netto lading heeft, terwijl een ion dat wel heeft. Dit gebeurt omdat alles in dit universum evenwicht wil bereiken.
Atomen doen dit door moleculen en ionen te vormen. Ook worden moleculen ontwikkeld door elektronen te delen, terwijl ionen worden gevormd door de uitwisseling van elektronen.
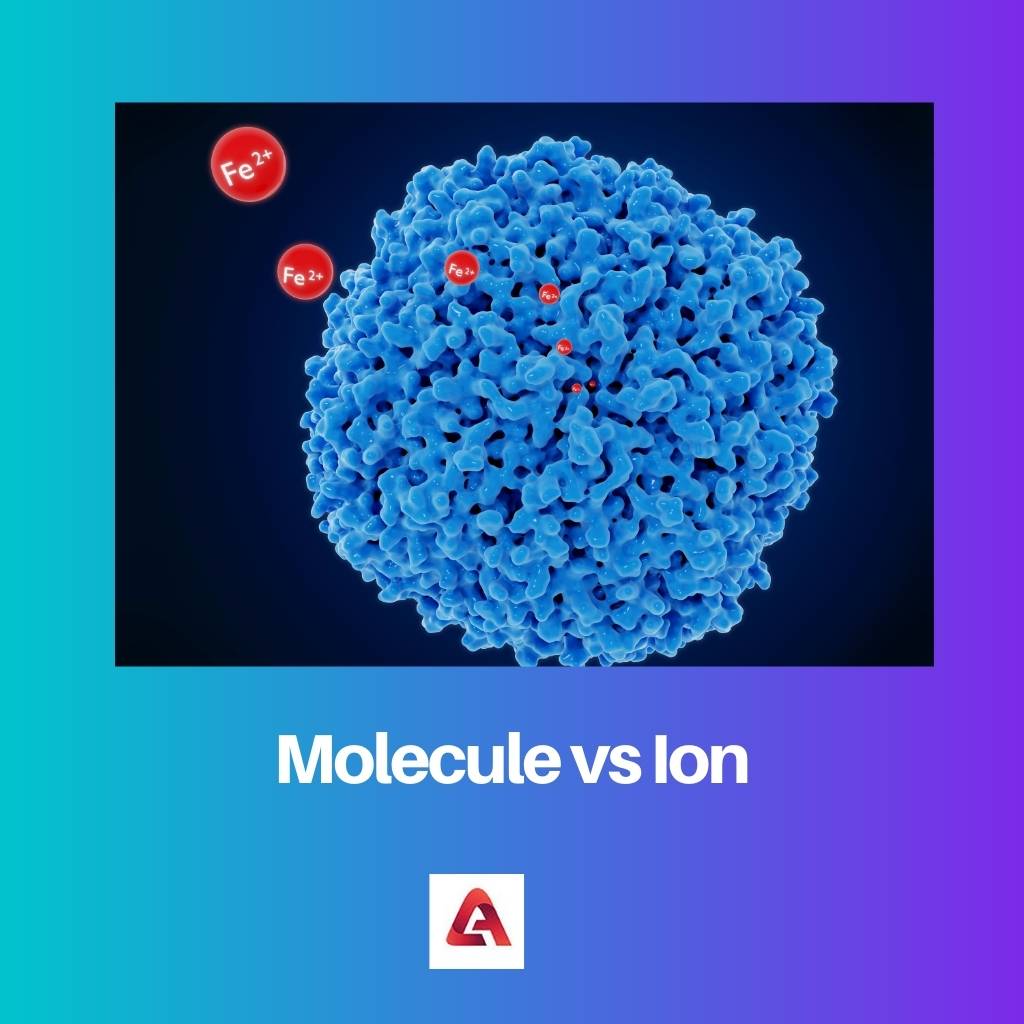
Een of meer atomen vormen covalente bindingen om een molecuul te worden. De kleinste eenheid waaruit een stof bestaat, is een molecuul. Een molecuul behoudt alle chemische eigenschappen van de essentie. Atomen stellen moleculen voor, weergegeven met behulp van cirkels, die samen bindingen vormen.
Een chemische soort met een netto positieve of negatieve lading staat bekend als een ion. Een atoom en een molecuul kan een ion worden genoemd als ze nettorekeningen hebben die niet nul zijn. Daarom hebben alle ionen ofwel meer elektronen dan protonen of meer protonen dan elektronen in hun moleculaire of atomaire structuur.
Vergelijkingstabel
| Parameters van vergelijking: | molecule | ion |
|---|---|---|
| Distributie van elektronen | Moleculen worden gevormd door het delen van elektronen tussen twee of meer atomen of door twee tegengesteld geladen ionen. | Ionen worden gevormd wanneer atomen lading krijgen of verliezen om een edelgasconfiguratie te bereiken. |
| Maat | De molecuulgrootte hangt af van de grootte van de atomen of ionen die betrokken zijn bij de bindingsvorming. | Anionen zijn belangrijker dan moedermoleculen en kationen zijn minder belangrijk dan moedermoleculen. |
| Stabiliteit | Moleculen zijn stabieler dan ionen. | Ionen zijn minder stabiel dan moleculen. |
| Training | Covalente bindingen of ionische bindingen vormen moleculen. | Ionen worden gevormd door ionische binding tussen twee ionen met tegengestelde lading en zijn krachtiger dan covalent. |
| Elektriciteitsgeleiding | Omdat moleculen geen netto lading hebben, zijn ze geen goede geleiders van elektriciteit. | Ionen zijn goede geleiders van elektriciteit. |
Wat is een molecuul?
De kleinste eenheid van een verbinding, die de chemische eigenschappen van de verbinding laat zien, staat bekend als een molecuul. Moleculen bestaan uit twee of meer atomen die covalent aan elkaar gebonden zijn, dwz ze delen een of meer elektronen.
Moleculen omvatten het grootste deel van de aarde en bijna alle organische stoffen zijn gemaakt van moleculen.
Moleculen kunnen homonucleair en heteronucleair zijn, wat betekent dat ze respectievelijk dezelfde of verschillende elementen bevatten.
Een covalente binding wordt gevormd wanneer twee atomen met onvolledige octetten bits delen. Een covalente binding transformeert de verschillende atomen in een molecuul.
Moleculen bestaan uit atomen die bij elkaar zijn gegroepeerd door middel van covalente bindingen of ionische bindingen.
De covalent gebonden moleculen zijn zwakker dan de ionische gebonden moleculen. Dit gebeurt omdat ionische bindingen een krachtige elektrostatische kracht hebben die de ionen bij elkaar houdt.
Hierdoor zijn ionische moleculen stabieler dan covalent gebonden moleculen.

Wat is een ion?
Een ion is een chemische soort met een netto positieve of negatieve lading van een bepaalde grootte. Ionen verwijzen naar moleculen en atomen die een niet-nul netto controle hebben.
Daarom hebben ionen ofwel meer protonen dan elektronen of meer elektronen dan protonen in hun moleculaire of atomaire structuur.
Ionen die een groter aantal elektronen hebben dan protonen en een netto negatieve lading hebben, worden anionen genoemd.
Omgekeerd staan ionen met een groter aantal protonen dan elektronen en met een netto positieve lading bekend als kationen.
Ionische bindingen worden alleen gevormd als er elektrostatische krachten optreden tussen een negatief geladen anion en een positief geladen kation.
Deze elektrostatische krachten trekken de anionen en kationen naar elkaar toe om de netto lading te stabiliseren. Deze elektrostatische krachten helpen bij de vorming van Ionische bestanddelen.
Ionen gemaakt van slechts één element worden atomaire of mono-atomaire ionen genoemd. De deelnemende atomen bevatten enige netto lading, positief of negatief.
Terwijl als twee of meer elementen bij een ion betrokken zijn, ze moleculaire of polyatomische ionen worden genoemd.
Belangrijkste verschillen tussen moleculen en ionen
- Moleculen hebben geen netto lading, terwijl ionen een netto positieve of negatieve controle hebben.
- Moleculen worden gevormd wanneer twee of meer atomen elektronen delen om hun octet te voltooien, terwijl ionen elektronen uitwisselen en vormen Ionische bestanddelen door elektrostatische krachten.
- Omdat ionen bij elkaar worden gehouden door elektrostatische krachten, zijn ze veel stabieler dan moleculen gevormd door covalente bindingen.
- Vanwege de hoge aantrekkingskracht tussen twee ionen hebben ze meer roosterenergie dan de covalent gebonden moleculen.
- Vanwege de hogere roosterenergie zijn ionen stabieler dan covalent gebonden.
- De grootte van moleculen hangt af van de atomen die betrokken zijn bij de bindingsformaties. Kationen zijn kleiner dan hun moedermoleculen, terwijl anionen belangrijker zijn dan hun moedermoleculen.

- https://ui.adsabs.harvard.edu/abs/1988STIA…8915174M/abstract
- https://pubs.acs.org/doi/pdf/10.1021/ja00260a006
Laatst bijgewerkt: 11 juni 2023

Piyush Yadav heeft de afgelopen 25 jaar als natuurkundige in de lokale gemeenschap gewerkt. Hij is een natuurkundige die gepassioneerd is om wetenschap toegankelijker te maken voor onze lezers. Hij heeft een BSc in natuurwetenschappen en een postdoctoraal diploma in milieuwetenschappen. Je kunt meer over hem lezen op zijn bio pagina.


De vergelijkingstabel van het artikel was bijzonder nuttig bij het begrijpen van de verschillende kenmerken van moleculen en ionen. Het is een geweldig referentiepunt voor snelle vergelijkingen.
Ik vond de vergelijkingen ook erg nuttig. Het is een handige manier om snel de belangrijkste verschillen tussen moleculen en ionen te begrijpen.
Het artikel bood een alomvattende vergelijking van moleculen en ionen, maar het ontbrak aan een boeiendere aanpak om de inhoud boeiender te maken voor de lezers.
Ik begrijp je punt. Hoewel de informatie waardevol was, had een boeiender verhaal de algehele aantrekkingskracht van het artikel kunnen vergroten.
De vergelijkingstabel van het artikel vatte effectief de belangrijkste verschillen tussen moleculen en ionen samen. Het is een handig hulpmiddel om de concepten te herzien en te versterken.
Het artikel gaf een duidelijk en beknopt inzicht in moleculen en ionen, wat waardevol is voor beginners op het gebied van de chemie.
Daar ben ik het mee eens. Het is een goed startpunt voor iedereen die nieuw is in de scheikunde, maar het had meer geavanceerde concepten kunnen bevatten voor mensen met een dieper begrip van het onderwerp.
Dit artikel is een fascinerende kijk in de wereld van moleculen en ionen. De gedetailleerde uitleg en vergelijkingen leverden geweldige inzichten op.
Ik vond het artikel zeer informatief en goed gestructureerd. Het heeft me echt geholpen de verschillen tussen moleculen en ionen te begrijpen.
Ik ben het er helemaal mee eens. De geboden informatie is zeer leerzaam en interessant.
Het artikel slaagde er goed in complexe concepten te vereenvoudigen, maar het ontbeerde diepgaande discussies over de chemische eigenschappen en het gedrag van moleculen en ionen.
Ik ben het met je eens. Hoewel het artikel een algemeen overzicht gaf, had het meer gedetailleerde inzichten in de chemische eigenschappen van deze fundamentele eenheden kunnen bevatten.
De verstrekte vergelijkingen waren zeer nuttig bij het begrijpen van de verschillen tussen moleculen en ionen. Ik waardeer de duidelijkheid in de uitleg.
Ik vond het artikel een beetje te elementair. Het bood niet veel diepgang voor wie op zoek was naar meer geavanceerde informatie.
Ik ben het daar volledig mee eens. De duidelijkheid en eenvoud van het artikel maken het tot een waardevolle bron voor iedereen die geïnteresseerd is in scheikunde.
Ik denk dat het artikel effectief de belangrijkste verschillen tussen moleculen en ionen benadrukt, waardoor het gemakkelijker te begrijpen is voor niet-chemie-experts.
Ik denk dat het artikel de concepten van moleculen en ionen te simpel heeft gemaakt. Er had dieper ingegaan kunnen worden op de chemie achter deze fundamentele bouwstenen.
Ik begrijp uw punt, maar voor een algemeen overzicht biedt het artikel een goed startpunt. Het is belangrijk om complexe onderwerpen toegankelijk te maken voor een breed publiek.
De uitleg was duidelijk en beknopt, waardoor het gemakkelijker werd om de verschillen tussen moleculen en ionen te begrijpen. Het artikel bood een sterke basis voor verder leren.
Ik vond de duidelijkheid van de uitleg ook erg nuttig. Het is geweldig voor het opbouwen van een goed begrip van deze concepten.