A tabela periódica da química é algo que os alunos estão sendo solicitados a memorizar tediosamente, mesmo sem saber o motivo real por trás de aprendê-la. Para algumas pessoas, é apenas um tópico incluído em seu currículo.
Mas, na verdade, essa pequena tabela periódica é muito mais importante do que isso; é um roteiro que abre um milhão de oportunidades para cientistas e pesquisadores em todo o mundo. Dmitri Mendeleyev é o inventor da tabela periódica.
Antes dele, muitos se esforçaram para organizar os elementos químicos de maneiras diferentes. Mas o resultado de Dmitri foi aceito mundialmente.
Nas abreviações científicas, as linhas são chamadas de Períodos e as colunas de Grupos, respectivamente.
Principais lições
- Períodos são as linhas horizontais na tabela periódica, indicando o número de camadas de elétrons nos átomos de um elemento, com elementos no mesmo período tendo estruturas atômicas semelhantes.
- Grupos são as colunas verticais da tabela periódica, consistindo de elementos com o mesmo número de elétrons em sua camada externa, o que leva a propriedades químicas semelhantes.
- Tanto os períodos quanto os grupos organizam os elementos da tabela periódica, com períodos representando linhas horizontais baseadas em camadas de elétrons e grupos representando colunas verticais baseadas em elétrons de camada externa e propriedades químicas.
Período vs Grupo
Um período é uma linha horizontal que vai do lado esquerdo para o lado direito da tabela periódica, e a eletronegatividade aumenta através dela. Um grupo é uma vertical coluna que vai do topo da tabela periódica para baixo, e a eletronegatividade aumenta de baixo para cima.

Durante o tempo de arranjo, Mendeleyev deixou algumas linhas vazias com a impressão de que alguns outros elementos entrariam em um futuro próximo. E surpreendentemente, um dos elementos que se encaixou nessa lacuna foi Gálio.
Tabela de comparação
| Parâmetro de Comparação | de Payback | Grupo |
|---|---|---|
| Direção | Períodos são as linhas horizontais na tabela periódica moderna | Grupos são as colunas verticais que percorrem o topo da tabela periódica |
| Propriedades | Os elementos em um período não têm propriedades semelhantes. | Os elementos em cada grupo têm algumas propriedades semelhantes, mas não propriedades idênticas. |
| Semelhança | Elementos no mesmo período têm um número igual de composição de elétrons | Elementos em cada grupo têm um número igual de elétrons de valência |
| Soma | Existem 7 períodos na tabela periódica | O grupo contém 18 elementos dispostos verticalmente na tabela periódica moderna. |
| Eletro-negatividade | Aumenta da esquerda para a direita. | Ele aumenta de baixo para cima em um grupo. |
O que é Período?
Um período é uma linha horizontal da extrema esquerda para a extrema direita na tabela periódica. A partir de agora, existem 7 períodos na tabela periódica.
Um novo período começa quando um novo nível de energia fundamental se soma aos elétrons. Cada elemento em um período provavelmente terá um número igual de orbitais atômicos.
Por exemplo - cada elemento no 1st período tem apenas 1 orbital por seus elétrons, 2nd período inclui 2 orbitais para os elétrons. Da mesma forma, os orbitais continuam aumentando à medida que você desce na linha.
O tamanho do elemento diminui à medida que você se move ao longo de um período, pois o número de camadas de elétrons permanece constante, mas o número de prótons aumenta no núcleo. É por isso que o átomo fica mais pesado, mas o tamanho continua diminuindo.
Olhando para a tabela periódica, você veria diferentes elementos encaixados em cada linha. O 1º período tem apenas 2 elementos (1 e 18), o 2º e 3º períodos têm 8 elementos cada, o 4º e 5º períodos têm 18 elementos e o 6º e 7º períodos têm 32 elementos cada, respectivamente.
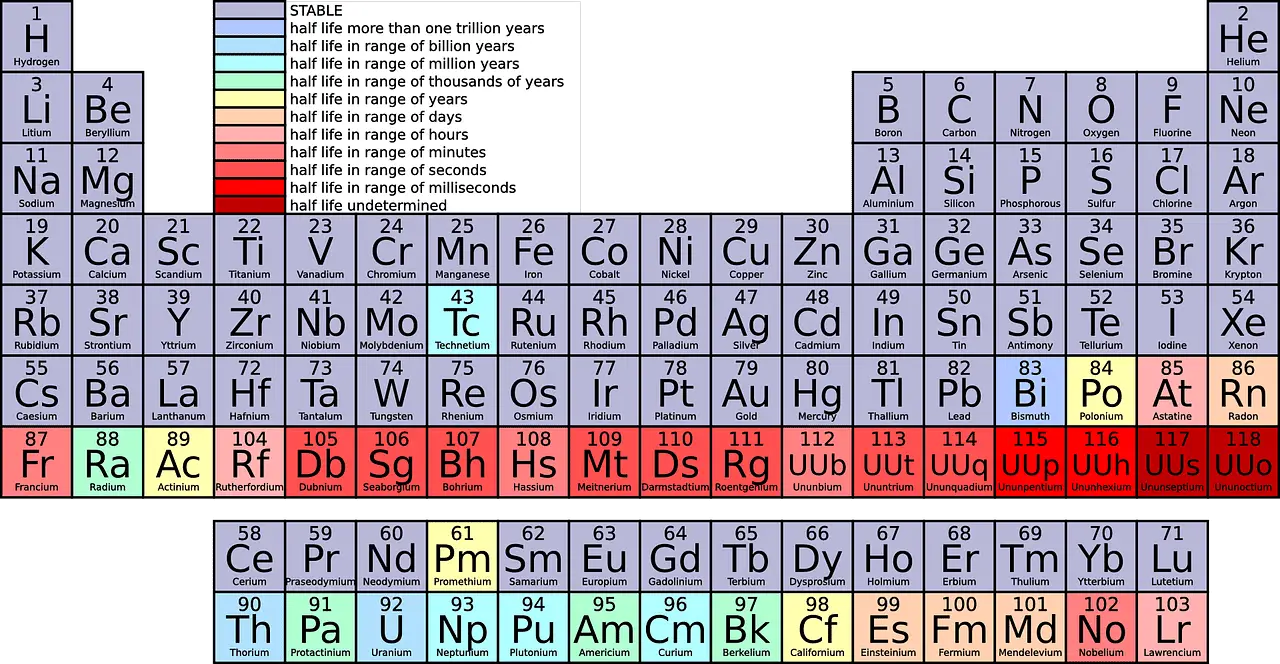
O que é Grupo?
Contando de cima para baixo, existem 18 grupos na tabela periódica. Todos os grupos recebem nomes distintos.
Os grupos são categorias mistas de metais, não metais e semimetais, agrupados em famílias de acordo com suas propriedades semelhantes. Por exemplo, o grupo 1 pertence à família do lítio, classificado como metais alcenos.
Da mesma forma, cada grupo na raia tem seu nome de família. Os elementos do grupo relacionado têm características semelhantes porque têm a mesma contagem de elétrons em suas camadas mais externas.
O tamanho do elemento aumenta conforme você move qualquer grupo para baixo. Isso ocorre porque um grande número de prótons e nêutrons existe no núcleo.
Além disso, uma camada extra de elétrons torna o átomo mais pesado. Para grupos, existem duas maneiras diferentes de ilustrar os elementos.
Compreender os dois sistemas de numeração é essencial porque a tabela periódica aparece em ambos os formatos. Nos Estados Unidos, eles usaram as letras A&B para indicar cada elemento do grupo, mas, infelizmente, foi observado como um sistema de numeração desorganizado.
Para eliminar todas as possíveis confusões, o International União de Química Pura e Aplicada (IUPAC) Teve a ideia de numerar os elementos como (1,2, 3… 18). No entanto, ambos os sistemas de numeração são aceitáveis. Mas a numeração da IUPAC parece bem organizada e direta.
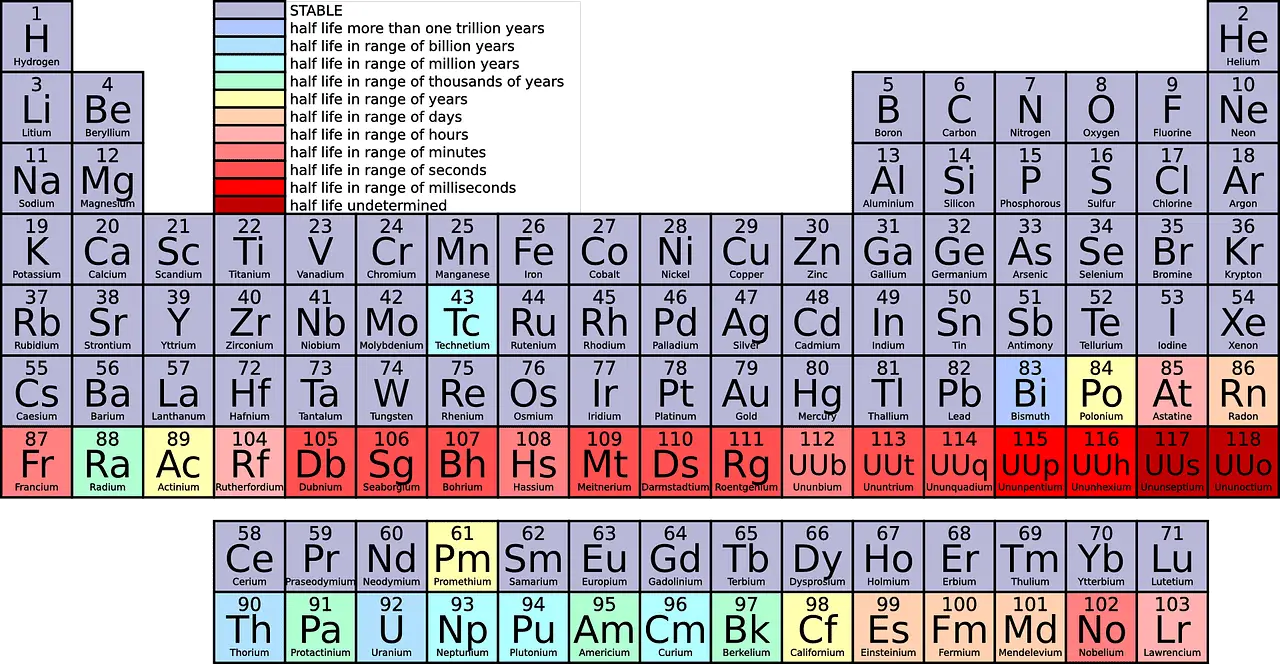
Principais diferenças entre Período e Grupo
- Locação: Os grupos são a coluna vertical, enquanto os períodos são as linhas retas na tabela periódica.
- Número: Há um total de 18 grupos e 7 períodos na tabela periódica, entre os quais os grupos são categorizados em diferentes famílias e tipos de metais.
- Propriedades quimicas: Todos os elementos do grupo têm propriedades químicas ou físicas análogas, enquanto os períodos compartilham a mesma hierarquia de elétrons.
- Nível de energia: À medida que descemos no grupo de cima para baixo, o nível de energia dos elétrons aumenta. Por outro lado, em cada período, o nível de energia do elétron permanece o mesmo.
- Eletro-negatividade: Isso declina de cima para baixo em um grupo e sobe da esquerda para a direita em um período. Esta é uma consideração essencial ao estudar a tabela periódica.

Última atualização: 11 de junho de 2023

Piyush Yadav passou os últimos 25 anos trabalhando como físico na comunidade local. Ele é um físico apaixonado por tornar a ciência mais acessível aos nossos leitores. Ele é bacharel em Ciências Naturais e pós-graduado em Ciências Ambientais. Você pode ler mais sobre ele em seu página bio.


Ótimo artigo! Isso dá uma ótima visão sobre a importância da tabela periódica. Eu realmente gostei disso!
Estou muito feliz que você tenha achado útil. Eu fiz também!
Com certeza, todo estudante de ciências deveria ler isso.
Postagem muito informativa. Deveríamos pressionar por uma melhor educação e compreensão dos tópicos científicos.
É exatamente disso que precisamos.
Este é apenas mais um exemplo de padrões educacionais desatualizados. Deveríamos estar ensinando tópicos mais relevantes aos alunos.
Acredito que é de vital importância que os alunos entendam a tabela periódica.
Essa é uma opinião controversa, Joel.
Acho que as pessoas subestimam o valor da tabela periódica. Deveríamos estar fazendo mais para melhorar nosso ensino sobre isso.
Com certeza, este é um ponto importante.
Acho realmente interessante que uma tabela aparentemente tão simples possa conter tantas informações valiosas.
Sim, é bastante fascinante.
Isto é esclarecedor. A tabela periódica está subestimada.
Esta foi uma leitura muito necessária para começar o meu dia!
Alguns pontos válidos apresentados aqui, mas ainda não estou convencido da importância da tabela periódica.
Concordo com você, Zach.
A tabela periódica é a pedra angular da química e deve ser tratada como tal.
Eu não poderia concordar mais.
Discordo, acredito que o ensino da tabela periódica da forma atual está ultrapassado e deveria ser revisto.
Posso ver por que alguns podem considerá-lo desatualizado, mas é realmente vital para o desenvolvimento científico.
Entendo o que você está dizendo, mas não concordo totalmente.
Embora eu compreenda a importância da tabela periódica, é difícil argumentar que o sistema educacional atual seja adequado.
Você levantou um ponto importante, Erin.