Xeton và andehit là hai loại phân tử hữu cơ. Chúng có thể được sản xuất nhân tạo, tuy nhiên, có một số chất tự nhiên. Có thể cả hai đã nhầm lẫn vì thành phần hóa học của chúng.
Cả hai đều có một nhóm carbonyl và là hợp chất hữu cơ. Nguyên tử carbon trong nhóm này sở hữu một liên kết hydroxyl đôi. Điều này chỉ ra rằng một cấu hình phẳng lượng giác trong xeton và andehit bao quanh nguyên tử cacbonyl cacbon.
Tuy nhiên, có sự khác biệt đáng kể giữa hai loại chức năng và mục đích của bài luận này là giúp bạn phân biệt giữa chúng.
Chìa khóa chính
- Anđehit chứa một nhóm cacbonyl liên kết với một nguyên tử hiđro, trong khi xeton có một nhóm cacbonyl liên kết với hai nguyên tử cacbon.
- Aldehyd thể hiện khả năng phản ứng cao hơn ketone do có nguyên tử hydro, khiến chúng dễ bị tấn công nucleophin hơn.
- Aldehyd trải qua quá trình oxy hóa dễ dàng hơn ketone, tạo thành axit cacboxylic và rượu tương ứng.
Anđehit vs Xeton
Aldehyd được biết đến là các hợp chất hữu cơ hoặc axit bao gồm một liên kết đôi carbon và oxy với hai nhóm aryl hoặc nhóm alkyl xung quanh hai liên kết của nguyên tử carbon carbonyl. Xeton là hợp chất hữu cơ có liên kết đôi giữa cacbon và oxi (C=O). Lưỡng cực của cacbonyl cacbon có hai nhóm metyl gắn với nó trong xeton.

Anđehit là hợp chất phân tử chứa nhóm chức có công thức CHO, bao gồm trung tâm cacbonyl liên kết với H và bất kỳ nhóm ankyl bazơ hoặc nhóm R có chiều dài chuỗi nào. Một nhóm aldehyde hoặc formyl là nhóm chức năng hoàn toàn.
Xeton (/kiton/) là một hợp chất chứa hóa sinh có công thức R2C=O, trong đó R có thể là bất kỳ phối tử chứa cacbon nào. Các nhóm carbonyl được tìm thấy trong các phân tử xeton.
Acetone (R = R' = dimetyl) là từ xeton cơ bản nhất, với công thức CH3C(O)CH3. Xeton có vai trò quan trọng trong hóa học sinh học cũng như trong công nghiệp.
Ví dụ như nhiều loại đường (ketose), nhiều hormone (ví dụ như testosterone) và dung môi acetone.
Bảng so sánh
| Các thông số so sánh | Anđehit | Ketones |
|---|---|---|
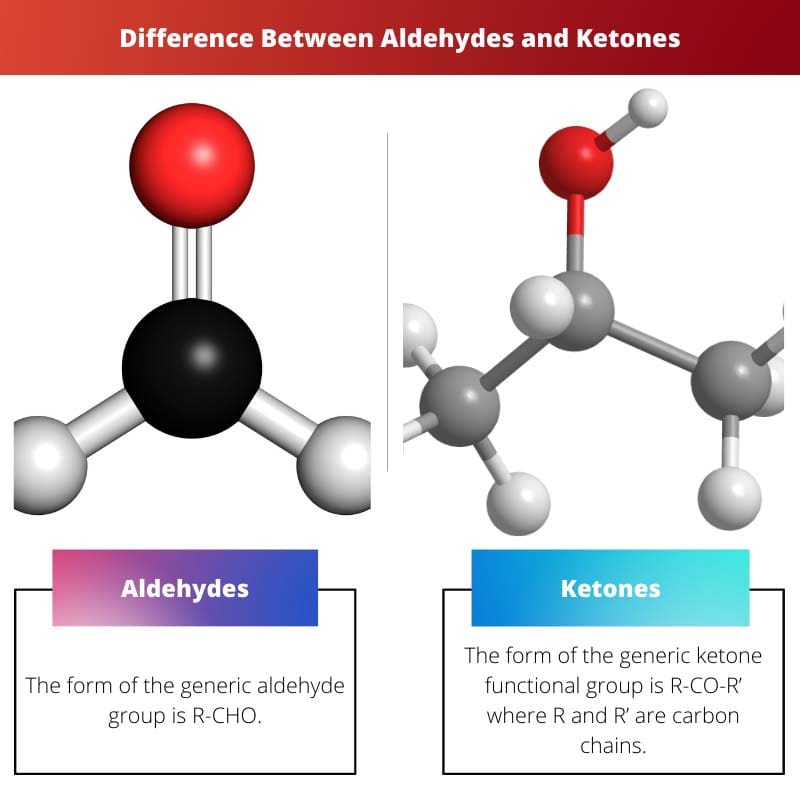
| Structure | Hình thức của nhóm aldehyde chung là R-CHO. | Dạng của nhóm chức ketone chung là R-CO-R' trong đó R và R' là các chuỗi cacbon. |
| Định nghĩa | Anđehit là hợp chất phân tử có chứa nhóm chức có công thức CHO. | Xeton là một hợp chất chứa trong hóa sinh có công thức R2C=O, trong đó R có thể là bất kỳ phối tử chứa cacbon nào |
| Cường độ phản ứng | Rất phản ứng | Ít phản ứng hơn |
| Xảy ra | Đầu cuối của một chuỗi carbon. | Luôn xảy ra ở giữa chuỗi carbon. |
| Thử nghiệm của Fehling | Xuất hiện kết tủa đỏ hồng. | Không phản ứng |
| Thử nghiệm của Tollen | thu được kết tủa đen. | Không áp dụng |
| Thử nghiệm natri hydroxit | Kết tủa dạng gel màu nâu. | Không áp dụng |
| Kết quả kiểm tra của Schiff | Màu hồng. | Không màu. |
Andehit là gì?
Andehit là một nhóm chức năng công nghiệp và sinh hóa quan trọng bao gồm một nguyên tử cacbon liên kết với một nguyên tử hydro và sau đó liên kết đôi với một nguyên tử oxy (công thức hóa học O=CH-).
Rượu đã được khử hydro dường như là nguồn gốc của thuật ngữ aldehyde. Aldehyd đã từng được gọi theo rượu mà chúng có liên quan, chẳng hạn như aldehyde rượu cho acetaldehyde.
(Vinous xuất phát từ tiếng Latin vinum, có nghĩa là rượu vang, góp phần vào sự khởi đầu của ethanol) Họ andehit có cực. Bởi vì oxy ít điện dương hơn carbon, nên nó thu hút các electron bên trong liên kết carbon-oxy.
Nó liên kết với một nguyên tử hydro ở đầu đối diện. Formaldehyde được coi là loại aldehyde cơ bản nhất.
Việc formaldehyde đi chệch khỏi phương trình thông thường bằng cách sở hữu một nguyên tử hydro chứ không phải nhóm R là điều khiến nó trở nên phổ biến.
Nhóm carbonyl được kết nối với hai nguyên tử H trong formaldehyde, aldehyd cơ bản nhất. Cacbocation được liên kết với một nhóm hydro nhưng một nhóm carbon khác trong nhiều andehit khác.
Carbocation của một aldehyd được biểu thị dưới dạng CHO theo khía cạnh của các công thức bền vững. Phương trình của formaldehyd là HCHO, trong khi phương trình của acetaldehyde là CH3CHO.
Xeton là gì?
Thuật ngữ xeton xuất phát từ tiếng Đức cổ aketon, có nghĩa là “axeton”. Các ký hiệu xeton được tạo ra bằng cách thay đổi hậu tố -ane của ankan ban đầu thành -anyone, theo hướng dẫn danh pháp IUPAC.
Mặc dù vị trí của nhóm chức carbonyl nucleophile được biểu thị bằng một số, nhưng những tên gọi truyền thống không thể đo lường được của các xeton nổi bật nhất, chẳng hạn như axeton cũng như benzophenone, vẫn được sử dụng rộng rãi.
Các liên kết ketone CH gần với carbonyl có tính axit cao hơn nhiều (pKa 20) so với các tương tác CH alkane (pKa 50). Sự khác biệt này là do sự ổn định cộng hưởng của ion điện di sau khi phân ly.
Độ ph tương đối của hydro rất quan trọng trong quá trình enol hóa xeton và các chất khác quá trình oxy hóa sản phẩm.
Do tính axit của -hydrogen, xeton và các sản phẩm oxy hóa khác có thể phản ứng với tư cách là chất xúc tác với tỷ lệ mol và bazơ xúc tác tại vị trí đó.
Các nhóm thế trong xeton được sử dụng để phân loại chúng. Sự tương đương của hai nhóm metyl hữu cơ kết nối với lõi carbonyl phân biệt xeton thành các dẫn xuất đối xứng và không đối xứng, theo một cách phân loại chung.
Axeton (C6H5C(O)C6H5) là một xeton đối xứng, cũng như benzophenon (C6H5C(O)C6H5). Acetophenone là một ketone có cấu trúc không đối xứng.
Sự khác biệt chính giữa Aldehyd và Ketone
- Aldehyd là một nhóm chức phản ứng mạnh hơn nhóm ketone.
- Aldehyd nằm ở đầu hoặc cuối chuỗi carbon, trong khi nhóm ketone xuất hiện ở giữa chuỗi carbon.
- Trong thử nghiệm của Schiff, aldehyd tạo ra màu hồng, trong khi ketone không tạo ra màu.
- Andehit tạo ra kết tủa màu đen, trong khi xeton không tạo ra phản ứng nào đối với phép thử này.
- Cấu trúc của aldehyd là R-CHO, trong khi cấu trúc của ketone là R-CO-R'.
Cập nhật lần cuối: ngày 11 tháng 2023 năm XNUMX

Piyush Yadav đã dành 25 năm qua làm việc với tư cách là một nhà vật lý trong cộng đồng địa phương. Anh ấy là một nhà vật lý đam mê làm cho khoa học dễ tiếp cận hơn với độc giả của chúng tôi. Ông có bằng Cử nhân Khoa học Tự nhiên và Bằng Sau Đại học về Khoa học Môi trường. Bạn có thể đọc thêm về anh ấy trên trang sinh học.


Bài tiểu luận này cung cấp một cái nhìn tổng quan rõ ràng và toàn diện về aldehyd và xeton, khiến nó trở thành nguồn tài liệu quý giá cho những cá nhân đang tìm kiếm kiến thức chi tiết về hóa học hữu cơ. Các lời giải thích có cấu trúc tốt và sâu sắc.
Bài viết này cung cấp sự khác biệt rõ ràng giữa aldehyd và ketone, mang đến sự hiểu biết sâu sắc hơn về cấu trúc hóa học và khả năng phản ứng của chúng. Các tài liệu tham khảo được cung cấp hỗ trợ độ tin cậy của thông tin.
Hiểu được sự khác biệt giữa aldehyd và ketone là điều cần thiết trong hóa học hữu cơ. Bài viết này khám phá một cách hiệu quả các tính chất và đặc điểm riêng của từng hợp chất hóa học này.
Tôi đánh giá cao bảng so sánh chi tiết trình bày sự khác biệt về cấu trúc và phản ứng giữa aldehyd và xeton. Đó là một tài liệu tham khảo rất hữu ích cho sinh viên hóa học và các chuyên gia.
Aldehyd và xeton là hai loại phân tử hữu cơ quan trọng, với sự khác biệt về khả năng phản ứng và cấu trúc phân tử khiến chúng trở nên khác biệt. Bài viết này cung cấp một lời giải thích kỹ lưỡng về sự khác biệt giữa chúng.
Phân tích chuyên sâu về tính chất và đặc điểm của aldehyd và xeton mang lại nhiều thông tin hữu ích. Bài viết làm rõ một cách hiệu quả những đặc điểm độc đáo của các hợp chất hữu cơ này.
Việc giải thích cặn kẽ về sự khác biệt về cấu trúc và khả năng phản ứng giữa aldehyd và xeton giúp nâng cao kiến thức của những người đam mê hóa học. Bảng so sánh chi tiết đặc biệt làm sáng tỏ.
Thông tin toàn diện được cung cấp trong bài tiểu luận này cho phép người đọc xác định những khác biệt chính giữa aldehyd và xeton. Nó có giá trị cho những ai quan tâm đến hóa học hữu cơ.