Dalam Kimia, senyawa yang berbeda dibentuk oleh berbagai jenis ikatan antar molekul.
Berbagai faktor menentukan jenis ikatan apa yang harus dibentuk antara molekul yang berbeda, dan jenis molekul memainkan peran besar dalam pembentukan ikatan tersebut.
Ikatan adalah gaya tarik menarik yang bekerja antara dua molekul.
Pengambilan Kunci
- Ikatan ionik terbentuk antara logam dan nonlogam melalui transfer elektron, sedangkan ikatan kovalen terbentuk antara nonlogam melalui penggunaan bersama elektron.
- Senyawa ionik memiliki titik leleh dan titik didih yang tinggi, sedangkan senyawa kovalen memiliki titik leleh dan titik didih yang lebih rendah.
- Senyawa ionik menghantarkan listrik ketika dilarutkan dalam air atau meleleh, tetapi senyawa kovalen tidak.
Ikatan Ionik vs Ikatan Kovalen
Ikatan ion terbentuk antara atom melalui transfer elektron, menciptakan ion yang tertarik satu sama lain karena muatannya berlawanan. Ikatan kovalen melibatkan pembagian elektron antar atom, menciptakan daya tarik timbal balik yang menyatukan atom.
Ikatan ionik terbentuk dalam kasus senyawa ionik. Senyawa ionik terbuat dari molekul yang mengandung ion bermuatan, yang dapat bermuatan positif atau negatif.
Jadi ini menciptakan gaya tarik-menarik antar molekul karena muatan yang berlawanan saling tarik-menarik. Gaya tarik-menarik ini menghasilkan pembentukan ikatan.
Ikatan kovalen terbentuk antara non-logam. Jenis ikatan ini terbentuk karena pembagian elektron antara dua molekul.
Karena salah satu molekul dalam senyawa kovalen kekurangan elektron, ia menerima jumlah elektron yang diperlukan dari molekul donor untuk membuat senyawa kovalen yang stabil.
Tabel perbandingan
| Parameter Perbandingan | Ikatan ionik | Ikatan kovalen |
|---|---|---|
| Penciptaan | Ikatan ion terbentuk karena transfer ion antar molekul | Ikatan kovalen terbentuk karena penggunaan bersama elektron antara dua molekul |
| Keadaan senyawa | Senyawa yang terbentuk hanya ada dalam keadaan padat | Senyawa yang terbentuk ada di semua keadaan materi |
| Jenis molekul | Ikatan terjadi antara logam dan non-logam | Ikatan terjadi antara dua non-logam |
| Polaritas | Senyawa ionik bersifat nonpolar | Senyawa kovalen bersifat polar |
| melting Point | Senyawa ionik memiliki titik leleh yang lebih tinggi | Senyawa kovalen memiliki titik leleh yang lebih rendah |
Apa itu Ionic Bond?
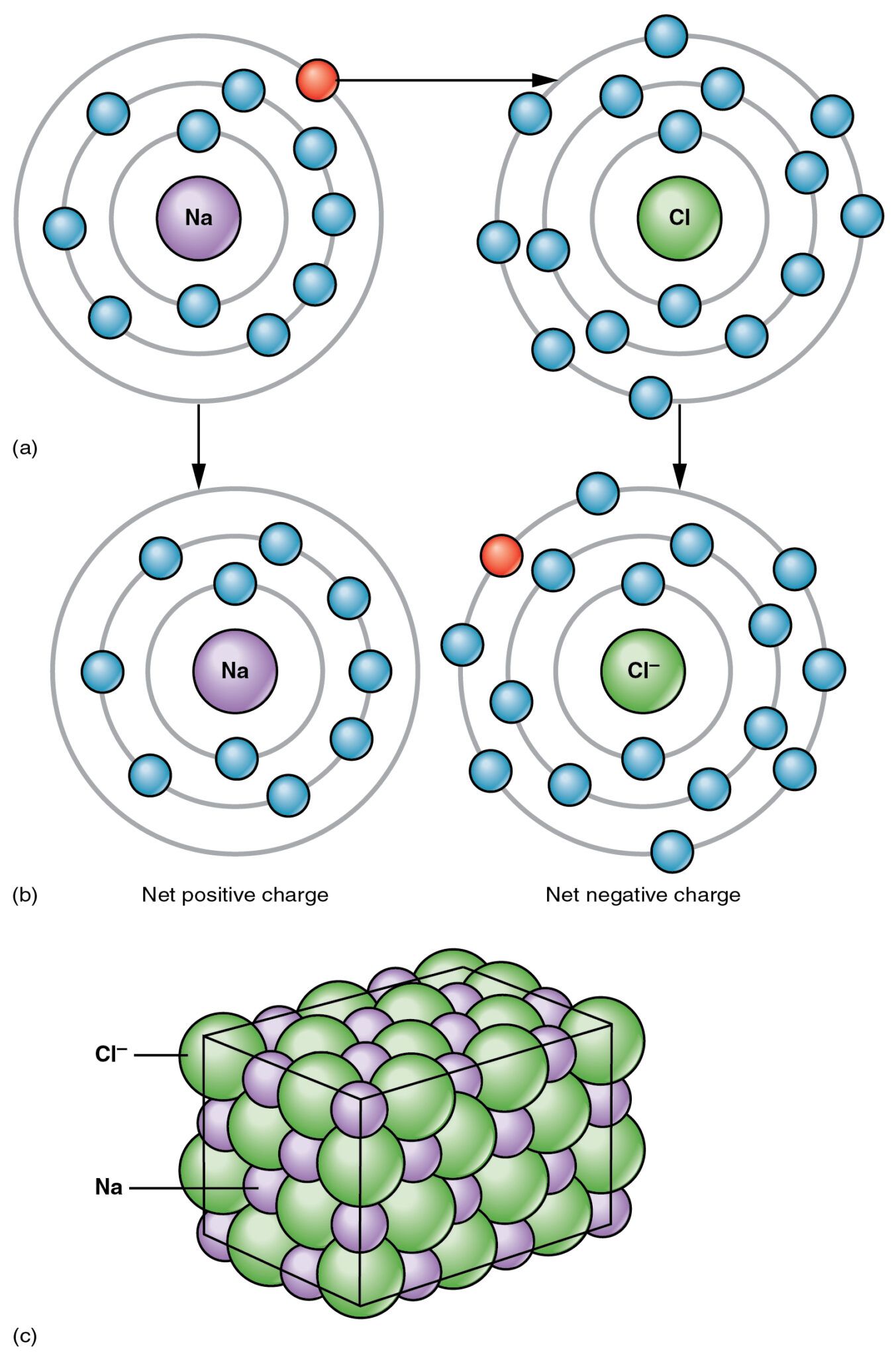
Ikatan ionik adalah salah satu dari tiga jenis ikatan yang terjadi antar molekul, membentuk senyawa ionik.
Ikatan terjadi antara logam dan nonlogam, dan salah satu contoh paling umum dari senyawa tersebut adalah garam (NaCl), di mana Natrium (Na) adalah logam dan Klorin (Cl) adalah nonlogam.
Ini adalah ikatan yang kuat dan tidak dapat dipatahkan semudah ikatan kovalen. Ikatan terjadi karena adanya penggunaan bersama elektron antara logam dan nonlogam.
Salah satu molekul dalam senyawa ionik kekurangan elektron, sedangkan molekul lainnya kaya elektron, menciptakan gaya tarik-menarik antara dua molekul.
Gaya tarik elektrostatik menghasilkan interaksi antara dua molekul, berbagi elektron dari atom yang kaya elektron ke atom yang kekurangan elektron.
Atom atau molekul donor sepenuhnya mentransfer atom ke molekul atau atom penerima, menghasilkan ikatan yang kuat dan bersih antara kedua molekul.
Karakteristik senyawa ionik tersebut adalah titik lelehnya yang tinggi dan konduktivitas listrik yang tinggi dalam keadaan cair atau terlarut. Senyawa ionik juga sangat larut dalam air.
Apa itu Ikatan Kovalen?
Ikatan kovalen adalah jenis ikatan kimia antara molekul yang mengarah pada pembentukan senyawa kovalen.
Ini adalah yang terlemah dari tiga jenis ikatan kimia, dan molekul dalam senyawa kovalen dapat dengan mudah dipisahkan.
Ikatan kovalen terbentuk antara dua non-logam, dan ikatan logam molekul tergantung pada jumlah kulit valensi elektron.
Ikatan terjadi dengan berbagi pasangan elektron, dan pembagian elektron ini terjadi untuk menjaga keseimbangan kimia antara molekul atau atom.
Pembagian elektron antara dua molekul yang tidak stabil menciptakan kulit valensi yang stabil di kedua molekul.
Ketika kedua atom telah mencapai keadaan valensi penuhnya, ikatan terbentuk antara dua atom atau molekul.
Pasangan elektron bersama hadir di antara kedua atom untuk menjaga stabilitas senyawa.
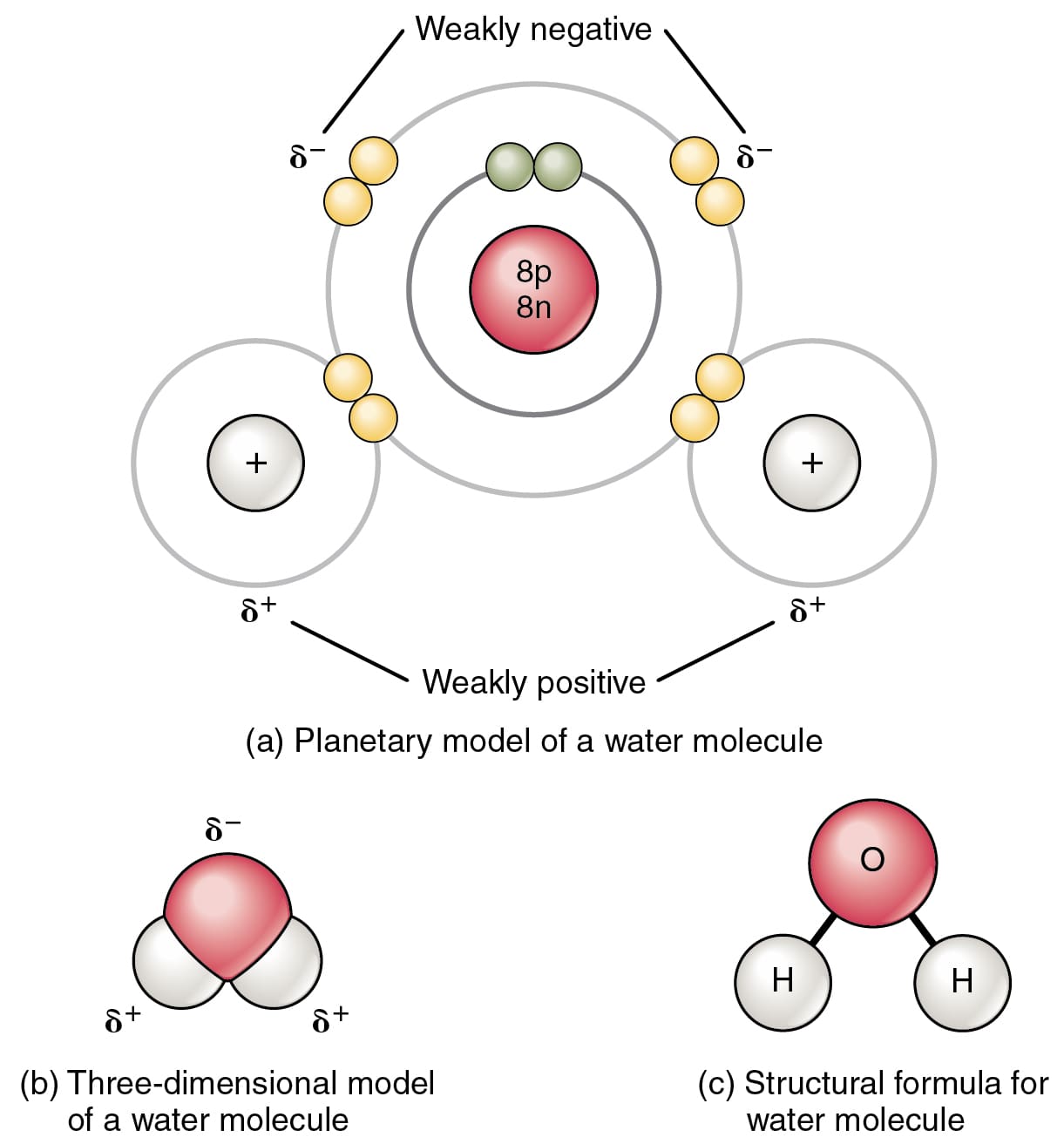
Contoh paling umum dari ikatan kovalen adalah antara dua atom Hidrogen dalam molekul H2.
Dalam molekul H2, dua atom Hidrogen berbagi dua elektron yang mengarah ke ikatan kovalen.
Faktor kunci yang diperlukan untuk pembentukan ikatan kovalen adalah keelektronegatifan molekul. Dua atom dengan keelektronegatifan yang sama menghasilkan ikatan kovalen.
Perbedaan Utama Antara Ionik dan Ikatan Kovalen
- Ikatan ion terbentuk karena transfer ion antar molekul. Ikatan kovalen terbentuk karena penggunaan bersama elektron antar atom.
- Senyawa ionik hanya ada dalam keadaan padat. Senyawa kovalen hadir di semua keadaan materi.
- Ikatan ionik terbentuk antara logam dan nonlogam. Ikatan kovalen terbentuk antara dua non-logam.
- Senyawa ion bersifat non polar, sedangkan senyawa kovalen bersifat polar
- Senyawa ionik memiliki titik leleh yang sangat tinggi, sedangkan senyawa kovalen memiliki titik leleh yang rendah.
- https://link.springer.com/article/10.1007/s00214-007-0282-x
- https://journals.aps.org/pr/abstract/10.1103/PhysRev.168.905
Terakhir Diperbarui : 14 Juni 2023

Piyush Yadav telah menghabiskan 25 tahun terakhir bekerja sebagai fisikawan di masyarakat setempat. Dia adalah fisikawan yang bersemangat membuat sains lebih mudah diakses oleh pembaca kami. Dia memegang gelar BSc dalam Ilmu Pengetahuan Alam dan Diploma Pasca Sarjana dalam Ilmu Lingkungan. Anda dapat membaca lebih lanjut tentang dia di nya halaman bio.


Informasi menarik tentang ikatan ionik dan kovalen, jumlah informasi yang dirinci dalam artikel ini luar biasa dan sangat mudah dipahami
Artikel menarik. Saya mengapresiasi pembahasan mendalam tentang ciri-ciri senyawa ionik dan kovalen.
Saya tidak setuju. Ikatan kovalen belum tentu merupakan ikatan terlemah di antara ketiga jenis ikatan kimia. Ada beberapa kasus di mana ikatan ini lebih kuat daripada ikatan ionik.
Hal ini benar dalam keadaan tertentu, namun secara umum, pernyataan tersebut berlaku. Obligasi kovalen dianggap paling lemah karena mudahnya pemutusan ikatan tersebut.
Penjelasan yang sangat bagus tentang ikatan ionik dan kovalen. Saya berharap dapat membaca lebih banyak dari penulis ini.
Ya, postingannya sangat informatif dan mudah dimengerti. Saya menghargai tabel perbandingan untuk merangkum perbedaan antara kedua jenis obligasi tersebut.
Artikel ini menyederhanakan topik tetapi tampaknya referensi datanya sangat kurang. Kredibilitas lebih dapat diberikan dengan kutipan yang tepat
Saya setuju. Saya memeriksa referensi yang diberikan dan itu adalah sumber yang dapat dipercaya.
Saya menemukan informasinya sangat membantu, terutama untuk ujian kimia saya yang akan datang
Penulis sepertinya sangat berpengetahuan dalam bidang Kimia. Saya menikmati membaca postingan mendetail seperti ini.
Sepakat. Tabel perbandingan sangat membantu dalam menyoroti perbedaan antara ikatan ionik dan kovalen.
Artikel tersebut menjelaskan topik-topik yang sangat berguna untuk pembelajaran pendahuluan.
Posting ini memberikan gambaran komprehensif tentang ikatan ionik dan kovalen. Contoh-contoh yang diberikan sangat membantu dalam memahami konsep.
Informasi memadai yang berharga untuk tujuan pendidikan. Wajib dibaca oleh siswa sekolah menengah
Tabel perbandingan adalah cara yang bagus untuk mengilustrasikan perbedaannya, bagi siapa pun yang memiliki pengetahuan dasar kimia, artikel ini bisa menjadi sumber yang bagus.
Saya setuju. Poin-poin penting yang dapat diambil juga cukup membantu dan menyederhanakan konsep.
Artikel ini menyajikan perbedaan antara ikatan ionik dan kovalen dengan jelas. Saya merasa ini sangat berguna.