Zinātne mūsu ikdienas dzīvē satur daudz aspektu. Visu, ko redzam ar neapbruņotu aci, veido miljardiem atomu un molekulu.
Ķīmijas valodā procesu, kurā atomi saskaras viens ar otru un veido objektus, sauc par ķīmisko saiti.
Atslēgas
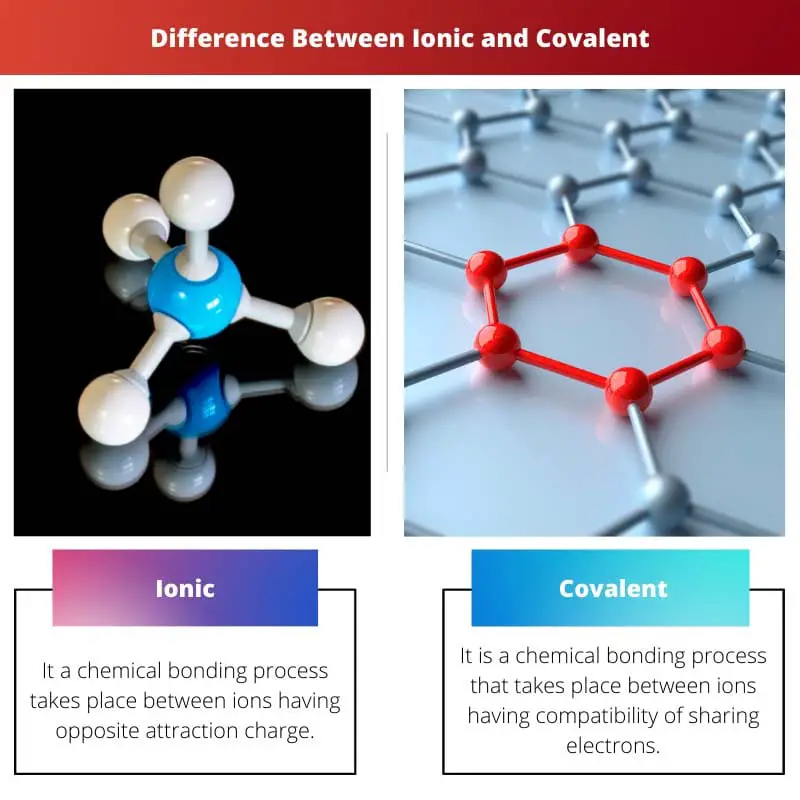
- Jonu saites veidojas, kad atomi pārnes elektronus, radot lādētus jonus, kas piesaista viens otru, savukārt kovalentās saites ietver atomus, kas dalās ar elektroniem, kā rezultātā nav neto lādiņa.
- Jonu savienojumiem ir augsta kušanas un viršanas temperatūra, jo starp joniem ir spēcīgi elektrostatiskie spēki. Turpretim kovalentiem savienojumiem ir zemāka kušanas un viršanas temperatūra vājāku starpmolekulāro spēku dēļ.
- Kovalentie savienojumi var izšķīst dažādos polāros šķīdinātājos, bet jonu savienojumi vieglāk izšķīst polāros šķīdinātājos, piemēram, ūdenī.
Jonu vs kovalento
Starpība starp Jonu un kovalentais ir tas, ka, lai gan abi šie ir ķīmiskās saites procesi, pirmais attiecas uz saiti, kurā atoms piesaista tos atomus, kas ir pretēji tā pievilkšanas spēkam. Kamēr pēdējais attiecas uz sasaisti, kurā divi nemetāli sadala savus elektronus vienādi, nevienam nezaudējot savus elektronus.

Jonu saite attiecas uz ķīmisku procesu, kurā divi joni, kas ir uzlādēti pretēji, savienojas viens ar otru, veidojot savienojumu.
No otras puses, kovalentā saite starp nemetāliem notiek precīzi. Tam nav nepieciešama pievilcība starp pretējiem joniem, bet gan saikne starp vienādi lādētiem joniem.
Salīdzināšanas tabula
| Salīdzināšanas parametri | Jonu | Kovalents |
|---|---|---|
| Nozīme | Tas notiek ķīmiskā savienojuma process starp joniem ar pretēju piesaistes lādiņu. | Tas ir ķīmisks savienošanas process, kas notiek starp joniem, kuriem ir elektronu koplietošanas savietojamība. |
| Notiek starp | Metāli un nemetāli. | Nemetāli |
| Valsts | Tas pastāv tikai cietā stāvoklī. | Tas pastāv cietā, gāzveida un šķidrā stāvoklī, visos trīs stāvokļos. |
| Kušanas punkts | Šī saite kūst ļoti augstā kušanas temperatūrā. | Šī saite kūst salīdzinoši zemā kušanas temperatūrā. |
| Vārīšanās punkts | Šī saite kūst ļoti augstā viršanas temperatūrā. | Šī saite kūst ļoti zemā kušanas temperatūrā. |
| Elektrības vadīšana | Šīs saites var vadīt elektrību. | Šīs saites nevar vadīt elektrību. |
| Darba / Zvanu laiks | Mazāk izplatīts | Biežāk |
| Veidojas sakarā ar | Kad divi pretēji lādēti joni, kas ir saderīgi viens ar otru, savienojas kopā, šī saite tiek izveidota. Tā rezultātā viens zaudē elektronus un otrs palielina elektronus. | Šīs saites pamatā nav elektronu pārnešana, bet gan elektronu koplietošana. Tas neizraisa nekādus elektronu zudumus vai pieaugumu nevienā no savienojošajiem joniem. |
Kas ir jonu?
Jonu saturs attiecas uz ķīmiskās saites vai divu atomu savienošanas procesu, lai radītu jaunu savienojumu vai objektu.
Šajā procesā divi atomi saplūst vienā vietā, un, lai pabeigtu šo procesu, šiem diviem ir jābūt atšķirīgam un pretējam elektriskajam lādiņam.
Vienu atomu, kuram ir pozitīvs lādiņš, tautā sauc par metālu. Tas ziedo daļu no saviem elektroniem otram atomam, kas satur negatīvu lādiņu un tiek saukts par nemetālu.
Populārs šīs saites piemērs ir galda sāls. Tas sastāv no nātrija un hlora,
- Nātrijs satur 11 protonus un 11 elektronus. Viens šī atoma elektrons atrodas tā ārējā ciklā, un tam ir pozitīvs lādiņš.
- Hlors satur 17 protonus un 17 elektronus, un tam ir negatīvs lādiņš.
- Pēc savienošanas nātrijs nodod savu ārējo elektronu hloram.
Kas ir kovalents?
Kovalents ir tikai vēl viens svarīgs ķīmiskās saites process, kas notiek, veidojot jaunus savienojumus un vielas.
Tam nav nepieciešams pozitīvs un negatīvs lādiņš iesaistītajos atomos, un tāpēc tas tikai savienojas ar nemetāliem (atomiem ar negatīvu lādiņu).
Ļoti slavens šīs saites piemērs ir ūdeņraža hlorīds (HCl)
- Šeit hlora ārējā perimetrā ir 7 atomi
- savukārt ūdeņradim ir 1 elektrons.
- Šie divi reaģēt kopā un apvienoties perfekti līdzsvarotā molekulā.
Galvenās atšķirības starp jonu un kovalento
- Jonu var redzēt tikai cietā stāvoklī, savukārt kovalento var redzēt visos trīs matērijas stāvokļos.
- Ionic retāk notiek un nav īpaši izplatīta, savukārt kovalentā ir liela iespēja notikt un tas ir ļoti izplatīts.
- https://www.tandfonline.com/doi/abs/10.1080/10408437108243425
- https://iopscience.iop.org/article/10.1088/0953-8984/11/30/309/meta
Pēdējo reizi atjaunināts: 23. gada 2023. jūlijā

Pijušs Jadavs pēdējos 25 gadus ir pavadījis, strādājot par fiziķi vietējā sabiedrībā. Viņš ir fiziķis, kurš aizrautīgi cenšas padarīt zinātni pieejamāku mūsu lasītājiem. Viņam ir bakalaura grāds dabaszinātnēs un pēcdiploma diploms vides zinātnē. Vairāk par viņu varat lasīt viņa vietnē bio lapa.


Patiešām labi izpētīts raksts, saturs patiešām atbilst ķīmiskās saites tēmai.
Protams, šeit sniegtā informācija ir ļoti vērtīga ķīmisko procesu ilustrēšanai.
Raksts noteikti padziļināja manu izpratni par ķīmijas jēdzieniem, ļoti labi izskaidrots ieraksts.
Piekritu. Visaptverošie skaidrojumi ievērojami uzlaboja manas zināšanas par ķīmijas procesiem.
Pamatīga, detalizēta un informatīva. Šāds raksts patiesi bagātina izpratni par ķīmisko saiti.
Absolūti, informācijas dziļums patiešām ir bagātinošs ikvienam, kam interesē ķīmija.
Esmu ļoti pārsteigts par raksta saturu, tas sniedz ļoti labi strukturētu ieskatu ķīmiskās savienošanas koncepcijās.
Es ieteiktu šo rakstu kursa biedriem, tas ir ļoti bagātinošs un saistošs lasījums.
Šeit sniegtā informācija un paskaidrojumi noteikti padara to par lielisku lasāmvielu gan studentiem, gan entuziastiem.
Es jums piekrītu, paskaidrojumi ir ļoti studentiem draudzīgi
Ļoti izsmeļošs un informatīvs raksts, paldies. Lai gan es zinu šos jēdzienus, es novērtēju, cik labi idejas tika aprakstītas šeit.
Es pilnībā piekrītu jums abiem. Šis ir ļoti izglītojošs raksts
Pilnīgi piekrītu! Sīkāka informācija ir labi uzrakstīta, un šeit sniegtās definīcijas ir izglītojošas.
Ļoti interesanta lasāmviela. Tas ir lielisks atgādinājums par ķīmijas pamatjēdzieniem
Raksts ir patiešām informatīvs un noderīgs, pārskatot ķīmijas pamatus.
Absolūti labi uzrakstīts informatīvs raksts, kas palīdz izprast saistīšanas principus.
Šis raksts ir ļoti labi strukturēts, un tajā ir sniegta detalizēta informācija ļoti organizētā veidā.
Piekrītu, raksta struktūra ļauj ļoti viegli uztvert jēdzienus
Šis saturs patiešām palīdz izprast ķīmijas nozīmi mūsu ikdienas dzīvē.
Noteikti, ka ķīmija ir mums visapkārt, un ir ļoti svarīgi saprast tās jēdzienus
Es novērtēju skaidru atšķirību starp jonu un kovalento saiti rakstā, kas ir ļoti informatīvs
Patiešām, skaidrība divu savienojuma veidu nošķiršanā padara rakstu par lielisku lasāmvielu.
Man patika paskaidrojumu detalizācijas pakāpe, tas noteikti uzlabo izpratni par ķīmisko saiti
Protams, raksts sniedz padziļinātu izpratni par ķīmiskās saites tēmu.
Detalizētības līmenis noteikti piešķir rakstam vērtību, padarot to par lielisku resursu izglītojamajiem.