Постоји толико много ствари у природи које се везују једна за другу да би формирале нову структуру или нову класу елемената. На пример: Размотрите воду, како настаје?
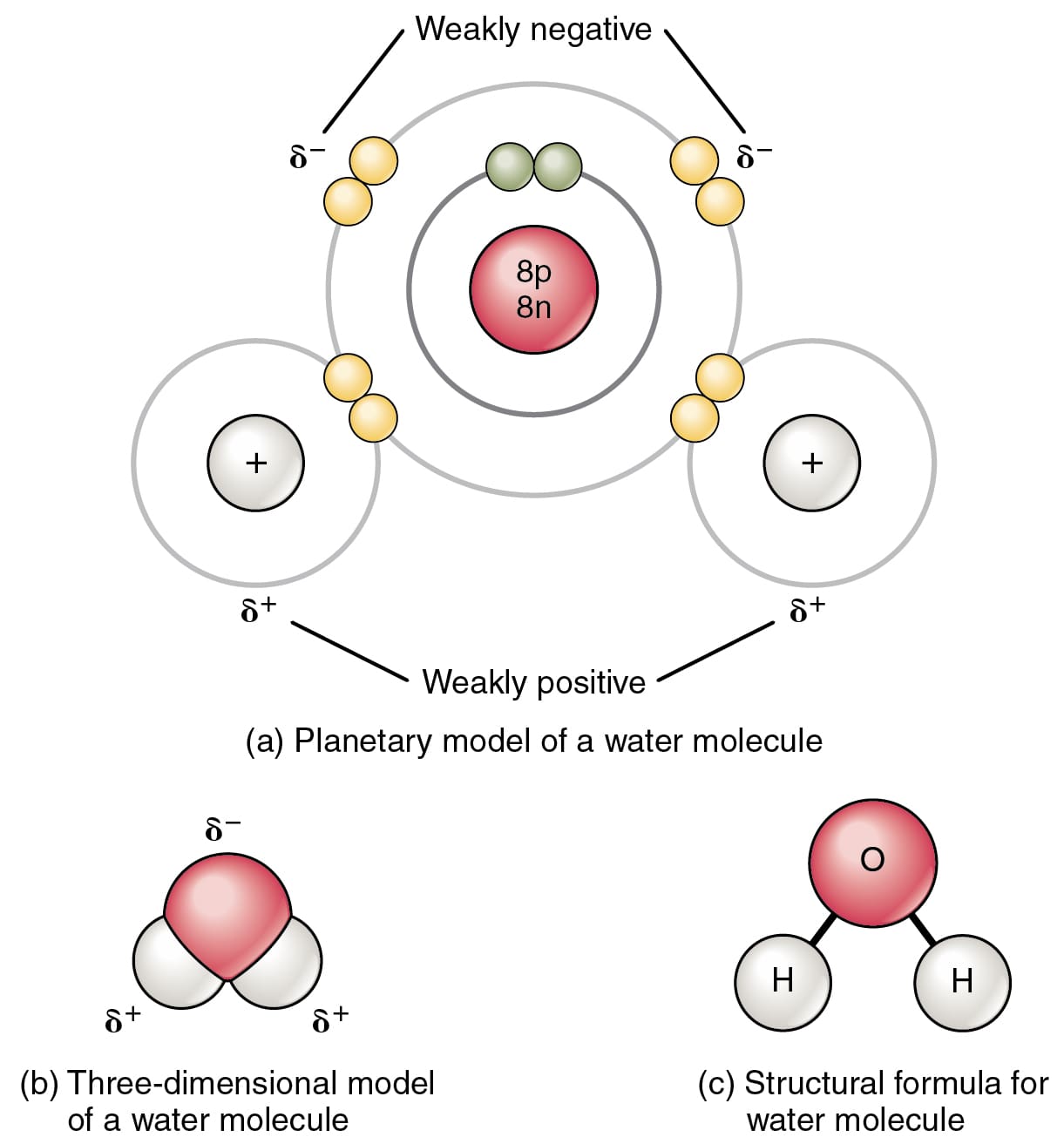
Настаје процесом хемијског везивања у којем се 2 атома водоника и 1 атом кисеоника везују да би формирали течно стање воде. Хемијско везивање је важно за живе организме и правилно функционисање делова њиховог тела.
Кључне Такеаваис
- Јонске везе се формирају између металних и неметалних елемената путем преноса електрона, док се ковалентне везе формирају између неметала путем дељења електрона.
- Металне везе се јављају између атома метала, укључујући море делокализованих електрона.
- Јонска једињења имају високе тачке топљења и кључања. Ковалентна једињења имају ниже тачке топљења и кључања, а метална једињења имају различите тачке топљења и кључања.
Јонске против ковалентних против металних веза
Јонске везе се формирају између јона супротних наелектрисања. Ови јони се могу формирати преносом једног или више електрона са једног атома на други. Ковалентне везе се формирају када атоми деле један или више парова електрона. Ова врста везе се јавља између два атома неметала. Металне везе се формирају између атома метала. У металној вези, валентни електрони нису локализовани на одређеном атому, већ су слободни да се крећу по целој металној решетки.

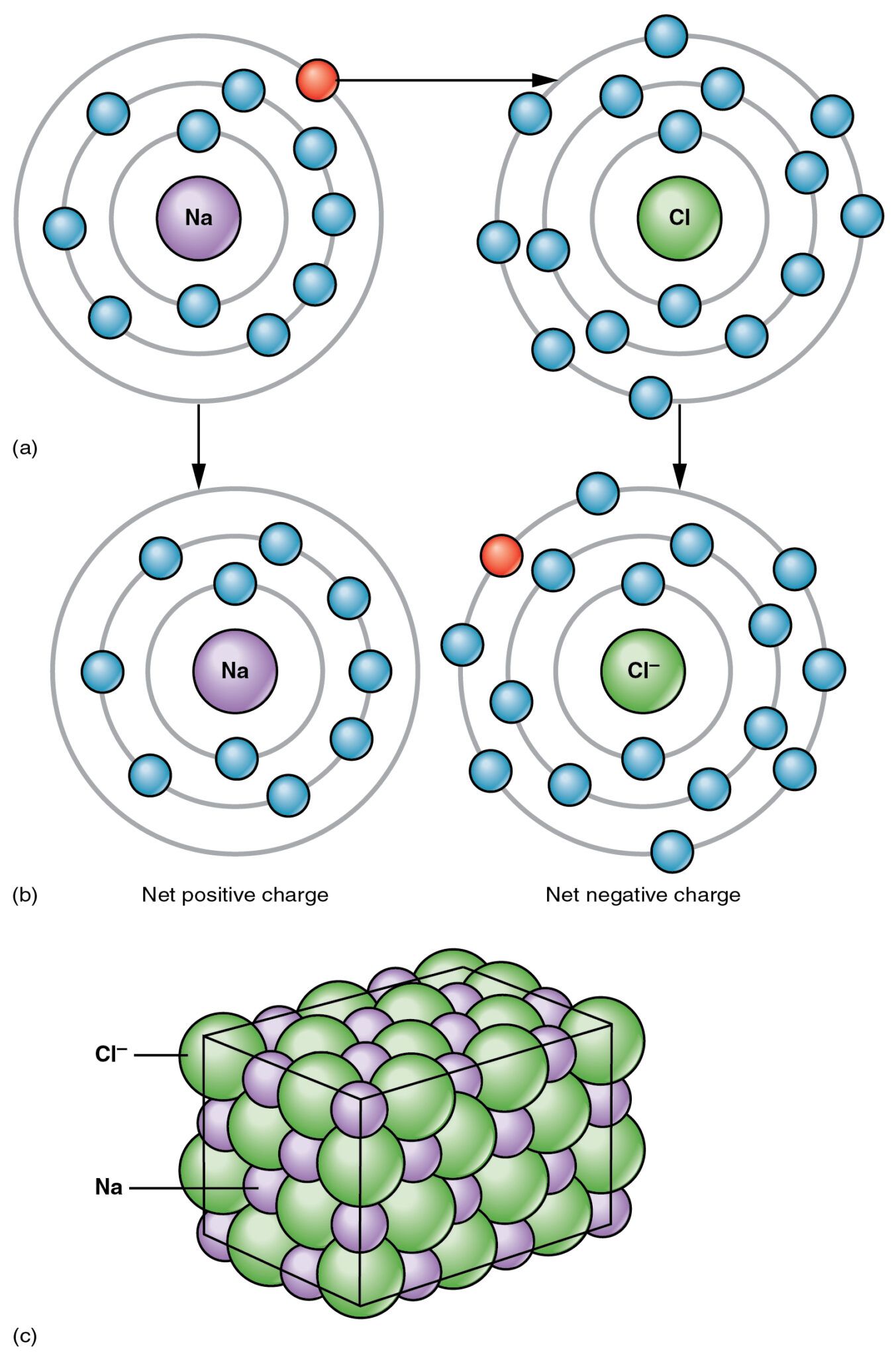
Јонска веза је пренос електрона са металног атома на неметални атом, на пример, узмите у обзир натријум хлорид; Атомски број натријума је 11, а електронска конфигурација је 2,8,1. Натријум има додатни електрон у својој крајњој љусци.
С друге стране, хлорАтомски број је 17, а електронска конфигурација је 2,8,7. Хлор има 7 електрона у својој крајњој љусци, тако да је хлору потребан још један електрон да доврши своју крајњу љуску како би сви атоми били стабилни.
Како натријум има додатни електрон када натријум реагује са хором, натријум донира тај додатни електрон хору. У овом процесу, натријум постаје позитивно наелектрисани јони (На+) и након прихватања електрона хорин постаје негативно наелектрисани јони (Цл-).
Ова два супротно наелектрисана јона држе јака електростатичка сила привлачења позната као јонска веза.
A Ковалентна веза настаје када се два или више атома споје међусобном дељењем електрона. На пример, узимајући у обзир формирање гаса кисеоника (О2), узећемо 2 атома кисеоника пошто знамо да је број електрона у кисеонику 8 и да постоји 6 валентних електрона у спољашњој љусци.
Када ове две спољне валентне љуске које садрже 6 електрона кисеоника добију још 2 електрона, биће стабилно, пошто ће његово октетно правило бити испуњено.
Да би се стабилизовали ова два атома кисеоника се комбинују и деле два атома кисеоника међусобно да би формирали гас кисеоника, ово се зове ковалентна веза.
Метално везивање је електростатичка привлачност између металних јона распоређених у структуру решетке (регуларни образац који се понавља) и слободног плутања електрона око њих.
У металној структури постоје само метални јони, ови метални јони су распоређени један поред другог у редовном понављајућем узорку, а слободно плутајући електрони делују као лепак и држе структуру на месту.
Ово је веома јака привлачност, стога је тачка топљења и тачка кључања метала веома висока. Слободно лебдећи електрони су разлози због којих је метал добар проводник електричне енергије.
Упоредна табела
| Параметри поређења | Јонска веза | Ковалентна веза | Металлиц Бонд |
|---|---|---|---|
| тренинг | Металне и неметалне | Два неметална | Позитивно пуни атоме и слободно лебдеће електроне |
| Поларитет | висок | низак | Неполарни |
| Облик молекула | Нема одређеног облика, решеткасте структуре | Дефинитивни облик | Нема одређеног облика |
| Примери | Натријум хлорид, сумпорна киселина | Метан, хорична киселина | Натријум, магнезијум |
| Тачка топљења | Висока тачка топљења | Ниска тачка топљења | Висока тачка топљења |
Шта је јонска веза?
Јонско везивање се дешава када долази до добијања и губитка електрона између метала и неметала, да би дошло до јонског везивања требало би да постоји најмање један метал.
На пример, атом магнезијума је изгубио два електрона и формирао јоне магнезијума који су позитивно наелектрисани и то су јони метала; с друге стране, атом кисеоника добија два електрона и постаје негативно наелектрисани оксидни јони и то је неметал.
Ова два атома се међусобно привлаче јер је један позитиван, а други негативан и ово привлачење се назива јонско везивање.
Шта је ковалентна веза?
Ковалентно везивање се одвија само у неметалу, никада се не може догодити са металима, настаје када два или више од два неметала међусобно деле пар електрона.
На пример, имамо два атома хлора и спољашње љуске ових атома хлора се преклапају и деле пар електрона да формирају елемент.
Два атома су спојена заједно што формира веома јаку везу која их држи заједно. Ова врста везе се назива ковалентно везивање.
Шта је метална веза?
Метална веза се јавља између метала, метали губе електроне да би формирали позитивне јоне, а лабави електрони постају делокализовани електрони што значи да више нису везани ни за какве јоне и лебде около у мору делокализованих електрона.
Пошто су јони позитивни, а делокализовани електрони негативни, између њих ће доћи до привлачења. Електростатичка привлачност између позитивних јона и негативних делокализованих електрона назива се метално везивање.
Главне разлике између јонских, ковалентних и металних веза
- У јонској вези један атом обезбеђује електроне другом, у ковалентној вези два атома размењују валентне електроне, док у металној вези метална решетка садржи атоме који деле неколико електрона.
- У јонском Енергија везе везе је већа него код металне везе, исто важи и за ковалентну везу, док у металној вези има мање енергије везе него у другим примарним везама.
- Јонска веза је слаб проводник, са друге стране, ковалентна веза је веома слаб проводник, док је метална веза јак проводник.
- Јонска веза може бити у чврстом стању, ковалентна веза може бити у чврстом, течном и гасовитом стању, док металне везе могу бити само у чврстом стању.
- Јонска веза нема флексибилну особину, исто важи и за ковалентну везу, док метална веза има особину савитљивости
- https://journals.aps.org/pr/abstract/10.1103/PhysRev.171.701
- https://www.tandfonline.com/doi/abs/10.1080/00150199208019535
Последње ажурирање: 02. јул 2023

Пијуш Јадав је последњих 25 година провео радећи као физичар у локалној заједници. Он је физичар који страствено жели да науку учини доступнијом нашим читаоцима. Дипломирао је природне науке и постдипломске студије заштите животне средине. Више о њему можете прочитати на његовом био паге.


Сложеност интеракција између различитих врста веза је апсолутно фасцинантна.
Овај чланак је свакако повећао моје знање о јонским, ковалентним и металним везама. Аутор је фантастично обавио посао у изношењу информација.
Објашњење како се атоми међусобно везују да би формирали различите врсте веза је добро илустровано. Одличан посао на овом чланку!
Чланак је јасно написан и овде има толико драгоцених информација. Ценим табелу поређења, она заиста поставља ствари у перспективу.
Табела поређења је заиста врло корисна и концизна.
Очигледно је да аутор добро разуме тему и да је ефикасно пренео ове принципе.
Ово је врло информативан чланак. Јасно објашњава разлике између јонских, ковалентних и металних веза и одлична је референца за све који студирају хемију.
Договорено! Пружа свеобухватан преглед предмета.
Верујем да ће овај чланак бити веома користан за студенте из области хемије.
Ово објашњење је невероватно темељно и проницљиво. Осећам се као да сам заиста нешто научио.