Thế giới là một nơi tuyệt đẹp. Núi, biển, bầu trời và tất cả những thứ tồn tại trong vật chất đều bao gồm các nguyên tử.
Chúng là những khối xây dựng của vũ trụ. Tuy nhiên, các nguyên tử không ổn định. Do đó, chúng tự ổn định bằng cách tạo ra các phân tử và ion.
Chìa khóa chính
- Một phân tử là một nhóm gồm hai hoặc nhiều nguyên tử liên kết hóa học với nhau, trong khi một ion là một nguyên tử hoặc phân tử có điện tích.
- Các phân tử là trung tính, trong khi các ion có thể tích điện dương hoặc âm.
- Các phân tử được hình thành thông qua liên kết cộng hóa trị, trong khi các ion được hình thành thông qua việc chuyển các electron giữa các nguyên tử.
Phân tử so với ion
Phân tử và ion khác nhau vì phân tử không có điện tích ròng, trong khi ion thì có. Điều này xảy ra bởi vì mọi thứ trong vũ trụ này đều muốn đạt được trạng thái cân bằng.
Các nguyên tử làm điều này bằng cách hình thành các phân tử và ion. Ngoài ra, các phân tử được phát triển bằng cách chia sẻ các điện tử, trong khi các ion được hình thành do trao đổi điện tử.
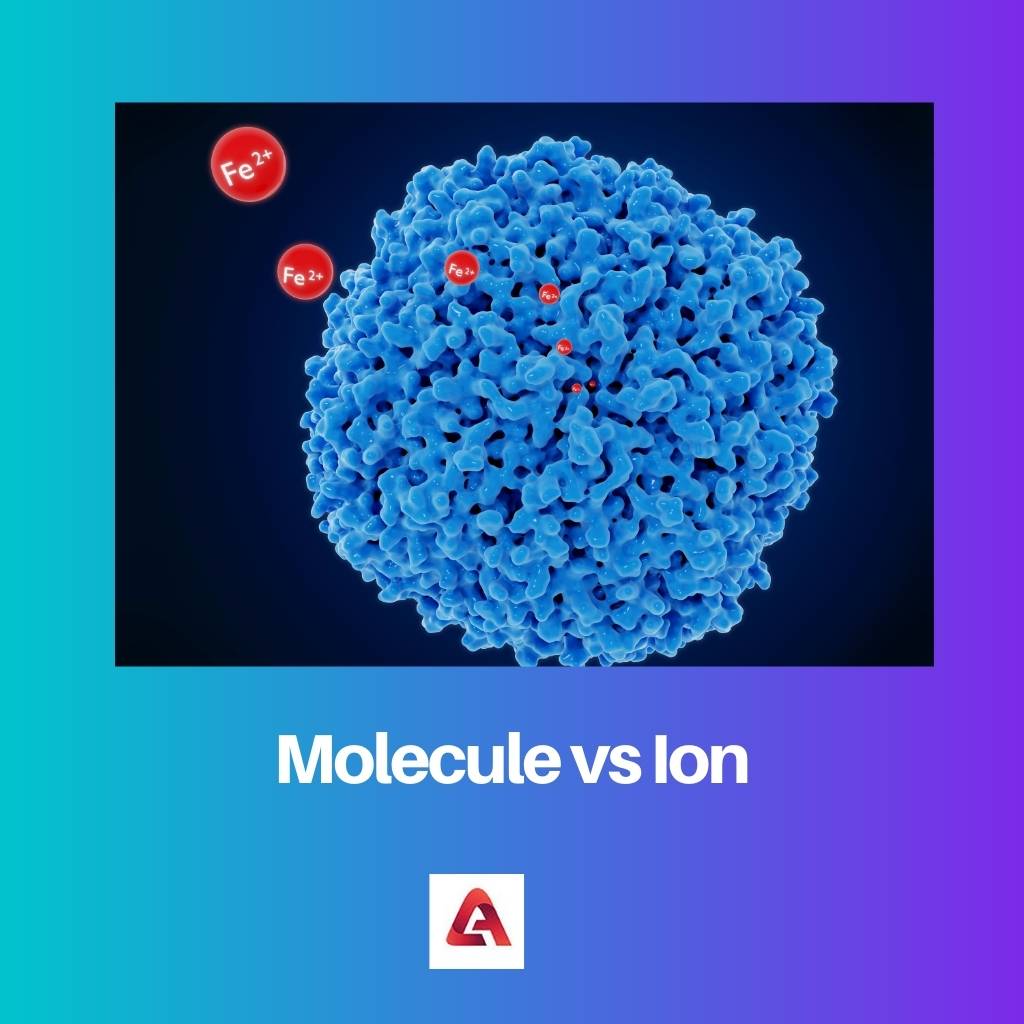
Một hoặc nhiều nguyên tử hình thành liên kết cộng hóa trị để trở thành một phân tử. Đơn vị nhỏ nhất cấu tạo nên một chất là phân tử. Một phân tử giữ lại tất cả các tính chất hóa học của bản chất. Các nguyên tử mô tả các phân tử, được biểu diễn bằng các vòng tròn, tạo thành các liên kết với nhau.
Một loại hóa chất có điện tích dương hoặc âm được gọi là ion. MỘT nguyên tử và một phân tử có thể được gọi là ion nếu chúng có tài khoản mạng khác không. Do đó, tất cả các ion đều có nhiều electron hơn proton hoặc nhiều proton hơn electron trong cấu trúc phân tử hoặc nguyên tử của chúng.
Bảng so sánh
| Các thông số so sánh | Phân tử | ion |
|---|---|---|
| Sự phân bố điện tử | Phân tử được hình thành do sự góp chung electron giữa hai hay nhiều nguyên tử hoặc do hai ion mang điện tích trái dấu. | Các ion được hình thành khi các nguyên tử tăng hoặc giảm điện tích để đạt được cấu hình khí hiếm. |
| Kích thước máy | Kích thước phân tử phụ thuộc vào kích thước của các nguyên tử hoặc ion tham gia vào sự hình thành liên kết. | Các anion có ý nghĩa quan trọng hơn các phân tử mẹ và các cation nhỏ hơn các phân tử mẹ. |
| Tính ổn định | Các phân tử ổn định hơn các ion. | Ion kém bền hơn phân tử. |
| đào tạo | Liên kết cộng hóa trị hoặc liên kết ion tạo thành phân tử. | Ion được hình thành do liên kết ion giữa hai ion mang điện tích trái dấu và mạnh hơn cộng hóa trị. |
| dẫn điện | Vì các phân tử có điện tích bằng không nên chúng không phải là chất dẫn điện tốt. | Ion là chất dẫn điện tốt. |
Phân tử là gì?
Đơn vị nhỏ nhất của hợp chất, thể hiện tính chất hóa học của hợp chất, được gọi là phân tử. Các phân tử bao gồm hai hoặc nhiều nguyên tử liên kết cộng hóa trị với nhau, nghĩa là chúng dùng chung một hoặc nhiều electron.
Các phân tử bao gồm hầu hết trái đất và hầu hết các chất hữu cơ đều được tạo thành từ các phân tử.
Các phân tử có thể là đồng nhân và dị nhân, nghĩa là chúng lần lượt bao gồm các nguyên tố giống nhau hoặc khác nhau.
Một liên kết cộng hóa trị được hình thành khi hai nguyên tử có octet không đầy đủ chia sẻ bit. Một liên kết cộng hóa trị biến các nguyên tử khác nhau thành một phân tử.
Các phân tử bao gồm các nguyên tử được nhóm lại với nhau thông qua liên kết cộng hóa trị hoặc liên kết ion.
Các phân tử có liên kết cộng hóa trị yếu hơn so với các phân tử có liên kết ion. Điều này xảy ra vì liên kết ion có lực tĩnh điện mạnh giữ các ion lại với nhau.
Do đó, các phân tử ion ổn định hơn các phân tử liên kết cộng hóa trị.

Ion là gì?
Một ion là một loại hóa chất có điện tích dương hoặc âm ở một mức độ nào đó. Các ion đề cập đến các phân tử và nguyên tử có kiểm soát mạng khác không.
Do đó, các ion có nhiều proton hơn electron hoặc nhiều electron hơn proton trong cấu trúc phân tử hoặc nguyên tử của chúng.
Các ion có số lượng electron đáng kể hơn proton và giữ điện tích âm được gọi là anion.
Ngược lại, các ion có số lượng proton nhiều hơn electron và giữ điện tích dương được gọi là cation.
Liên kết ion chỉ được hình thành khi lực tĩnh điện phát sinh giữa anion mang điện tích âm và cation mang điện tích dương.
Các lực tĩnh điện này thu hút các anion và cation với nhau để ổn định điện tích ròng. Các lực tĩnh điện này giúp hình thành hợp chất ion.
Các ion chỉ tạo bởi một nguyên tố được gọi là ion nguyên tử hoặc ion đơn nguyên tử. Các nguyên tử tham gia giữ một số điện tích ròng, dương hoặc âm.
Trong khi đó, nếu hai hoặc nhiều nguyên tố tham gia vào một ion, thì chúng được gọi là ion phân tử hoặc đa nguyên tử.
Sự khác biệt chính giữa các phân tử và ion
- Các phân tử không có điện tích ròng, trong khi các ion có điện tích dương hoặc âm.
- Các phân tử được hình thành khi hai hoặc nhiều nguyên tử chia sẻ các electron để hoàn thành bộ tám của chúng, trong khi các ion trao đổi electron và hình thành hợp chất ion do lực tĩnh điện.
- Vì các ion được giữ với nhau bằng lực tĩnh điện nên chúng ổn định hơn nhiều so với các phân tử được hình thành bởi liên kết cộng hóa trị.
- Do lực hấp dẫn cao giữa hai ion, chúng có nhiều năng lượng mạng tinh thể hơn so với các phân tử liên kết cộng hóa trị.
- Do năng lượng mạng cao hơn, các ion ổn định hơn so với liên kết cộng hóa trị.
- Kích thước của các phân tử phụ thuộc vào các nguyên tử tham gia vào sự hình thành liên kết. Các cation nhỏ hơn các phân tử mẹ của chúng, trong khi các anion có ý nghĩa hơn các phân tử mẹ của chúng.

- https://ui.adsabs.harvard.edu/abs/1988STIA…8915174M/abstract
- https://pubs.acs.org/doi/pdf/10.1021/ja00260a006
Cập nhật lần cuối: ngày 11 tháng 2023 năm XNUMX

Piyush Yadav đã dành 25 năm qua làm việc với tư cách là một nhà vật lý trong cộng đồng địa phương. Anh ấy là một nhà vật lý đam mê làm cho khoa học dễ tiếp cận hơn với độc giả của chúng tôi. Ông có bằng Cử nhân Khoa học Tự nhiên và Bằng Sau Đại học về Khoa học Môi trường. Bạn có thể đọc thêm về anh ấy trên trang sinh học.


Bảng so sánh của bài viết đặc biệt hữu ích trong việc tìm hiểu các đặc điểm riêng biệt của phân tử và ion. Đó là một điểm tham khảo tuyệt vời để so sánh nhanh chóng.
Tôi thấy sự so sánh cũng rất hữu ích. Đó là một cách thuận tiện để nhanh chóng nắm bắt được sự khác biệt chính giữa các phân tử và ion.
Bài viết đưa ra sự so sánh toàn diện về các phân tử và ion, nhưng lại thiếu cách tiếp cận hấp dẫn hơn để khiến nội dung trở nên hấp dẫn hơn đối với người đọc.
Tôi thấy điểm của bạn. Mặc dù thông tin có giá trị nhưng một câu chuyện hấp dẫn hơn có thể nâng cao sức hấp dẫn tổng thể của bài viết.
Bảng so sánh của bài viết đã tóm tắt một cách hiệu quả những khác biệt chính giữa phân tử và ion. Đây là một công cụ hữu ích để xem xét và củng cố các khái niệm.
Bài viết đã cung cấp sự hiểu biết rõ ràng và ngắn gọn về các phân tử và ion, rất có giá trị cho những người mới bắt đầu trong lĩnh vực hóa học.
Tôi đồng ý. Đây là điểm khởi đầu tốt cho những ai mới làm quen với hóa học, nhưng nó có thể bao gồm các khái niệm nâng cao hơn cho những người hiểu sâu hơn về chủ đề này.
Bài viết này là một cái nhìn hấp dẫn về thế giới của các phân tử và ion. Những giải thích và so sánh chi tiết đã cung cấp những hiểu biết sâu sắc.
Tôi thấy bài viết rất nhiều thông tin và có cấu trúc tốt. Nó thực sự giúp tôi hiểu được sự khác biệt giữa phân tử và ion.
Tôi hoàn toàn đồng ý. Thông tin được cung cấp rất giáo dục và thú vị.
Bài báo đã làm rất tốt việc đơn giản hóa các khái niệm phức tạp, nhưng nó thiếu các thảo luận chuyên sâu về tính chất hóa học và hành vi của các phân tử và ion.
Tôi đồng ý với bạn. Mặc dù bài viết cung cấp một cái nhìn tổng quan nhưng nó có thể bao gồm những hiểu biết chi tiết hơn về tính chất hóa học của các đơn vị cơ bản này.
Những so sánh được cung cấp rất hữu ích trong việc tìm hiểu sự khác biệt giữa các phân tử và ion. Tôi đánh giá cao sự rõ ràng trong các lời giải thích.
Tôi thấy bài viết còn hơi sơ đẳng. Nó không cung cấp nhiều chiều sâu cho những người đang tìm kiếm thông tin nâng cao hơn.
Tôi không thể đồng ý nhiều hơn. Sự rõ ràng và đơn giản của bài viết khiến nó trở thành một nguồn tài liệu quý giá cho những ai quan tâm đến hóa học.
Tôi nghĩ rằng bài báo đã nêu bật một cách hiệu quả những khác biệt chính giữa phân tử và ion, giúp các chuyên gia không chuyên về hóa học dễ dàng nắm bắt hơn.
Tôi nghĩ bài viết đã đơn giản hóa quá mức các khái niệm về phân tử và ion. Nó có thể đã nghiên cứu sâu hơn về tính chất hóa học đằng sau những khối xây dựng cơ bản này.
Tôi hiểu quan điểm của bạn, nhưng để có cái nhìn tổng quát, bài viết cung cấp một điểm khởi đầu tốt. Điều quan trọng là làm cho các chủ đề phức tạp có thể tiếp cận được với nhiều đối tượng.
Các giải thích rõ ràng và ngắn gọn, giúp bạn dễ hiểu hơn về sự khác biệt giữa phân tử và ion. Bài viết đã cung cấp một nền tảng vững chắc cho việc học tập sâu hơn.
Tôi thấy sự giải thích rõ ràng cũng rất hữu ích. Thật tuyệt vời khi xây dựng sự hiểu biết vững chắc về những khái niệm này.