Menschen verwechseln Ethanol und Ethansäure wegen der Ähnlichkeit ihrer Namen. Abgesehen davon ist die einzige gemeinsame Verbindung zwischen beiden ihr physischer Zustand. Beide liegen in flüssiger Form vor und sind farblos. Abgesehen von diesen beiden Faktoren weisen beide Säuren viele Unterschiede auf.
Ethanol ist einfach Alkohol, der eine brennbare und flüchtige Flüssigkeit und auch eine alternative Brennstoffquelle ist. Es ist eine psychoaktive Substanz als Freizeitdroge und Wirkstoff in alkoholischen Getränken.
Im Gegensatz dazu ist Essigsäure die nachfolgende Carbonsäure der Ameisensäure. Weltweit beträgt der Bedarf bis zu 6.5 Millionen Tonnen pro Jahr.
Ihre Dichte, Geruch, Geschmack, Siede- und Schmelzpunkte unterscheiden sich voneinander. Die Summenformel von Ethanol ist C2H5OH und Essigsäure ist CH3COH.
Key Take Away
- Ethanol ist ein Alkohol mit der chemischen Formel C2H5OH, während Ethansäure eine Carbonsäure mit CH3COOH ist.
- Ethanol ist eine farblose Flüssigkeit mit leichtem Geruch, die üblicherweise als Brennstoff und Lösungsmittel verwendet wird. Gleichzeitig ist Essigsäure eine farblose Flüssigkeit mit starkem Geruch, die üblicherweise in der Essigherstellung verwendet wird.
- Ethanol hat einen niedrigeren Siedepunkt als Essigsäure, wodurch es leichter verdampft und weniger sauer als Essigsäure ist.
Ethanol gegen Essigsäure
Ethanol, auch als Ethylalkohol bekannt, ist eine farblose, brennbare Flüssigkeit, die häufig als Lösungsmittel, Brennstoff und in alkoholischen Getränken verwendet wird. Seine chemische Formel ist C2H5OH. Ethansäure, auch bekannt als Essigsäure, ist eine klare, farblose Flüssigkeit, die einen scharfen, stechenden Geruch hat. Seine chemische Formel ist CH3COOH.

Vergleichstabelle
| Vergleichsparameter | Ethanol | Essigsäure |
|---|---|---|
| IUPAC-Name | Der Name der International Union of Pure and Applied Chemistry (IUPAC) für Ethanol ist derselbe wie er genannt wird. | Der Name der International Union of Pure and Applied Chemistry (IUPAC) einer Ethansäure ist eine Essigsäure. |
| Molekulare Formeln | Seine Summenformel ist C2H5OH | Seine Summenformel ist CH3COH. |
| Signaldichte | 0.789 g / cm3 | 1.05 g / cm3 |
| Odur | Es hat einen angenehmen parfümartigen Geruch. | Es hat einen stechenden oder nach Essig riechenden Geruch. |
| Genieße | Es ist brennend und bitter. | Es ist Sauer. |
| Siedepunkte | Es hat einen Siedepunkt von 78.37 ℃ oder 173.1 ℉. | Es hat einen Siedepunkt von 117.9 ℃ oder 244.2 ℉. |
| Schmelzpunkte | Es hat einen Schmelzpunkt von -114.1 ℃ oder -173.5 ℉. | Es hat einen Schmelzpunkt von 16.6 ℃ oder 61.9 ℉. |
| Funktionelle Gruppe | Es hat Alkohol (-OH) als funktionelle Gruppe. | Es hat eine Carbonsäure (-OOH) als funktionelle Gruppe. |
| Existenz anderer Gruppen | Ethyl- und Hydroxylgruppen existieren in Ethanol. | Methyl- und Carboxylgruppen existieren in Ethanol. |
| Der Lackmus-Papiertest | Es weist eine 7.33 auf pH-Skala bei einer Konzentration. | Es weist eine 2 bis 4 auf pH-Skala bei einer Konzentration. |
| NaHCO3 Test | Es reagiert nicht mit Natriumbicarbonat. | Es reagiert mit Natriumbicarbonat und setzt CO frei2 Gas. |
| Ostertest | Es bildet Ester nur nach Reaktion mit der Gegenwart von Essigsäure. | Es bildet nach der Reaktion mit Schwefelsäure Ester. |
| Molmasse | X | X |
| Benutzt für | Es kann als Sterilisationsmittel oder zur Herstellung von alkoholischen Getränken verwendet werden. | Es kann als Toilettenreiniger oder zur Herstellung von Essig verwendet werden. |
Was ist Ethanol?
Der Name der International Union of Pure and Applied Chemistry (IUPAC) für Ethanol ist derselbe wie er genannt wird.
Seine Summenformel lautet „C2H5OH,' und seine Dichte beträgt 0.789 g/cm3. Es hat einen bitteren, brennenden Geschmack und ist angenehm Parfüm-ähnlicher Geruch. Es kann als Sterilisationsmittel oder zur Herstellung alkoholischer Getränke verwendet werden.
Die Molmasse dieser Säure beträgt 46.07 g/mol. Der Schmelzpunkt von Ethanol beträgt -114.1 ℃ oder -173.5 ℉. Und sein Siedepunkt beträgt 78.37 ℃ oder 173.1 ℉. Bei der Gärung entsteht Ethanol mithilfe von Hefen wie Saccharomyces cerevisiae oder Schizo-saccharomyces.
Der Lackmus-Papiertest weist eine pH-Skala von 7.33 (Wasserstoffpotential) auf. Es reagiert nicht mit Natriumbicarbonat. Es bildet Ester erst nach einer Reaktion in Gegenwart von Essigsäure. Es hat Alkohol (-OH) als funktionelle Gruppe. Abgesehen davon gibt es Ethyl- und Hydroxylgruppen, die existieren.

Was ist Essigsäure?
Der Name der International Union of Pure and Applied Chemistry (IUPAC) einer Ethansäure ist eine Essigsäure. Es hat einen säuerlichen Geschmack und einen stechenden oder nach Essig riechenden Geruch. Seine Molekularformel lautet „CH3COOH“ und seine Dichte beträgt 1.05 g/cm3. Es kann als Toilettenreiniger oder zur Herstellung von Essig verwendet werden.
Es weist im Lackmus-Papiertest eine pH-Skala von 2–4 (Wasserstoffpotential) auf. Es reagiert mit Natriumbicarbonat und setzt CO frei2 Gas. Es bildet auch nach der Reaktion mit Schwefelsäure Ester.
Es hat eine Carbonsäure (-OOH) als funktionelle Gruppe. Abgesehen davon gibt es Methyl- und Carboxylgruppen, die existieren.
Die Molmasse dieser Säure beträgt 60.052 g/mol. Acetobacter-Bakterien bilden bei der Fermentation Essigsäure. Wenn Essigsäure durch die Kalkflüssigkeit geht, wird sie undurchsichtig und wird zu CO2 Gas. Sein Siedepunkt beträgt 17.9 ℃ oder 244.2 ℉. Und der Schmelzpunkt beträgt 16.6 ℃ oder 61.9 ℉.
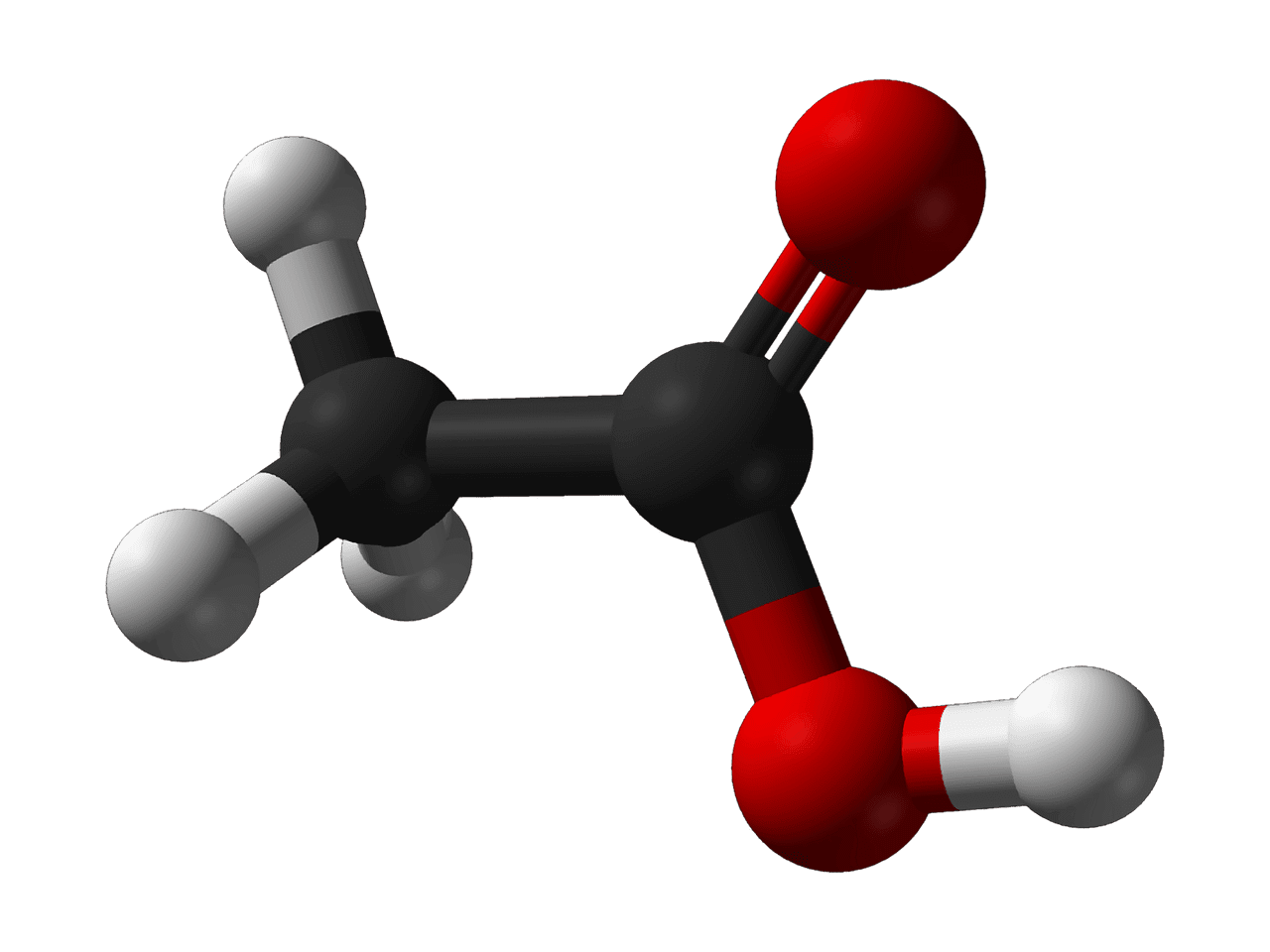
Hauptunterschiede zwischen Ethanol und Essigsäure
- Die Molekularformel von Ethanol ist C2H5OH, während Essigsäure CH ist3COH.
- 0.789 g/cm3 ist die Dichte von Ethanol, während 1.05 g/cm3 Essigsäure ist.
- Das erste hat einen angenehmen parfümartigen Geruch. Im Gegenteil, die zweite hat einen stechenden oder nach Essig riechenden Geruch.
- Das Ethyl schmeckt wenig brennend und bitter. Die Essigsäure schmeckt säuerlich.
- Der Siedepunkt von Ethanol beträgt 78.37 ℃ oder 173.1 ℉. Umgekehrt hat Essigsäure 117.9 ℃ oder 244.2 ℉.
- Der Schmelzpunkt des ersten beträgt -114.1 ℃ oder -173.5 ℉. Andererseits hat der zweite 16.6 ℃ oder 61.9 ℉.
- Das vorherige hat Alkohol (-OH) als funktionelle Gruppe. Im Gegensatz dazu hat das folgende eine Carbonsäure (-OOH).
- Das Ethanol weist im Lackmuspapiertest eine pH-Skala von 7.33 auf, während Essigsäure eine pH-Skala von 2 bis 4 aufweist.
- Ersteres reagiert nicht mit Natriumbicarbonat. Umgekehrt reagiert letzteres und setzt CO frei2 Gas.
- Die Molmasse von Ethanol beträgt 46.07 g/mol, während die Molmasse von Essigsäure 60.052 g/mol beträgt.
- https://pubs.acs.org/doi/abs/10.1021/je300810p
- https://www.sciencedirect.com/science/article/pii/S0378775301010679
- https://www.sciencedirect.com/science/article/pii/S0022328X04004668
Dieser Artikel wurde geschrieben von: Supriya Kandekar
Letzte Aktualisierung: 11. Juni 2023

Piyush Yadav hat die letzten 25 Jahre als Physiker in der örtlichen Gemeinde gearbeitet. Er ist ein Physiker, der sich leidenschaftlich dafür einsetzt, die Wissenschaft für unsere Leser zugänglicher zu machen. Er hat einen BSc in Naturwissenschaften und ein Postgraduiertendiplom in Umweltwissenschaften. Sie können mehr über ihn auf seinem lesen Bio-Seite.


Dieser Beitrag ist ein Hauch frischer Luft und bietet aufschlussreiches Wissen über Ethanol und Ethansäure.
Auf jeden Fall, es ist informativ und aufschlussreich.
Diese Informationen sind von entscheidender Bedeutung für Chemiebegeisterte, die ihr Wissen erweitern möchten.
Als jemand, der Chemie liebt, schätze ich die Tiefe dieser Erklärung.
Da ich mich sehr für Chemie interessiere, halte ich diesen Artikel für eine außergewöhnliche Informationsquelle.
Tatsächlich ist es eine gut artikulierte und ausführliche Erklärung des Themas.
Ich bin froh, dass es diesen Beitrag gibt, viele Menschen wissen nichts über den Unterschied zwischen Ethanol und Ethansäure.
Auf jeden Fall helfen die wissenschaftlichen Details dem Leser beim Verständnis.
Dieser Artikel ist eine hervorragende Ressource für Studierende und Fachleute auf dem Gebiet der Chemie.
Die ausführliche Analyse hebt diesen Artikel von anderen ab.
Sicherlich bietet es wertvolles Wissen, das zu einem tieferen Verständnis des Themas beiträgt.
Der Beitrag unterscheidet anhand wissenschaftlicher Erkenntnisse effektiv zwischen Ethanol und Ethansäure.
Zugegebenermaßen findet man selten so gut recherchierte Inhalte.
Der informative Inhalt ist ein Beweis für die Fachkompetenz des Autors in der Thematik.
Ich schätze den detaillierten und objektiven Charakter dieses Beitrags.
Der wissenschaftlich fundierte Vergleich liefert wertvolle Erkenntnisse.
Ich finde die detaillierte Vergleichstabelle und die wichtigsten Erkenntnisse sehr nützlich und aufschlussreich.
Die Klarheit der hier präsentierten Informationen ist lobenswert.
Ich stimme zu, dieser Beitrag bietet einen ganzheitlichen Überblick über die Unterschiede zwischen Ethanol und Ethansäure.
Dies ist ein sehr informativer Artikel, der alle Zweifel am Unterschied zwischen Ethanol und Ethansäure ausräumt.
Dank dieses Artikels verstehe ich endlich den Unterschied zwischen den beiden.
Ich stimme zu, das wird auf wissenschaftliche Weise klar erklärt.
Die hier bereitgestellten ausführlichen Erläuterungen sind äußerst hilfreich und bereichernd.
Auf jeden Fall verbessert es das Verständnis des Lesers für die Thematik.