La ciencia en nuestra vida diaria contiene muchos aspectos. Todo lo que vemos a simple vista está formado por miles de millones de átomos y moléculas.
En el lenguaje de la química, el proceso por el cual los átomos entran en contacto y forman objetos se llama enlace químico.
Puntos clave
- Los enlaces iónicos se forman cuando los átomos transfieren electrones, creando iones cargados que se atraen entre sí, mientras que los enlaces covalentes involucran átomos que comparten electrones, lo que resulta en una carga neta nula.
- Los compuestos iónicos exhiben altos puntos de fusión y ebullición debido a las fuertes fuerzas electrostáticas entre los iones. Por el contrario, los compuestos covalentes tienen puntos de fusión y ebullición más bajos debido a fuerzas intermoleculares más débiles.
- Los compuestos covalentes pueden disolverse en varios solventes polares, pero los compuestos iónicos se disuelven más fácilmente en solventes polares como el agua.
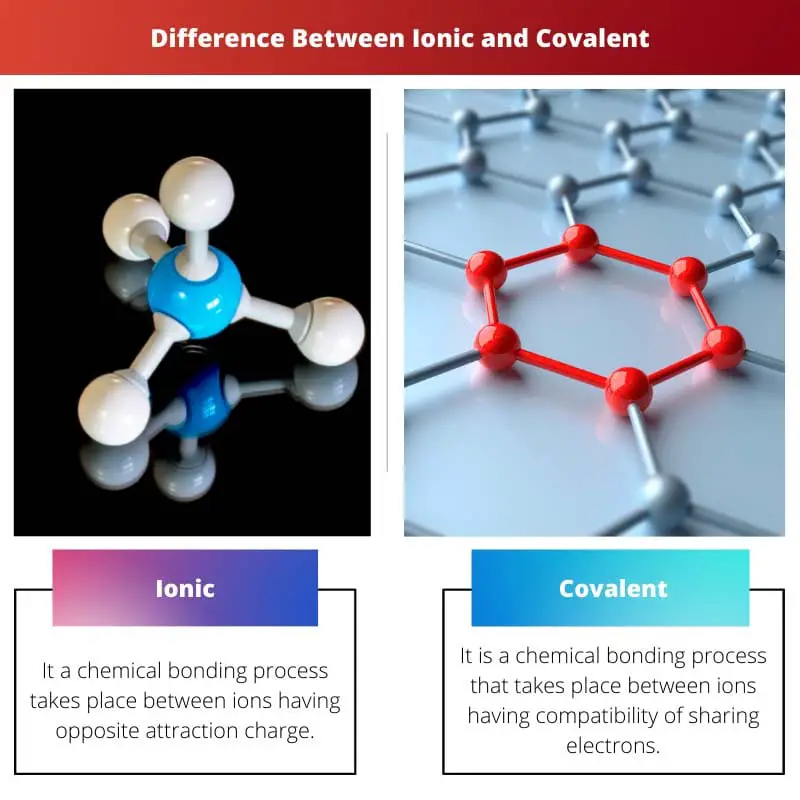
Iónico vs Covalente
La diferencia entre los Iónico y covalente es que, si bien ambos son procesos de enlace químico, el primero se refiere al enlace en el que un átomo atrae a los átomos que son opuestos a su fuerza de atracción. Mientras que el último se refiere a un vínculo en el que dos no metales comparten sus electrones por igual sin que uno tenga que perder sus electrones.

El enlace iónico se refiere a un proceso químico precisamente en el que dos iones que están cargados de manera opuesta se unen entre sí para formar un compuesto.
Mientras que, por otro lado, el enlace covalente se produce precisamente entre los no metales. No requiere atracción entre iones opuestos sino un enlace entre iones igualmente cargados.
Tabla de comparación
| Parámetros de comparación | Iónico | Covalente |
|---|---|---|
| Sentido | Se produce un proceso de enlace químico entre iones que tienen carga de atracción opuesta. | Es un proceso de enlace químico que tiene lugar entre iones que tienen compatibilidad de compartir electrones. |
| ocurre entre | Metales y no metales. | No metales |
| Estado | Sólo existe en la posición sólida. | Existe en estado sólido, gaseoso y líquido, los tres estados. |
| punto de fusión | Este enlace se funde en un punto de fusión muy alto. | Este enlace se funde en un punto de fusión comparativamente bajo. |
| Punto de ebullición | Este enlace se funde en un punto de ebullición muy alto. | Este enlace se funde a un punto de fusión muy bajo. |
| Conducción de Electricidad | Estos enlaces pueden conducir electricidad. | Estos enlaces no pueden conducir la electricidad. |
| Disponibilidad | Menos común | Más común |
| Formado debido a | Cuando dos iones de carga opuesta que son compatibles entre sí se unen, se crea este enlace. Resulta en la pérdida de electrones por uno y la ganancia de electrones por el otro. | Este enlace no se basa en la transferencia de electrones, sino en el intercambio de electrones. No provoca ninguna pérdida o ganancia de electrones en ninguno de los iones que se unen. |
¿Qué es iónico?
Iónico se refiere al proceso de enlace químico o unión de dos átomos para dar nacimiento a un nuevo compuesto u objeto.
En este proceso, dos átomos se unen en un solo lugar, y el requisito es que estos dos tengan una carga eléctrica diferente y opuesta para finalizar este proceso.
Un átomo que tiene una carga positiva se conoce popularmente como metal. Dona algunos de sus electrones al otro átomo, que contiene una carga negativa y se denomina no metal.
Un ejemplo popular de este vínculo es la sal de mesa. Está compuesto de sodio y cloro.
- El sodio contiene 11 protones y 11 electrones. Un electrón de este átomo está presente en su ciclo exterior y lleva una carga positiva.
- El cloro contiene 17 protones y 17 electrones y tiene carga negativa.
- Después de unirse, el sodio dona su electrón externo al cloro.
¿Qué es covalente?
Covalente es solo otro proceso importante de enlace químico que tiene lugar para formar nuevos compuestos y sustancias.
No necesita carga positiva y negativa en los átomos participantes, por eso sólo une no metales (átomos con carga negativa).
Un ejemplo muy famoso de este enlace es el cloruro de hidrógeno (HCl)
- Aquí el Cloro tiene 7 átomos en su perímetro exterior
- mientras que el hidrógeno tiene 1 electrón.
- Estos dos reaccionar juntos y se combinan en una molécula perfectamente equilibrada.
Principales diferencias entre iónico y covalente
- Ionic se puede ver solo en estado sólido, mientras que Covalent se puede ver en los tres estados de la materia.
- Ionic tiene menos probabilidades de ocurrir y no es muy común, mientras que Covalent tiene una alta posibilidad de ocurrir y es muy común.
- https://www.tandfonline.com/doi/abs/10.1080/10408437108243425
- https://iopscience.iop.org/article/10.1088/0953-8984/11/30/309/meta
Última actualización: 23 julio, 2023

Piyush Yadav ha pasado los últimos 25 años trabajando como físico en la comunidad local. Es un físico apasionado por hacer que la ciencia sea más accesible para nuestros lectores. Tiene una licenciatura en Ciencias Naturales y un Diploma de Postgrado en Ciencias Ambientales. Puedes leer más sobre él en su página de biografía.

De hecho, es un artículo bien investigado, el contenido realmente hace justicia al tema de los enlaces químicos.
Absolutamente, la información proporcionada aquí es muy valiosa para ilustrar procesos químicos.
El artículo ciertamente profundizó mi comprensión de los conceptos de química, un post muy bien explicado.
Acordado. Las explicaciones completas mejoraron enormemente mi conocimiento de los procesos químicos.
Completo, detallado e informativo. Un artículo como este realmente enriquece la comprensión del enlace químico.
Absolutamente, la profundidad de la información es realmente enriquecedora para cualquier persona interesada en la química.
Estoy muy impresionado con el contenido del artículo, ofrece una visión muy bien estructurada de los conceptos de enlaces químicos.
Recomendaría este artículo a mis compañeros de estudios, es una lectura muy enriquecedora y atractiva.
Por supuesto, los detalles y explicaciones que se proporcionan aquí lo convierten en una excelente lectura tanto para estudiantes como para entusiastas.
Estoy de acuerdo contigo, las explicaciones son muy amigables para los estudiantes.
Un artículo muy completo e informativo, gracias. Aunque conozco estos conceptos, aprecio lo bien que se describen aquí las ideas.
Estoy completamente de acuerdo con ambos. Este es un artículo muy educativo.
¡Totalmente de acuerdo! Los detalles están bien escritos y las definiciones aquí son esclarecedoras.
Lectura muy interesante. Es un gran recordatorio de los conceptos básicos de la química.
El artículo es realmente informativo y útil para repasar los fundamentos de la química.
Absolutamente, un artículo informativo bien escrito que ayuda a comprender los principios del vínculo.
Este artículo está muy bien estructurado y presenta la información detallada de una manera muy organizada.
Estoy de acuerdo, la estructura del artículo hace que sea muy fácil comprender los conceptos.
Este contenido realmente ayuda a comprender la importancia de la química en nuestra vida diaria.
Definitivamente, la química está a nuestro alrededor y comprender los conceptos detrás de ella es crucial.
Aprecio la clara distinción hecha entre enlaces iónicos y covalentes en el artículo, muy informativo.
De hecho, la claridad al distinguir los dos tipos de vínculo hace que el artículo sea una excelente lectura.
Disfruté el nivel de detalle en las explicaciones, ciertamente mejora la comprensión del enlace químico.
Definitivamente, el artículo proporciona una comprensión profunda sobre el tema de los enlaces químicos.
El nivel de detalle definitivamente agrega valor al artículo, lo que lo convierte en un gran recurso para los estudiantes.