Le persone confondono l'etanolo e l'acido etanoico a causa della somiglianza nei loro nomi. A parte questo, l’unico legame comune tra entrambi è il loro stato fisico. Entrambi sono in forma liquida e sono incolori. Oltre a questi due fattori, entrambi gli acidi presentano molte differenze.
L'etanolo è semplicemente alcol che è un liquido infiammabile e volatile e anche una fonte di carburante alternativa. È una sostanza psicoattiva come droga ricreativa e ingrediente attivo nelle bevande alcoliche.
Al contrario, l'acido etanoico è l'acido carbossilico successivo all'acido formico. A livello globale, la sua domanda arriva fino a 6.5 milioni di tonnellate all'anno.
La loro densità, l'odore, il sapore, l'ebollizione e i punti di fusione differiscono l'uno dall'altro. La formula molecolare dell'etanolo è C2H5OH, e l'acido etanoico è CH3COO.
Punti chiave
- L'etanolo è un alcol con la formula chimica C2H5OH, mentre l'acido etanoico è un acido carbossilico con CH3COOH.
- L'etanolo è un liquido incolore con un leggero odore comunemente usato come combustibile e solvente. Allo stesso tempo, l'acido etanoico è un liquido incolore con un forte odore comunemente usato nella produzione di aceto.
- L'etanolo ha un punto di ebollizione inferiore rispetto all'acido etanoico, rendendo più facile l'evaporazione e meno acido dell'acido etanoico.
Etanolo vs acido etanoico
L'etanolo, noto anche come alcol etilico, è un liquido incolore e infiammabile comunemente usato come solvente, carburante e nelle bevande alcoliche. La sua formula chimica è C2H5OH. L'acido etanoico, noto anche come acido acetico, è un liquido limpido e incolore che ha un odore acuto e pungente. La sua formula chimica è CH3COOH.

Tavola di comparazione
| Parametri di confronto | etanolo | acido etanoico |
|---|---|---|
| Nome IUPAC | Il nome dell'etanolo dell'Unione internazionale di chimica pura e applicata (IUPAC) è lo stesso come viene chiamato. | Il nome IUPAC (International Union of Pure and Applied Chemistry) di un acido etanoico è un acido acetico. |
| Formule molecolari | La sua formula molecolare è C2H5ooh | La sua formula molecolare è CH3COO. |
| Densità | 0.789 g / cm3 | 1.05 g / cm3 |
| Odour | Ha un gradevole odore simile a un profumo. | Ha un odore pungente o di aceto. |
| Gusto | È bruciante e amaro. | È acido. |
| Punti di ebollizione | Ha un punto di ebollizione di 78.37 ℃ o 173.1 ℉. | Ha un punto di ebollizione di 117.9 ℃ o 244.2 ℉. |
| Punti di fusione | Ha un punto di fusione di -114.1 ℃ o -173.5 ℉. | Ha un punto di fusione di 16.6 ℃ o 61.9 ℉. |
| Gruppo funzionale | Ha l'alcol (-OH) come gruppo funzionale. | Ha acido carbossilico (-OOH) come gruppo funzionale. |
| Esistenza di altri gruppi | I gruppi etile e ossidrile esistono nell'etanolo. | I gruppi metile e carbossilico esistono in etanolo. |
| Il test della cartina di tornasole | Mostra un 7.33 pScala H ad una concentrazione. | Mostra un 2 a 4 pScala H ad una concentrazione. |
| NaHCO3 Test | Non reagisce con bicarbonato di sodio. | Reagisce con il bicarbonato di sodio e rilascia CO2 gas. |
| Prova di Pasqua | Forma Ester solo dopo aver reagito con la presenza di acido etanoico. | Forma estere dopo aver reagito con la presenza di acido solforico. |
| Massa molare | X | X |
| Usato per | Può essere utilizzato come agente sterilizzante o per la preparazione di bevande alcoliche. | Può essere usato come detergente per WC o per fare l'aceto. |
Cos'è l'etanolo?
Il nome dell'etanolo dell'Unione internazionale di chimica pura e applicata (IUPAC) è lo stesso come viene chiamato.
La sua formula molecolare è 'C2H5OH,' e la sua densità è di 0.789 g/cm3. Ha un sapore amaro, bruciante e gradevole profumo-simile all'odore. Può essere utilizzato come agente sterilizzante o per la preparazione di bevande alcoliche.
La massa molare di questo acido è 46.07 g/mol. Il punto di fusione dell'etanolo è -114.1 ℃ o -173.5 ℉. E il suo punto di ebollizione è 78.37 ℃ o 173.1 ℉. Durante la fermentazione si forma etanolo utilizzando lieviti come Saccharomyces cerevisiae o Schizo-saccharomyces.
Il Litmus Paper Test presenta una scala di 7.33 pH (potenziale di idrogeno). Non reagisce con il bicarbonato di sodio. Forma Ester solo dopo una reazione con la presenza di acido etanoico. Ha l'alcol (-OH) come gruppo funzionale. Oltre a questo, esistono gruppi etilici e idrossilici.

Cos'è l'acido etanoico?
Il nome IUPAC (International Union of Pure and Applied Chemistry) di un acido etanoico è un acido acetico. Ha un sapore aspro e un odore pungente o di aceto. La sua formula molecolare è "CH3COOH" e la sua densità è di 1.05 g/cm3. Può essere usato come detergente per WC o per fare l'aceto.
Presenta una scala di pH 2-4 (potenziale di idrogeno) nel test della cartina di tornasole. Reagisce con il bicarbonato di sodio e rilascia CO2 gas. Forma anche estere dopo la reazione con la presenza di acido solforico.
Ha acido carbossilico (-OOH) come gruppo funzionale. Oltre a questo, esistono gruppi metilici e carbossilici.
La massa molare di questo acido è 60.052 g/mol. Durante la fermentazione, i batteri Acetobacter formano acido etanoico. Quando l'acido etanoico passa attraverso il liquido di calce, diventa opaco e diventa CO2 gas. Il suo punto di ebollizione è 17.9 ℃ o 244.2 ℉. E il punto di fusione è 16.6 ℃ o 61.9 ℉.
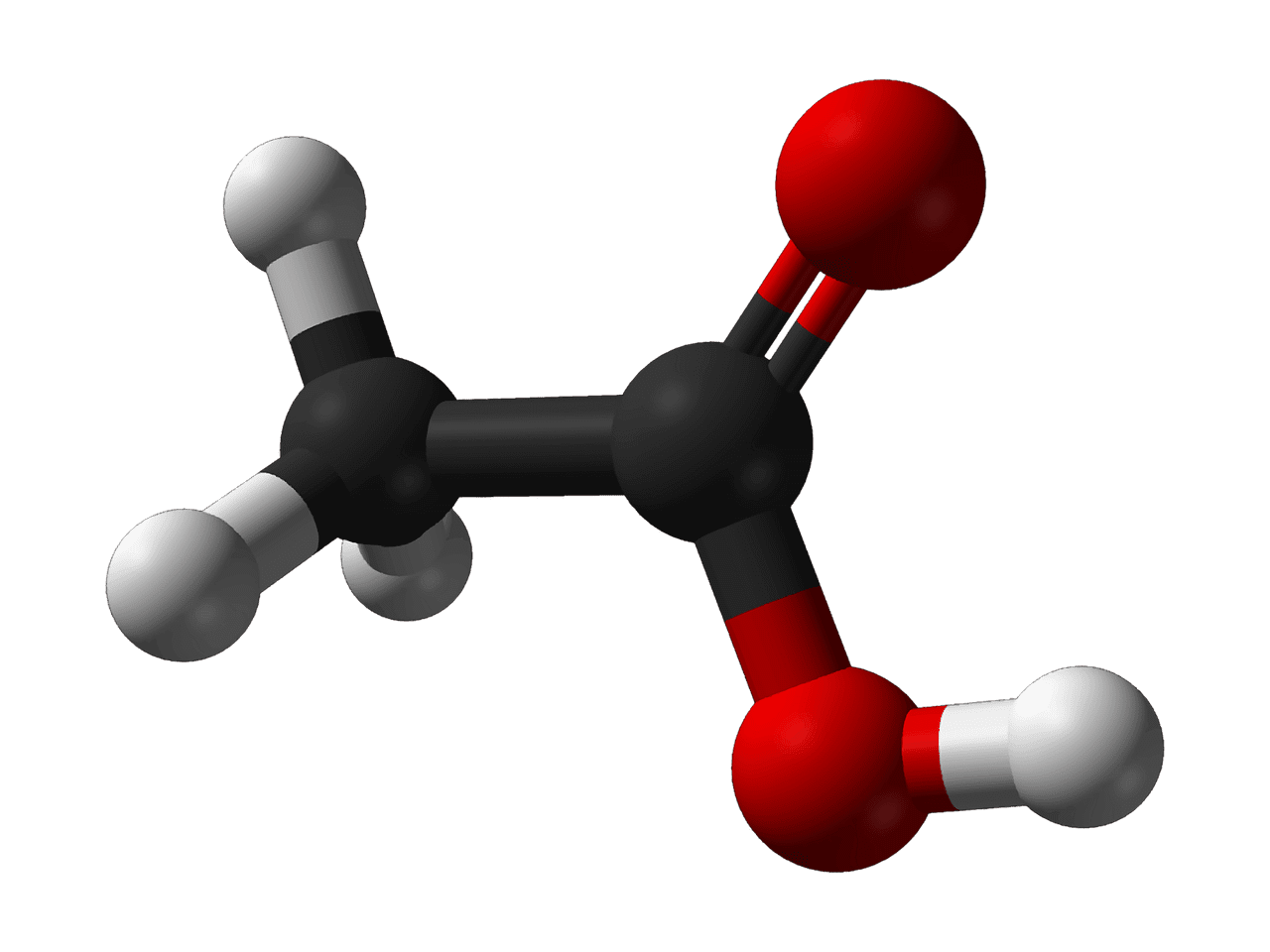
Principali differenze tra etanolo e acido etanoico
- La formula molecolare dell'etanolo è C2H5OH, mentre l'acido etanoico è CH3COO.
- 0.789 g/cm3 è la densità dell'etanolo, mentre 1.05 g/cm3 è l'acido etanoico.
- Il primo ha un gradevole odore simile a un profumo. Il secondo invece ha un odore pungente o di aceto.
- L'etile ha un sapore poco bruciante e amaro. L'acido acetico ha un sapore acido.
- Il punto di ebollizione dell'etanolo è 78.37 ℃ o 173.1 ℉. Al contrario, 117.9 ℃ o 244.2 ℉ dell'acido etanoico.
- Il punto di fusione del primo è -114.1 ℃ o -173.5 ℉. D'altra parte, il secondo è 16.6 ℃ o 61.9 ℉.
- Il precedente ha l'alcol (-OH) come gruppo funzionale. Al contrario, il successivo ha un acido carbossilico (-OOH).
- L'etanolo mostra una scala di pH 7.33 nella cartina di tornasole, mentre l'acido etanoico mostra una scala di pH da 2 a 4.
- Il primo non reagisce con il bicarbonato di sodio. Al contrario, quest'ultimo reagisce e rilascia CO2 gas.
- La massa molare dell'etanolo è 46.07 g/mol, mentre la massa molare dell'acido etanoico è 60.052 g/mol.
- https://pubs.acs.org/doi/abs/10.1021/je300810p
- https://www.sciencedirect.com/science/article/pii/S0378775301010679
- https://www.sciencedirect.com/science/article/pii/S0022328X04004668
Questo articolo è stato scritto da: Supriya Kandekar
Ultimo aggiornamento: 11 giugno 2023

Piyush Yadav ha trascorso gli ultimi 25 anni lavorando come fisico nella comunità locale. È un fisico appassionato di rendere la scienza più accessibile ai nostri lettori. Ha conseguito una laurea in scienze naturali e un diploma post-laurea in scienze ambientali. Puoi leggere di più su di lui sul suo pagina bio.


Questo post è una boccata d'aria fresca e offre conoscenze approfondite sull'etanolo e sull'acido etanoico.
Assolutamente, è informativo e illuminante.
Queste informazioni sono fondamentali per gli appassionati di chimica che desiderano approfondire le proprie conoscenze.
Come persona che ama la chimica, apprezzo la profondità di questa spiegazione.
Essendo una persona con un vivo interesse per la chimica, trovo che questo articolo sia un'eccezionale fonte di informazioni.
Effettivamente è una spiegazione ben articolata ed esauriente dell'argomento.
Sono felice che esista questo post, molte persone non conoscono il contrasto tra etanolo e acido etanoico.
Assolutamente sì, i dettagli scientifici aiutano i lettori a capire.
Questo articolo è un'eccellente risorsa per studenti e professionisti nel campo della chimica.
L'analisi approfondita distingue questo articolo dagli altri.
Certamente offre conoscenze preziose che contribuiscono a una comprensione più profonda dell’argomento.
Il post distingue efficacemente tra etanolo e acido etanoico utilizzando prove scientifiche.
D'accordo, è raro imbattersi in contenuti così ben studiati.
Il contenuto informativo testimonia la competenza dell'autore in materia.
Apprezzo la natura dettagliata e obiettiva di questo post.
Il confronto scientificamente accurato fornisce informazioni preziose.
Trovo che la tabella comparativa dettagliata e i principali punti salienti siano molto utili e approfonditi.
La chiarezza delle informazioni qui presentate è encomiabile.
Sono d'accordo, questo post offre una visione olistica delle differenze tra etanolo e acido etanoico.
Questo è un articolo molto informativo che chiarisce ogni dubbio sulla differenza tra etanolo e acido etanoico.
Finalmente capisco la distinzione tra i due grazie a questo articolo.
Sono d'accordo, questo è spiegato chiaramente in modo scientifico.
La spiegazione dettagliata fornita qui è estremamente utile e arricchente.
Assolutamente, migliora la comprensione dell'argomento da parte del lettore.