Наука в нашей повседневной жизни содержит множество аспектов. Все, что мы видим невооруженным глазом, состоит из миллиардов атомов и молекул.
На языке химии процесс, посредством которого атомы вступают в контакт друг с другом и образуют объекты, называется химической связью.
Основные выводы
- Ионные связи образуются, когда атомы переносят электроны, создавая заряженные ионы, которые притягиваются друг к другу, в то время как ковалентные связи включают атомы, разделяющие электроны, что приводит к отсутствию общего заряда.
- Ионные соединения имеют высокие температуры плавления и кипения из-за сильных электростатических сил между ионами. Напротив, ковалентные соединения имеют более низкие температуры плавления и кипения из-за более слабых межмолекулярных сил.
- Ковалентные соединения могут растворяться в различных полярных растворителях, но ионные соединения легче растворяются в полярных растворителях, таких как вода.
Ионные против ковалентных
Разница между ионный а ковалентная заключается в том, что, хотя оба они являются процессами химической связи, первый относится к связи, при которой атом притягивает те атомы, которые противоположны его силе притяжения. В то время как последний относится к связи, в которой два неметаллы делят свои электроны поровну без потери своих электронов.

Ионная связь относится к химическому процессу, в котором два противоположно заряженных иона соединяются друг с другом, образуя соединение.
С другой стороны, ковалентная связь возникает именно между неметаллами. Это не требует притяжения между противоположными ионами, а скорее связи между одинаково заряженными ионами.
Сравнительная таблица
| Параметры сравнения | ионный | Ковалентная |
|---|---|---|
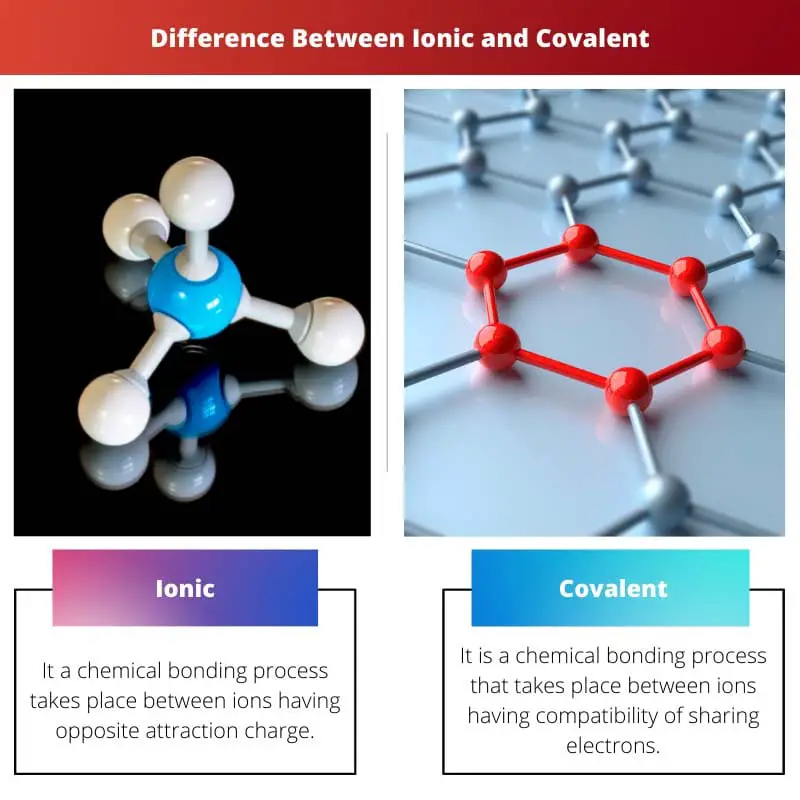
| Смысл | Это процесс химической связи происходит между ионами, имеющими противоположный заряд притяжения. | Это процесс химической связи, который происходит между ионами, обладающими совместимостью общих электронов. |
| Происходит между | Металлы и неметаллы. | Неметаллы |
| Область | Он существует только в твердом состоянии. | Он существует в твердом, газообразном и жидком состояниях, во всех трех состояниях. |
| Температура плавления | Эта связь плавится при очень высокой температуре плавления. | Эта связь плавится при сравнительно низкой температуре плавления. |
| Точка кипения | Эта связь плавится при очень высокой температуре кипения. | Эта связь плавится при очень низкой температуре плавления. |
| Проведение электричества | Эти связи могут проводить электричество. | Эти связи не могут проводить электричество. |
| Доступность | Менее употребителен | Чаще |
| Образовался из-за | Когда два противоположно заряженных иона, которые совместимы друг с другом, соединяются вместе, создается эта связь. Это приводит к потере электронов одним и приобретению электронов другим. | Эта связь основана не на переносе электронов, а на обмене электронами. Это не вызывает потери или приобретения электронов ни в одном из присоединяющихся ионов. |
Что такое ионический?
Ионный относится к процессу химической связи или соединения двух атомов с целью создания нового соединения или объекта.
В этом процессе два атома собираются вместе в одном месте, и требуется, чтобы эти два атома имели разный и противоположный электрический заряд, чтобы завершить этот процесс.
Один атом, который имеет положительный заряд, широко известен как металл. Он отдает часть своих электронов другому атому, который содержит отрицательный заряд и называется неметаллом.
Популярным примером этой связи является поваренная соль. Состоит из натрия и хлора.
- Натрий содержит 11 протонов и 11 электронов. Один электрон этого атома присутствует во внешнем цикле и несет положительный заряд.
- Хлор содержит 17 протонов и 17 электронов и имеет отрицательный заряд.
- После связывания натрий отдает свой внешний электрон хлору.
Что такое Ковалентный?
Ковалентная связь — это еще один важный процесс химической связи, в ходе которого образуются новые соединения и вещества.
Он не нуждается в положительном и отрицательном заряде участвующих атомов, и поэтому он объединяет только неметаллы (атомы, имеющие отрицательный заряд).
Очень известным примером этой связи является хлороводород (HCl).
- Здесь хлор имеет 7 атомов по внешнему периметру.
- в то время как водород имеет 1 электрон.
- Эти два реагировать вместе и объединяются в идеально сбалансированную молекулу.
Основные различия между ионным и ковалентным
- Ионные можно увидеть только в твердом состоянии, в то время как ковалентные можно увидеть во всех трех состояниях вещества.
- Ионные менее вероятны и не очень распространены, в то время как ковалентные имеют высокую вероятность и очень распространены.
- https://www.tandfonline.com/doi/abs/10.1080/10408437108243425
- https://iopscience.iop.org/article/10.1088/0953-8984/11/30/309/meta
Последнее обновление: 23 июля 2023 г.

Пиюш Ядав последние 25 лет работал физиком в местном сообществе. Он физик, увлеченный тем, чтобы сделать науку более доступной для наших читателей. Он имеет степень бакалавра естественных наук и диплом о высшем образовании в области наук об окружающей среде. Подробнее о нем можно прочитать на его био страница.

Действительно хорошо проработанная статья, ее содержание действительно отражает тему химической связи.
Безусловно, представленная здесь информация очень ценна для иллюстрации химических процессов.
Статья, безусловно, углубила мое понимание концепций химии, очень хорошо объясненный пост.
Согласованный. Подробные объяснения значительно расширили мои знания о химических процессах.
Подробно, подробно и информативно. Подобная статья действительно обогащает понимание химической связи.
Безусловно, глубина информации действительно обогащает любого, кто интересуется химией.
Я очень впечатлен содержанием статьи, она предлагает очень хорошо структурированное понимание концепций химической связи.
Я бы порекомендовал эту статью однокурсникам, это очень полезное и увлекательное чтение.
Безусловно, детали и пояснения, представленные здесь, делают книгу отличным чтением как для студентов, так и для энтузиастов.
Я согласен с вами, объяснения очень дружелюбны к студентам.
Очень подробная и информативная статья, спасибо. Несмотря на то, что я знаю эти концепции, я ценю, насколько хорошо идеи были здесь описаны.
Я полностью согласен с вами обоими. Это очень познавательная статья
Полностью согласен! Детали хорошо написаны, а определения здесь поучительны.
Очень интересно читать. Это отличное напоминание об основных понятиях химии.
Статья действительно информативна и полезна для изучения основ химии.
Безусловно, хорошо написанная информативная статья, которая помогает понять принципы склеивания.
Эта статья очень хорошо структурирована и представляет подробную информацию в очень организованной форме.
Согласен, структура статьи очень облегчает понимание понятий
Этот контент действительно помогает понять важность химии в нашей повседневной жизни.
Определенно, химия окружает нас повсюду, и понимание лежащих в ее основе концепций имеет решающее значение.
Я ценю четкое различие, сделанное между ионной и ковалентной связью в статье, очень информативной.
Действительно, ясность в различении двух типов связей делает статью интересной для чтения.
Мне понравился уровень детализации объяснений, это, безусловно, улучшает понимание химической связи.
Определенно, статья дает глубокое понимание темы химической связи.
Уровень детализации определенно повышает ценность статьи и делает ее отличным ресурсом для учащихся.