Có rất nhiều thứ trong tự nhiên liên kết với nhau để tạo thành một cấu trúc mới hoặc một loại nguyên tố mới. Ví dụ: Xét nước, nó được hình thành như thế nào?
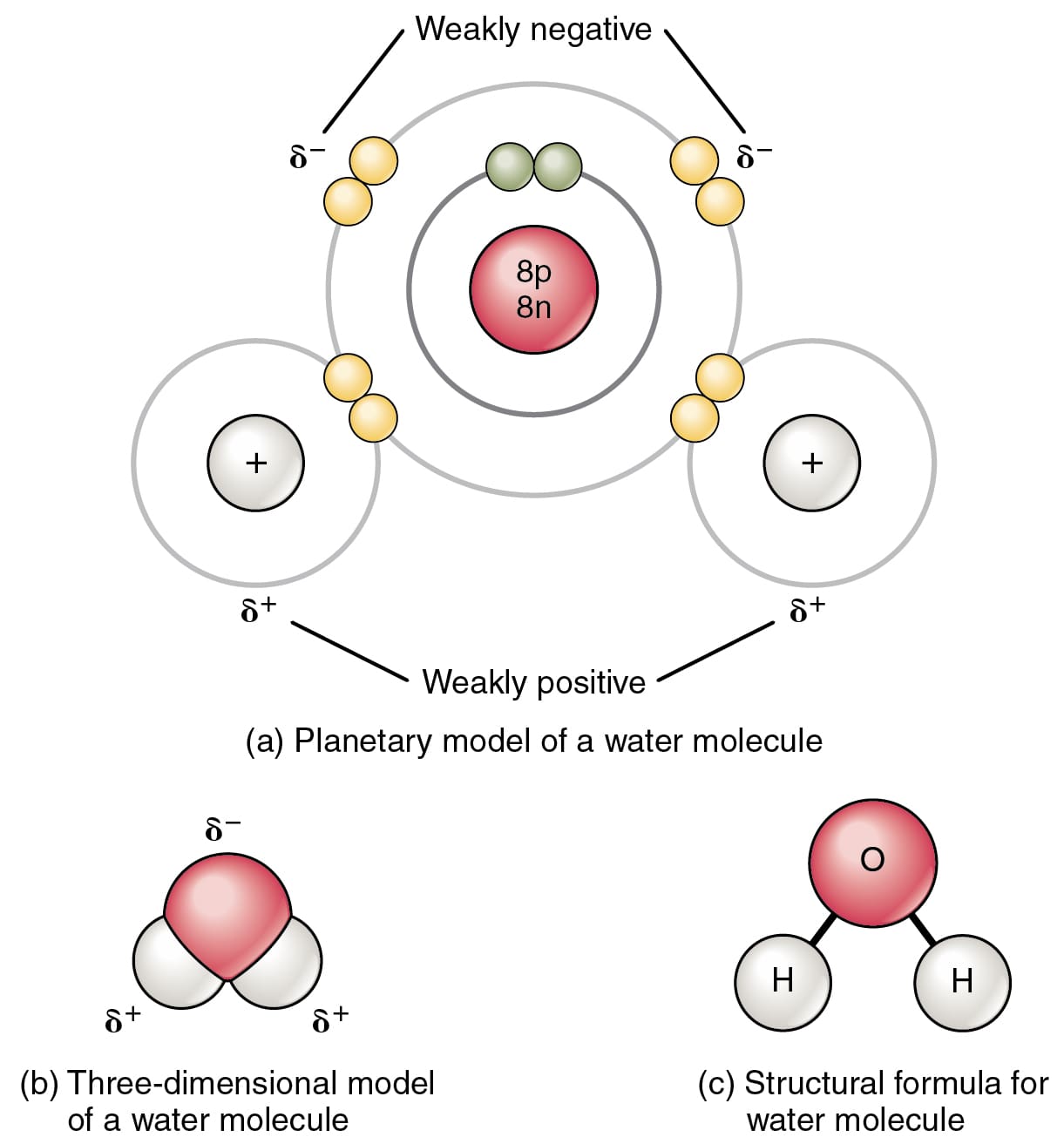
Nó được hình thành do quá trình liên kết hóa học trong đó 2 nguyên tử Hydro và 1 nguyên tử Oxy liên kết để tạo thành trạng thái lỏng của nước. Liên kết hóa học rất quan trọng đối với các sinh vật sống và hoạt động bình thường của các bộ phận cơ thể của chúng.
Chìa khóa chính
- Liên kết ion hình thành giữa các nguyên tố kim loại và phi kim thông qua chuyển điện tử, trong khi liên kết cộng hóa trị hình thành giữa các phi kim thông qua chia sẻ điện tử.
- Liên kết kim loại xảy ra giữa các nguyên tử kim loại, liên quan đến một biển các electron được định vị.
- Hợp chất ion có nhiệt độ nóng chảy và sôi cao. Các hợp chất cộng hóa trị có điểm nóng chảy và sôi thấp hơn, và các hợp chất kim loại có điểm nóng chảy và sôi khác nhau.
Trái phiếu ion vs cộng hóa trị vs kim loại
Liên kết ion được hình thành giữa các ion có điện tích trái dấu. Những ion này có thể được hình thành bằng cách chuyển một hoặc nhiều electron từ nguyên tử này sang nguyên tử khác. Liên kết cộng hóa trị được hình thành khi các nguyên tử có chung một hoặc nhiều cặp electron. Loại liên kết này xảy ra giữa hai nguyên tử phi kim loại. Liên kết kim loại được hình thành giữa các nguyên tử kim loại. Trong liên kết kim loại, các electron hóa trị không cố định trên một nguyên tử cụ thể mà có thể tự do di chuyển trong toàn bộ mạng kim loại.

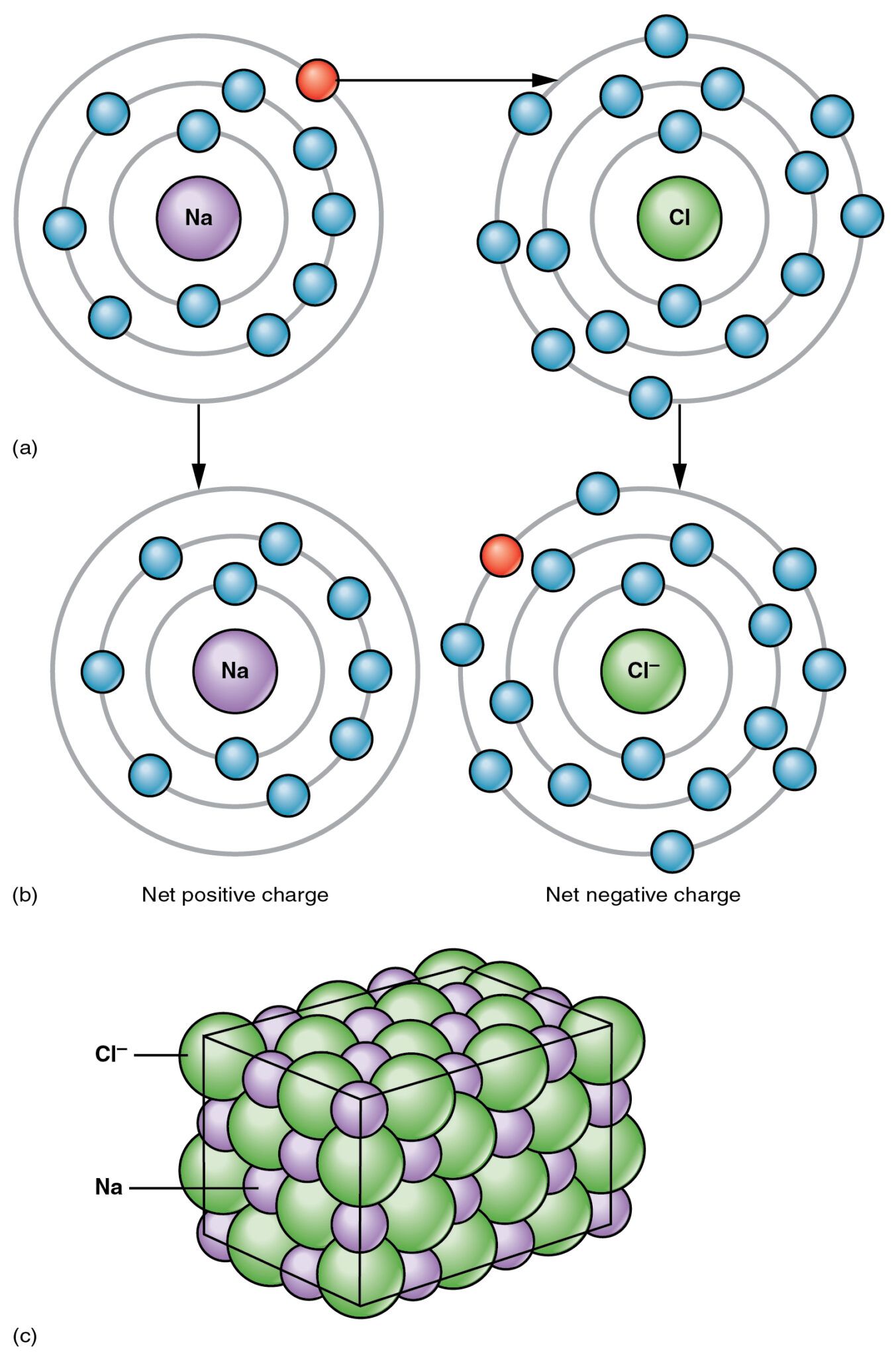
Liên kết ion là sự chuyển electron từ nguyên tử kim loại sang nguyên tử phi kim loại, ví dụ, xét Natri Clorua; Số nguyên tử của natri là 11 và cấu hình điện tử là 2,8,1 Natri có thêm một electron ở lớp vỏ ngoài cùng.
Mặt khác, Closố nguyên tử của nó là 17 và cấu hình điện tử là 2,8,7 Clo có 7 electron ở lớp vỏ ngoài cùng nên Clo cần thêm một electron để hoàn thành lớp vỏ ngoài cùng nên tất cả các nguyên tử sẽ ổn định.
Vì Natri có thêm một điện tử khi Natri phản ứng với Chorine, Natri sẽ tặng thêm điện tử đó cho Chorine. Trong quá trình này Natri trở thành ion mang điện tích dương (Na+ ) và sau khi nhận điện tử Chorine trở thành ion mang điện tích âm (Cl–).
Hai ion tích điện trái dấu này được giữ bởi lực hút tĩnh điện mạnh được gọi là Liên kết ion.
A Trái phiếu cộng hóa trị được hình thành khi hai hay nhiều nguyên tử liên kết với nhau bằng cách dùng chung electron. Ví dụ, xem xét sự hình thành của khí Oxy (O2), chúng ta sẽ lấy 2 nguyên tử oxy vì chúng ta biết số lượng electron trong Oxy là 8 và có 6 electron hóa trị ở lớp vỏ ngoài.
Khi hai lớp vỏ hóa trị bên ngoài chứa 6 electron của oxy nhận thêm 2 electron, nó sẽ ổn định, vì Quy tắc Octet của nó sẽ được đáp ứng.
Để tự ổn định, hai nguyên tử Oxy này kết hợp và chia sẻ lẫn nhau hai nguyên tử Oxy để tạo thành khí Oxy, đây được gọi là Liên kết cộng hóa trị.
Liên kết kim loại là lực hút tĩnh điện giữa các ion kim loại được sắp xếp theo cấu trúc mạng tinh thể (mẫu lặp lại đều đặn) và sự chuyển động tự do của các electron xung quanh chúng.
Trong cấu trúc kim loại, chỉ có các ion kim loại, các ion kim loại này được sắp xếp cạnh nhau theo kiểu lặp lại đều đặn và các electron chuyển động tự do hoạt động như chất keo và giữ cấu trúc ở đúng vị trí.
Đây là lực hút rất mạnh nên nhiệt độ nóng chảy và nhiệt độ sôi của kim loại rất cao. Các electron chuyển động tự do là nguyên nhân khiến kim loại dẫn điện tốt.
Bảng so sánh
| Các thông số so sánh | Sự gắn kết | Trái phiếu cộng hóa trị | Liên kết kim loại |
|---|---|---|---|
| đào tạo | Kim loại và phi kim loại | hai phi kim | Các nguyên tử tích điện dương và các electron tự do trôi nổi |
| Polarity | Cao | Thấp | Không phân cực |
| hình dạng của phân tử | Không có hình dạng xác định, cấu trúc mạng tinh thể | Hình dạng cụ thể | Không có hình dạng nhất định |
| Các ví dụ | Natri clorua, axit sunfuric | Mêtan, Axit Choric Hydro | Natri, Magie |
| Độ nóng chảy | Điểm nóng chảy cao | Điểm nóng chảy thấp | Điểm nóng chảy cao |
Liên kết ion là gì?
Liên kết ion diễn ra khi có sự tăng và giảm electron giữa kim loại và phi kim, để liên kết ion diễn ra thì phải có ít nhất một kim loại.
Ví dụ, một nguyên tử Magiê bị mất hai electron và tạo thành các ion Magiê tích điện dương và đó là các ion kim loại; mặt khác, nguyên tử Oxy nhận thêm hai electron và trở thành ion oxit tích điện âm và nó là phi kim.
Hai nguyên tử này hút nhau khi một nguyên tử dương và nguyên tử kia âm và lực hút này được gọi là Liên kết ion.
Trái phiếu cộng hóa trị là gì?
Liên kết cộng hóa trị chỉ diễn ra ở phi kim, nó không bao giờ có thể xảy ra với kim loại, nó xảy ra khi hai hoặc nhiều hơn hai phi kim chia sẻ lẫn nhau một cặp electron.
Ví dụ, chúng ta có hai nguyên tử Clo và lớp vỏ ngoài của các nguyên tử Clo này chồng lên nhau và dùng chung một cặp electron để tạo thành một nguyên tố.
Hai nguyên tử được liên kết với nhau tạo thành một liên kết rất mạnh giữ chúng lại với nhau. Loại liên kết này được gọi là liên kết cộng hóa trị.
Trái phiếu kim loại là gì?
Liên kết kim loại xảy ra giữa các kim loại, các kim loại mất electron để tạo thành các ion dương và các electron lỏng lẻo trở thành các electron được định vị, điều đó có nghĩa là chúng không còn liên kết với bất kỳ ion nào và trôi nổi trong một biển các electron được định vị.
Vì các ion dương và các electron được định vị là âm nên sẽ có một lực hút giữa chúng. Lực hút tĩnh điện giữa các ion dương và các electron được định vị âm được gọi là Liên kết kim loại.
Sự khác biệt chính giữa liên kết ion, cộng hóa trị và kim loại
- Trong liên kết ion, một nguyên tử cung cấp electron cho nguyên tử khác, trong liên kết cộng hóa trị, hai nguyên tử trao đổi electron hóa trị, trong khi ở mạng kim loại liên kết kim loại bao gồm các nguyên tử dùng chung một số electron.
- trong ion Năng lượng trái phiếu của một liên kết cao hơn so với liên kết kim loại, điều tương tự cũng xảy ra với Liên kết cộng hóa trị, trong khi ở Liên kết kim loại có ít năng lượng liên kết hơn so với các liên kết chính khác.
- Liên kết ion là một chất dẫn điện yếu, mặt khác, Liên kết cộng hóa trị là một chất dẫn điện rất yếu, trong khi Liên kết kim loại là một chất dẫn điện mạnh.
- Liên kết ion có thể ở trạng thái rắn, Liên kết cộng hóa trị có thể ở trạng thái rắn, lỏng và khí, trong khi liên kết kim loại chỉ có thể ở trạng thái rắn.
- Liên kết ion không có đặc điểm dễ uốn giống với Liên kết cộng hóa trị, trong khi Liên kết kim loại có đặc điểm dễ uốn
- https://journals.aps.org/pr/abstract/10.1103/PhysRev.171.701
- https://www.tandfonline.com/doi/abs/10.1080/00150199208019535
Cập nhật lần cuối: ngày 02 tháng 2023 năm XNUMX

Piyush Yadav đã dành 25 năm qua làm việc với tư cách là một nhà vật lý trong cộng đồng địa phương. Anh ấy là một nhà vật lý đam mê làm cho khoa học dễ tiếp cận hơn với độc giả của chúng tôi. Ông có bằng Cử nhân Khoa học Tự nhiên và Bằng Sau Đại học về Khoa học Môi trường. Bạn có thể đọc thêm về anh ấy trên trang sinh học.


Sự phức tạp của sự tương tác giữa các loại liên kết khác nhau thực sự rất hấp dẫn.
Bài viết này chắc chắn đã nâng cao kiến thức của tôi về liên kết ion, cộng hóa trị và kim loại. Tác giả đã thực hiện một công việc tuyệt vời trong việc trình bày thông tin.
Lời giải thích về cách các nguyên tử liên kết với nhau để tạo thành các loại liên kết khác nhau đã được minh họa rõ ràng. Làm tốt lắm về bài viết này!
Bài viết được viết rõ ràng và có rất nhiều thông tin có giá trị ở đây. Tôi đánh giá cao bảng so sánh, nó thực sự đặt ra mọi thứ theo quan điểm.
Bảng so sánh thực sự rất hữu ích và ngắn gọn.
Rõ ràng là tác giả có sự hiểu biết sâu sắc về chủ đề này và đã truyền đạt những nguyên tắc này một cách hiệu quả.
Đây là một bài viết rất nhiều thông tin. Nó giải thích rõ ràng sự khác biệt giữa liên kết ion, cộng hóa trị và kim loại và là tài liệu tham khảo tuyệt vời cho bất kỳ ai nghiên cứu về hóa học.
Đã đồng ý! Nó cung cấp một cái nhìn tổng quan toàn diện về chủ đề.
Tôi tin rằng bài viết này sẽ rất có ích cho sinh viên ngành hóa học.
Lời giải thích này cực kỳ kỹ lưỡng và sâu sắc. Tôi cảm thấy như mình thực sự đã học được điều gì đó.