प्रकृति में ऐसी बहुत सी चीज़ें हैं जो एक-दूसरे से जुड़कर एक नई संरचना या तत्वों का एक नया वर्ग बनाती हैं। उदाहरण के लिए: पानी पर विचार करें, यह कैसे बनता है?
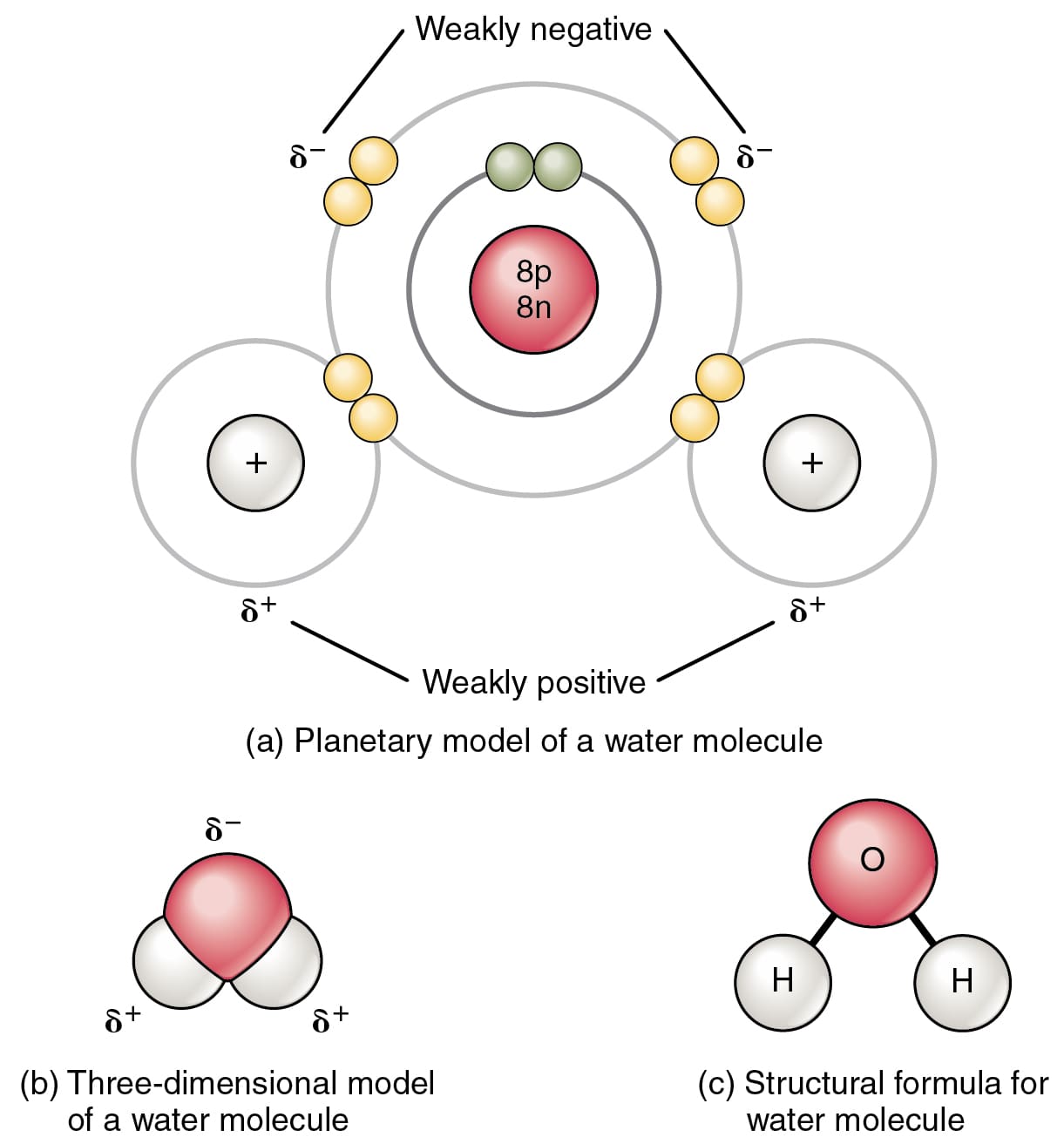
यह रासायनिक बंधन की प्रक्रिया से बनता है जिसमें हाइड्रोजन के 2 परमाणु और ऑक्सीजन का 1 परमाणु आपस में जुड़कर पानी की तरल अवस्था बनाते हैं। रासायनिक बंधन जीवित जीवों और उनके शरीर के अंगों के समुचित कार्य के लिए महत्वपूर्ण है।
चाबी छीन लेना
- आयनिक बंधन धातु और गैर-धातु तत्वों के बीच इलेक्ट्रॉन हस्तांतरण के माध्यम से बनते हैं, जबकि सहसंयोजक बंधन इलेक्ट्रॉन साझाकरण के माध्यम से गैर-धातुओं के बीच बनते हैं।
- धातु परमाणुओं के बीच धात्विक बंधन होते हैं, जिसमें डेलोकलाइज्ड इलेक्ट्रॉनों का एक समुद्र शामिल होता है।
- आयनिक यौगिकों में उच्च गलनांक और क्वथनांक होते हैं। सहसंयोजक यौगिकों के गलनांक और क्वथनांक कम होते हैं, और धात्विक यौगिकों के गलनांक और क्वथनांक अलग-अलग होते हैं।
आयनिक बनाम सहसंयोजक बनाम धात्विक बांड
विपरीत आवेश वाले आयनों के बीच आयनिक बंधन बनते हैं। ये आयन एक या अधिक इलेक्ट्रॉनों के एक परमाणु से दूसरे परमाणु में स्थानांतरण से बन सकते हैं। सहसंयोजक बंधन तब बनते हैं जब परमाणु एक या अधिक इलेक्ट्रॉन जोड़े साझा करते हैं। इस प्रकार का बंधन दो गैर-धातु परमाणुओं के बीच होता है। धातुओं के परमाणुओं के बीच धात्विक बंधन बनते हैं। एक धात्विक बंधन में, वैलेंस इलेक्ट्रॉन किसी विशेष परमाणु पर स्थानीयकृत नहीं होते हैं, बल्कि संपूर्ण धातु जाली में घूमने के लिए स्वतंत्र होते हैं।

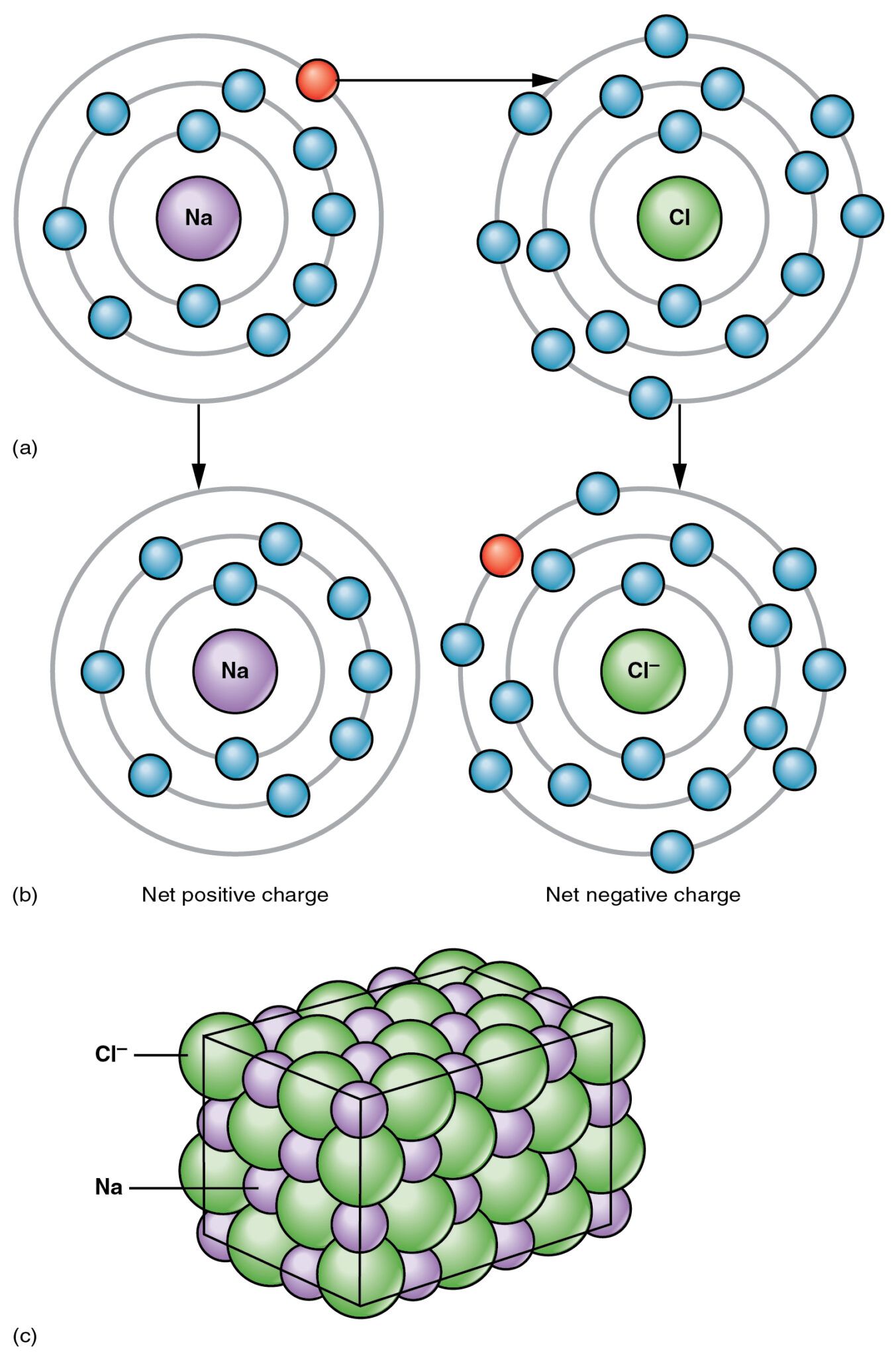
आयनिक बॉन्ड एक धात्विक परमाणु से गैर-धात्विक परमाणु में इलेक्ट्रॉनों का स्थानांतरण है, उदाहरण के लिए, सोडियम क्लोराइड पर विचार करें; सोडियम की परमाणु संख्या 11 और इलेक्ट्रॉनिक विन्यास 2,8,1 है। सोडियम के सबसे बाहरी कोश में एक अतिरिक्त इलेक्ट्रॉन होता है।
दूसरी ओर, क्लोरीनइसकी परमाणु संख्या 17 है और इलेक्ट्रॉनिक विन्यास 2,8,7 है। क्लोरीन के सबसे बाहरी कोश में 7 इलेक्ट्रॉन होते हैं, इसलिए क्लोरीन को अपने सबसे बाहरी कोश को पूरा करने के लिए एक और इलेक्ट्रॉन की आवश्यकता होती है, इसलिए सभी परमाणु स्थिर रहेंगे।
चूँकि जब सोडियम कोरीन के साथ प्रतिक्रिया करता है तो सोडियम में एक अतिरिक्त इलेक्ट्रॉन होता है, सोडियम उस अतिरिक्त इलेक्ट्रॉन को कोरीन को दान कर देता है। इस प्रक्रिया में, सोडियम धनावेशित आयन (Na+) बन जाता है और इलेक्ट्रॉन ग्रहण करने के बाद कोरीन ऋणावेशित आयन (Cl) बन जाता है।-).
ये दो विपरीत रूप से आवेशित आयन एक मजबूत इलेक्ट्रोस्टैटिक आकर्षण बल द्वारा धारण किए जाते हैं जिसे आयनिक बॉन्ड के रूप में जाना जाता है।
A सहसंयोजक बंधन यह तब बनता है जब दो या दो से अधिक परमाणु इलेक्ट्रॉनों के आपसी आदान-प्रदान से एक साथ जुड़ते हैं। उदाहरण के लिए, ऑक्सीजन गैस (O2) के निर्माण पर विचार करते हुए हम ऑक्सीजन के 2 परमाणु लेंगे क्योंकि हम जानते हैं कि ऑक्सीजन में इलेक्ट्रॉन की संख्या 8 है और बाहरी आवरण में 6 वैलेंस इलेक्ट्रॉन हैं।
जब ऑक्सीजन के 6 इलेक्ट्रॉनों वाले इन दो बाहरी संयोजकता कोशों को 2 और इलेक्ट्रॉन मिलेंगे तो यह स्थिर हो जाएगा, क्योंकि इसका ऑक्टेट नियम पूरा हो जाएगा।
स्वयं को स्थिर करने के लिए ऑक्सीजन के ये दो परमाणु आपस में जुड़कर ऑक्सीजन के दो परमाणुओं को आपस में साझा करके ऑक्सीजन गैस बनाते हैं, इसे सहसंयोजक बंधन कहते हैं।
धात्विक बंधन एक जाली (नियमित दोहराव पैटर्न) संरचना में व्यवस्थित धातु आयनों और उनके चारों ओर इलेक्ट्रॉनों के मुक्त-फ्लोटिंग के बीच इलेक्ट्रोस्टैटिक आकर्षण है।
किसी धात्विक संरचना में, केवल धातु आयन होते हैं, ये धातु आयन एक नियमित दोहराव पैटर्न में एक साथ व्यवस्थित होते हैं, और मुक्त-तैरने वाले इलेक्ट्रॉन गोंद के रूप में कार्य करते हैं और संरचना को अपनी जगह पर बनाए रखते हैं।
यह बहुत प्रबल आकर्षण है इसलिए धातुओं का गलनांक और क्वथनांक बहुत अधिक होता है। मुक्त-फ़्लोटिंग इलेक्ट्रॉन ही कारण हैं कि धातु बिजली का अच्छा संवाहक है।
तुलना तालिका
| तुलना के पैरामीटर | आयोनिक बंध | सहसंयोजक बंधन | धात्विक बंधन |
|---|---|---|---|
| निर्माण | धातु और अधातु | दो अधातु | परमाणुओं और मुक्त-तैरने वाले इलेक्ट्रॉनों को सकारात्मक रूप से चार्ज करता है |
| ध्रुवाभिसारिता | हाई | निम्न | गैर ध्रुवीय |
| अणु का आकार | कोई निश्चित आकार, जाली संरचना नहीं | निश्चित आकार | कोई निश्चित आकार नहीं |
| उदाहरण | सोडियम क्लोराइड, सल्फ्यूरिक एसिड | मीथेन, हाइड्रो कोरिक एसिड | सोडियम, मैग्नेशियम |
| गलनांक | उच्च पिघलने बिंदु | कम गलनांक | उच्च गलनांक |
आयनिक बांड क्या है?
आयनिक बंधन तब होता है जब किसी धातु और गैर-धातु के बीच इलेक्ट्रॉनों की प्राप्ति और हानि होती है, आयनिक बंधन के लिए कम से कम एक धातु होनी चाहिए।
उदाहरण के लिए, एक मैग्नीशियम परमाणु ने दो इलेक्ट्रॉन खो दिए और मैग्नीशियम आयन बनाए जो धनात्मक रूप से आवेशित होते हैं और ये धातु आयन होते हैं; दूसरी ओर, ऑक्सीजन परमाणु दो इलेक्ट्रॉन प्राप्त करता है और एक नकारात्मक चार्ज ऑक्साइड आयन बन जाता है और यह एक गैर-धातु है।
ये दोनों परमाणु एक दूसरे को आकर्षित करते हैं क्योंकि एक सकारात्मक है और दूसरा नकारात्मक है और इस आकर्षण को आयनिक बॉन्डिंग कहा जाता है।
सहसंयोजक बंधन क्या है?
सहसंयोजक बंधन केवल गैर-धातु में होता है, यह धातुओं के साथ कभी नहीं हो सकता है, यह तब होता है जब दो या दो से अधिक गैर-धातुएं परस्पर इलेक्ट्रॉनों की एक जोड़ी साझा करती हैं।
उदाहरण के लिए, हमारे पास दो क्लोरीन परमाणु हैं और इन क्लोरीन परमाणुओं के बाहरी गोले ओवरलैप होते हैं और एक तत्व बनाने के लिए एक इलेक्ट्रॉन की एक जोड़ी साझा करते हैं।
दो परमाणु आपस में जुड़ जाते हैं जो एक बहुत मजबूत बंधन बनाता है जो उन्हें एक साथ रखता है। इस प्रकार के बंधन को सहसंयोजक बंधन कहा जाता है।
धात्विक बांड क्या है?
धातुओं के बीच धात्विक बंधन होता है, धातुएँ सकारात्मक आयन बनाने के लिए इलेक्ट्रॉन खो देती हैं और ढीले इलेक्ट्रॉन डेलोकलाइज़्ड इलेक्ट्रॉन बन जाते हैं, जिसका अर्थ है कि वे अब किसी भी आयन से जुड़े नहीं रहते हैं और डेलोकलाइज़्ड इलेक्ट्रॉनों के समुद्र में इधर-उधर तैरते रहते हैं।
चूंकि आयन सकारात्मक हैं और डेलोकलाइज्ड इलेक्ट्रॉन नकारात्मक हैं, इसलिए उनके बीच आकर्षण होगा। सकारात्मक आयनों और नकारात्मक डेलोकलाइज्ड इलेक्ट्रॉनों के बीच इलेक्ट्रोस्टैटिक आकर्षण को धात्विक बंधन कहा जाता है।
आयनिक, सहसंयोजक और धात्विक बंधों के बीच मुख्य अंतर
- आयनिक बंधन में एक परमाणु दूसरे को इलेक्ट्रॉन प्रदान करता है, सहसंयोजक बंधन में दो परमाणु वैलेंस इलेक्ट्रॉनों का आदान-प्रदान करते हैं, जबकि धात्विक बंधन में धातु जाली में परमाणु शामिल होते हैं जो कई इलेक्ट्रॉनों को साझा करते हैं।
- आयनिक में बंधन ऊर्जा किसी बंधन का मान धात्विक बंधन से अधिक होता है, यही बात सहसंयोजक बंधन के साथ भी लागू होती है, जबकि धात्विक बंधन में अन्य प्राथमिक बांड की तुलना में कम बंधन ऊर्जा होती है।
- दूसरी ओर आयनिक बॉन्ड एक कमजोर कंडक्टर है, दूसरी ओर सहसंयोजक बॉन्ड एक बहुत कमजोर कंडक्टर है, जबकि मेटालिक बॉन्ड एक मजबूत कंडक्टर है।
- आयनिक बंधन ठोस अवस्था में हो सकते हैं, सहसंयोजक बंधन ठोस, तरल और गैसीय अवस्था में हो सकते हैं, जबकि धात्विक बंधन केवल ठोस अवस्था में हो सकते हैं।
- आयनिक बॉन्ड में कोई लचीला गुण नहीं होता है, यही बात सहसंयोजक बॉन्ड के साथ भी लागू होती है, जबकि मेटालिक बॉन्ड में एक लचीला गुण होता है
- https://journals.aps.org/pr/abstract/10.1103/PhysRev.171.701
- https://www.tandfonline.com/doi/abs/10.1080/00150199208019535
अंतिम अद्यतन: 02 जुलाई, 2023

पीयूष यादव ने पिछले 25 साल स्थानीय समुदाय में भौतिक विज्ञानी के रूप में काम करते हुए बिताए हैं। वह एक भौतिक विज्ञानी हैं जो विज्ञान को हमारे पाठकों के लिए अधिक सुलभ बनाने के लिए उत्सुक हैं। उनके पास प्राकृतिक विज्ञान में बीएससी और पर्यावरण विज्ञान में स्नातकोत्तर डिप्लोमा है। आप उनके बारे में और अधिक पढ़ सकते हैं जैव पृष्ठ.


विभिन्न प्रकार के बांडों के बीच परस्पर क्रिया की जटिलता बिल्कुल आकर्षक है।
इस लेख ने निश्चित रूप से आयनिक, सहसंयोजक और धात्विक बंधों के बारे में मेरा ज्ञान बढ़ाया है। लेखक ने जानकारी प्रस्तुत करने में शानदार काम किया है।
विभिन्न प्रकार के बंधन बनाने के लिए परमाणु एक साथ कैसे जुड़ते हैं, इसकी व्याख्या अच्छी तरह से चित्रित की गई है। इस लेख पर बहुत अच्छा लिखा गया है!
लेख स्पष्ट रूप से लिखा गया है और यहां बहुत सारी मूल्यवान जानकारी है। मैं तुलना तालिका की सराहना करता हूं, यह वास्तव में चीजों को परिप्रेक्ष्य में सेट करती है।
तुलना तालिका वास्तव में बहुत उपयोगी और संक्षिप्त है।
यह स्पष्ट है कि लेखक को विषय की गहरी समझ है और उसने इन सिद्धांतों को प्रभावी ढंग से संप्रेषित किया है।
यह बहुत सूचनाप्रद लेख है। यह आयनिक, सहसंयोजक और धात्विक बंधनों के बीच अंतर को स्पष्ट रूप से समझाता है और रसायन विज्ञान का अध्ययन करने वाले किसी भी व्यक्ति के लिए एक महान संदर्भ है।
मान गया! यह विषय का व्यापक अवलोकन प्रदान करता है।
मेरा मानना है कि यह लेख रसायन विज्ञान के क्षेत्र के छात्रों के लिए बहुत फायदेमंद होगा।
यह व्याख्या अविश्वसनीय रूप से गहन और ज्ञानवर्धक है। मुझे ऐसा लगता है जैसे मैंने सचमुच कुछ सीखा है।